��һ��ѧ����1�ӵ�һ�¸�ϰ��ټ�����
��һ�� ��ʵ��ѧ��ѧ
��һ�� ��ѧʵ���������
���________________ ����_________________
һ��ȷ��ʵ�鰲ȫӦע������⡣
1������ʵ���ҹ���
2���˽ⰲȫ��ʩ��
��ҩƷ��ȫ��ź�ȡ�� ��ʵ������İ�ȫ �������¹ʵĴ���
3��������ȷ�IJ���������
4��ʶ��һЩ���õ�Σ�ջ�ѧƷ�ı�־��
Σ�ջ�ѧƷ��־����ƾ������͡�����ȻҺ�壻ŨH2SO4��NaOH������ʴƷ
[��ϰ1]��������һЩ���õ�Σ��Ʒ��־��װ�˾ƾ��İ�װ��Ӧ����ͼ����( )

A B C D
[��ϰ2].����ʵ�������ȷ���ǣ� ��
A.������Ũ����մ��Ƥ���ϣ������ô���ˮ��ϴ
B.��ʳ����Һ�����ᾧ�Ĺ����У����������г��ֽ϶�������ʱ��ֹͣ����
C.������ƽ���������ϸ���һ����ͬ������ֽ���ٰ��������ƹ������ֽ�ϳ���
D.����ʱ�������ؽ�Һ��ֱ�ӵ���������С�
���������ķ�����ᴿ��
��1������������ᴿ������ѡ��
�����ٹ����������������ʻ���Ҫ�����ֽ⡢������ʱ�ü��ȷ�����һ�����ܣ���һ�����ܣ������ܽ���˷��������߾����ܣ����ܽ�����¶ȵ�Ӱ����ϴ����ؽᾧ�������ɼ���ij���Լ�ʹ���ʳ�ȥ��Ȼ���ٽᾧ�õ���Ҫ���ʡ�
�����ڹ�����Һ����������岻����Һ�壬���ù��˷�������������Һ�壬���ýᾧ��������
������Һ����Һ��������������ܣ����÷�Һ������������һ���ҷе���ϴ���������������һ���ҷе���ѡ��ij�ֻ�ѧ�Լ���ȡ��������
�������������������һ����ϴ��������ѡ��Һ����������Լ���
��2�����ֳ����Ļ����ķ�����ᴿ����
�ٹ��ˣ�����(����)��Һ��ķ��롣������������(����)��Һ����롣
�����е㲻ͬ��Һ������ķ��롣 �ܷ�Һ���������ܵ�Һ�����
����ȡ�����û������һ�������ڻ������ܵ��ܼ����ܽ��ԵIJ�ͬ����һ���ܼ������ʴ�������һ���ܼ�����ɵ���Һ����ȡ������
[��ϰ3]�����¹��˲����У�����ȷ���ǣ� ��
A����ֽӦ����©���ڱڲ�������ˮ��ʪ��ʹ��ֽ��©����֮��û������
B��©���¶˹ܿ�Ӧ�����ձ��ڱ�
C������©���Ĺ���Һ��Һ��Ӧ������ֽ��Ե
D��Ҫ���Ų�����������©�����㵹��Һ
[��ϰ4].�������ѡ�����и������ķ��뷽��������ţ�
��1��ʳ��ˮ����ɳ____________ ��2����ˮɹ��__________________
��3������ˮ_______ ��4������ˮ����ȡ_________��5����CCl4����ˮ�еĵ���ȡ����______
2�����ε��ᴿ��
��1�����εijɷ֣���Ҫ��NaCl��������MgCl2��CaCl2��Na2SO4����ɳ������
��2�����裺�ٽ������ܽ����ˣ�
���ڹ��˺�õ�������Һ�мӹ����Լ�BaCl2(��SO42��)��Na2CO3(��Ca2����������Ba2��)��NaOH(��Mg2��)��Һ����ˣ�
�۵õ���Һ������(��������CO32����OH��)��PH=7�õ�NaCl��Һ��
���������ᾧ�õ����Ρ�
���Լ�˳���ؼ���������Na2CO3��BaCl2֮��������������
3������װ��ע������ټ�����ƿҪ����ʯ������
���¶ȼƵ�ˮ����Ӧλ����ƿ��֧�ܿڴ���
�ۼ����Ƭ��Ŀ���Ƿ�ֹ���У�
������ˮ���¿ڽ����Ͽڳ���
4���ӵ�ˮ����ȡ���ʵ��ʱ��ѡ����ȡ��Ӧ����ԭ��
����ȡ�������뱻��ȡ�����ʷ�Ӧ��
����ȡ����ԭ��Һ�ܼ��������ܡ����ܶȣ���<ˮ<CCl4��
�۱���ȡ����������ȡ���е��ܽ�Ƚ�ԭ�ܼ���
��CCl4��ȡ��ˮ�еĵ�ʱ����Һ��Ϊ���㣬�ϲ�Һ���Ի�ɫ���²�Һ�����Ϻ�ɫ��
�ñ���ȡ��ˮ�еĵ�ʱ����Һ��Ϊ���㣬�ϲ�Һ��Ϊ�Ϻ�ɫ���²�Һ���Ի�ɫ��
[��ϰ5].����ֲ��纣���������к��зḻ�ĵ�Ԫ�أ���Ԫ���Ե����ӵ���ʽ���ڡ�ʵ������Ӻ�������ȡ����������£�(��֪C12+2KI=2KCl+I2)
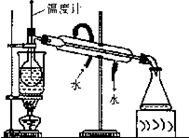
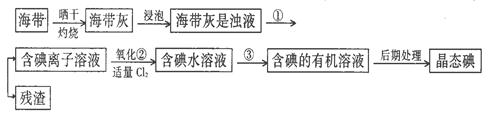
(1)ָ����ȡ��Ĺ������йص�ʵ��������ƣ��� ���� ��
(2)��ȡ��Ĺ����У��ɹ�ѡ����л��Լ���( )
A�������ƾ� B��CCl4���� C���͡�����
(3)�Ӻ�����л��ܼ�����ȡ��ͻ����л��ܼ�������Ҫ�����������(Ϊ��ֹ����������ʵ���в���ˮԡ����)��ָ����������ʵ��װ���еĴ���(����ͼ)
�� ���� ��
(4)��֪���ھƾ��е��ܽ�ȱ���ˮ�еĴ�ö࣬�ܲ����þƾ�����ȡ��ˮ�еĵ� ����ܡ����ܡ�������������
�������ӵļ��飺
��SO42����[�ȼ����ᣬ�ټ�BaCl2��Һ���� ]����а�ɫ������ԭ��Һ��һ������SO42����
Ba2����SO42����BaSO4��
��Cl�������ȼ�ϡ���ᣬ�ټ�AgNO3��Һ���飩����а�ɫ�������ɣ�ԭ��Һ��һ������Cl����
Ag����Cl����AgCl��
��CO32������ϡ������飩�ȼ�ϡ���ᣬ��������ɫ��ζ����ʹ����ʯ��ˮ����ǵ����壬��ԭ��Һ��һ������CO32����
[��ϰ6].Ϊ�˳�ȥ������Ca2����Mg2����SO42-����ɳ���ɽ���������ˮ�����ˣ�Ȼ������������������������ȷ�IJ���˳���ǣ��� ����
�ٹ��ˡ��ڼӹ�����NaOH��Һ���ۼ��������ᡡ�ܼӹ���Na2CO3��Һ���ݼӹ���BaCl2��Һ
A���٢ܢڢݢۡ����� B���ܢ٢ڢݢ� C���ݢܢڢ٢ۡ�����D���ݢڢܢ٢�
�ڶ��� ��ѧ������ʵ���е�Ӧ��
1�����ʵ�����n���ǹ��ʵ�λ����7������������֮һ��
2������µĻ�ѧ���ţ�

3��������֮��Ĺ�ϵ��
��ʽ��n=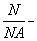 ��ʽ��n=
��ʽ��n=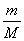 ��ʽ��n=
��ʽ��n=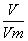 ��ʽ��nB=CB×V
��ʽ��nB=CB×V
��Һϡ���� C��Ũ��×V��Ũ��=C��ϡ��×V��ϡ)
[��ϰ7].ͬ��ͬѹ�£���ͬ�����N2��CO���壬������ͬ��( ��
A�������� B��ԭ���� C������ D��Ħ������
[��ϰ8].�����йذ���ӵ�����NA��˵���������( ��
A��32g����������ԭ����ĿΪNA B��0.5molˮ���е�ԭ����ĿΪ1.5mol
C�������11.2LCO2���еķ�����ĿΪ0.5NA D��2NA��H2���ӵ����ʵ�����2mol
[��ϰ9].����������ȷ���ǣ� ��
A.1 mol H2SO4������Ϊ98 g·mol��1 B.H2SO4��Ħ������Ϊ98 g
C.9.8 g H2SO4����NA��H2SO4���� D.6.02×1022��H2SO4���ӵ�����Ϊ9.8 g
[��ϰ10].��NA��ʾ�����ӵ�����������������ȷ���ǣ� ��
A����״���£�22.4 L H2���е�ԭ����Ϊ1 NA
B�����³�ѹ�£�106 g Na2CO3���е�Na+������Ϊ2 NA
C��ͨ��״���£�1 NA CO2����ռ�е����Ϊ22.4 L
D��0.5 mol/L MgCl2��Һ�У�����Cl-����Ϊ0.5 NA
[��ϰ11].������Һ��Cl����Ũ����50 mL 1 mol/L��MgCl2��Һ�е�Cl����ȵ��ǣ� ��
A. 100 mL 2 mol/L��NaCl��Һ B. 50 mL 0.5 mol/L��AlCl3��Һ
C. 1 L 0.2 mol/L��KCl��Һ D. 20 mL 0.5 mol/L��CaCl2��Һ
[��ϰ12].�����ʵ����� SO2 �� SO3 ��Ƚϣ����н��۴�����ǣ� ��
A.���ǵķ�����Ŀ֮���� 1��1 B.���ǵ���ԭ�� ��Ŀ֮��Ϊ 2��3
C.���ǵ�����֮��Ϊ 1��1 D.��������ԭ����Ŀ֮��Ϊ 3��4
[��ϰ13].0.5 L AlCl3��Һ��Al3+Ϊ6.02×1023������AlCl3��Һ�����ʵ���Ũ��Ϊ( ��
A��0.1 mol/L B��2 mol/L C��3 mol/L D��1.5 mol/L
[��ϰ14].��40gNaOH�ܽ���10mlˮ�У���ϡ�ͳ�1L������ȡ��10ml����10ml��Һ�����ʵ���Ũ����( ��
A��1mol/L B��0.01mol/L C��0.1mol/L D��10mol/L
4��һ�����ʵ���Ũ����Һ������
���磺����400mL0.1mol��L��Na2CO3��Һ��
��1�����㣺����ˮNa2CO3 5.3 g�� ��2����������������ƽ������ˮNa2CO3 5.3 g��
��3���ܽ⣺���������ձ�����������
��4��ת�ƣ����ձ��е���Һ��������С�ĵ�������500mL����ƿ�С�
��5�����ݣ���������ƿ�������ˮʱ����̶���2��3cm��ֹͣ��Ϊ�����ˮ��������࣬����
��ͷ�ι�������ˮ����Һ����Һ��������̶�����������������������ݡ�
��6�������������������һ�����ʵ���Ũ�ȵ���Һ��������Ϊ����ƿ���ݻ��ǹ̶��ģ�û�����������������ƿ��
��7����Һע������ƿǰ��ָ������£�������Ϊ����ƿ������ը�ѣ�ͬʱ��Һ�¶ȹ���ʹ����ƿ����Ӱ����Һ���Ƶľ�ȷ�ȡ�
��8���ý�ͷ�ιܶ��ݺ���������Һ����ڿ̶���ʱ��Ҫ�ټ�ˮ��������Ϊ��ʱ��������Һճ��ƿ���ϻ�û��ȫ��������Һ����ʱ���ڿ̶��ߣ�����ʱ�ּ�ˮ��ʹ��������Һ��Ũ��ƫ�͡�
��9�������ˮ����ʱ�����˿̶��ߣ����ܽ��������������ߣ���Ӧ�������ơ�
��10�����ҡ��ʱ��С���������Σ������ټ�ˮ���̶ȣ������������ƣ�������Ϊ�������ļ�����Һ�к������ʣ���ʹ��������Һ��Ũ��ƫ�͡�
��11�������ܽ��ת��������ƿʱ����������������ˮ���ձ���������ϴ��2��3�Σ�����ϴ��Һһ����������ƿ��������Ϊ�ձ�����������ճ���������ʣ�ֻ���������ܾ����ܵذ�����ȫ��ת�Ƶ�����ƿ����
���������ɹ�ʽ֪���������ʵ����ʵ������ٻ�ʹ��Һ�������IJ���������ʹcƫ�ͣ���֮ƫ�ߡ�
[��ϰ15].ʵ��������0.5 mol/L��NaOH��Һ500 mL�����������������ձ�����100 mL��Ͳ����1000 mL����ƿ����500 mL����ƿ���ݲ���������������ƽ�������룩
(1)������ʱ������ʹ�õ�������____________������ţ�����ȱ�ٵ�����_____________________����ʵ���������õ��������������÷ֱ���___________��___________
�ơ�ʹ������ƿǰ������е�һ��������_________��
�ǡ�����ʱ��һ����Է�Ϊ���¼������裺�ٳ������ڼ��㡢���ܽ⡢��ҡ�ȡ���ת�ơ���ϴ �ӡ��߶��ݡ�����ȴ����ȷ�IJ���____________________________
�ȡ������ƹ����У�������������ȷ�����в������������ƫ�ߵ��� ��ƫ��
��δϴ���ձ��������� ��δ��NaOH��Һ��ȴ�����¾�ת�Ƶ�����ƿ��
������ƿ�����������������ˮ �ܶ���ʱ��������ƿ�Ŀ̶�����
�ݶ���ʱ��������ƿ�Ŀ̶�������ҡ����Һ����Һ����ڿ̶��ߣ��ٲ���ˮ
5����ҺŨ�ȵ���ؼ��㣺
����������W%�� �����ʵ���Ũ��C ��CŨVŨ��CϡVϡ ��ע�ⵥλͳһ�ԣ�
����������W%�����ʵ���Ũ��C�Ĺ�ϵ��C=1000��W%/M����ѵ�λΪg/cm3��
[��ϰ16].��30 mL 0.5 mol/L NaCl��Һ��ˮϡ�͵�500 mL��ϡ�ͺ���Һ��NaCl��������Ũ��Ϊ
A��0.03 mol/L B��0.3 mol/L C��0.05 mol/L D�� 0.04 mol/L
������� ���ܲ� ����ƴ�� ��ߵ���
�ڶ�ƪ���ս̰���л�ѧ����һ֪ʶ�㸴ϰ ��һ�´�ʵ��ѧ��ѧ
��һ�´�ʵ��ѧ��ѧ
��һ�ڻ�ѧʵ���������
һ����ѧʵ�鰲ȫ
1. ����ʵ���ҹ���2. �˽ⰲȫ��ʩ��
��1�����ж������ʵ��ʱ��Ӧ��ͨ����н��У���ע���β�������ʵ����������ջ��ȼ�ȣ���������ȼ�ױ������ʵ��ʱӦע���鴿��β��Ӧȼ�յ������ʵ�������
��2����������ҽ��������
��3��Ũ������ʵ��̨�ϣ�����Na2CO3 ����NaHCO3���кͣ�����ˮ����ɾ���Ũ��մ��Ƥ���ϣ������ø�Ĩ����ȥ������ˮ�徻��Ũ�ὦ������Ӧ����ϡNaHCO3��Һ��ϴ��Ȼ����ҽ��������
��4��Ũ������ʵ��̨�ϣ�����ϡ�����кͣ�Ȼ����ˮ����ɾ���Ũ��մ��Ƥ���ϣ������ô���ˮ��ϴ����Ϳ��������Һ��Ũ������У���ˮϴ��������������Һ��ϴ��
��5���ơ���ʧ������ɳ���˸ǡ�
��6���ƾ���������ȼ�л���С���ʧ��ӦѸ����ʪĨ���˸ǡ�
3. ������ȷ�IJ������������磬����������ҩƷ��ʹ�á����ȷ����������ռ������ȡ�
���������ķ�����ᴿ

�������Ӽ���

��.����
ע�����Ϊ��ʹ���ʳ�����������Լ������ǡ�����������Ӧ�ǡ������������������Լ������ں��������б��ڳ�ȥ��
�ڶ��� ��ѧ������ʵ���е�Ӧ��
һ�����ʵ����ĵ�λ����Ħ��
1.���ʵ�����n���DZ�ʾ����һ����Ŀ���ӵļ������������
2.Ħ����mol��: �Ѻ���6.02 ×1023�����ӵ��κ����Ӽ������Ϊ1Ħ����
3.�����ӵ�����
��6.02 X1023mol-1���������ӵ�������
4.���ʵ��� �� ������������Ŀ/�����ӵ����� n =N/NA
5.Ħ��������M��
(1) ���壺��λ���ʵ��������������е�������Ħ������.��2����λ��g/mol �� g..mol-1
(3) ��ֵ�����ڸ����ӵ����ԭ����������Է�������.
6.���ʵ���=���ʵ�����/Ħ������ ( n = m/M )
��������Ħ�����
1.����Ħ�������Vm��
��1�����壺��λ���ʵ�����������ռ�������������Ħ�����.
��2�����L/mol
2.���ʵ���=��������/����Ħ�����n=V/Vm
3.��״����, Vm = 22.4 L/mol
�������ʵ����ڻ�ѧʵ���е�Ӧ��
1.���ʵ���Ũ��.
��1�����壺�Ե�λ�����Һ����������B�����ʵ�������ʾ��Һ��ɵ�����������������B�����ʵ�Ũ�ȡ�
��2�����mol/L
��3�����ʵ���Ũ�� �� ���ʵ����ʵ���/��Һ����� CB = nB/V
2.һ�����ʵ���Ũ�ȵ�����
��1������ԭ��:������������Һ����������ʵ����ʵ���Ũ�ȣ����й����ʵ���Ũ�ȼ���ķ���������������ʵ�������������������ڽ��������ܼ�ϡ��Ϊ�涨�����,�͵������Ƶ���Һ.
��2����Ҫ����
a.�����Ƿ�©ˮ.
b.������Һ 1����.2����.3�ܽ�.4ת��.5ϴ��.6����.7ҡ��.8������Һ.
ע�����A ѡ������������Һ�����ͬ������ƿ. B ʹ��ǰ�������Ƿ�©ˮ. C ����������ƿ��ֱ���ܽ�. D �ܽ������Һ����ȴ������ʱ��ת��. E ����ʱ����Һ����̶���1��2cmʱ���õιܣ���ƽ�ӷ��۲��ˮ��Һ����ʹ���̶�����Ϊֹ.
3.��Һϡ��
C(Ũ��Һ)·V(Ũ��Һ) =C(ϡ��Һ��·V(ϡ��Һ)
