必修二化学方程式
第一章 物质结构 元素周期律
1、Li与O2反应(点燃):4Li + O2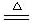 2Li2 O
2Li2 O
Na与O2反应(点燃): 2Na+O2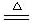 Na2O2
Na2O2
Na与H2O反应:2Na+2H2O===2NaOH+H2↑
K与H2O反应: 2K+2H2O===2KOH+H2↑
2、卤素单质F2、Cl2、Br2、I2与氢气反应:
F2 + H2 === 2HF Cl2 + H2=== 2HCl
Br2 + H2=== 2Br I2 + H2=== 2HI
3、卤素单质间的置换反应:
(1)氯水与饱和溴化钠、氯水与饱和碘化钠溶液反应:
① Cl2+2NaBr===Br2+2NaCl
② Cl2+2NaI===I2+2NaCl
(2)溴水与碘化钠溶液反应:Br2+2NaI===I2+2NaBr
4、Mg与H2O反应:Mg+2H2O === Mg(OH)2+H2↑
Al与HCl反应: 2Al+6HCl===2AlCl3+3H2↑
Mg与HCl反应: Mg+2 HCl === MgCl2+ H2↑
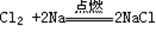 5、Na与Cl2反应(点燃): 6、用电子式表示氯化氢的形成过程:
5、Na与Cl2反应(点燃): 6、用电子式表示氯化氢的形成过程: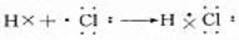
第二章 化学反应与能量
1、Ba(OH)2?8H2O与NH4Cl的反应 :
Ba(OH)2·8H2O+2NH4Cl==BaCl2+2NH3↑+10H2O
2、原电池原理
典型的原电池(Zn-Cu原电池)
负极(锌):Zn-2e-===Zn2+(氧化反应)
正极(铜):2H++2e-===H2↑(还原反应)
电子流动方向:由锌经过外电路流向铜。
总反应离子方程式:Zn+2H+===Zn2++H2↑
3、H2O2在催化剂作用下受热分解:2H2O2 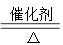 2H2O+O2↑
2H2O+O2↑
4、Na2SO4与CaCl2反应:Na2SO4+CaCl2===CaSO4↓+Na2CO3
5、高炉炼铁:2C + O2 === 2CO
Fe2O3 + 3CO ==2Fe + 3CO2
第三章 有机化合物
1、甲烷的主要化学性质
(1)氧化反应(与O2的反应):CH4(g)+2O2(g) CO2(g)+2H2O(l)
CO2(g)+2H2O(l)
(2)取代反应(与Cl2在光照条件下的反应,生成四种不同的取代物):
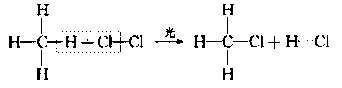

2、乙烯的主要化学性质
(1)氧化反应(与O2的反应):C2H4+3O2 2CO2+2H2O
2CO2+2H2O
(2)加成反应((与Br2的反应): 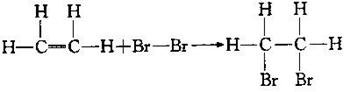
(3)乙烯还可以和氢气、氯化氢、水等发生加成反应:
CH2=CH2 + H2 CH3CH3
CH3CH3
CH2=CH2+HCl CH3CH2Cl(一氯乙烷)
CH3CH2Cl(一氯乙烷)
CH2=CH2+H2O CH3CH2OH(乙醇)
CH3CH2OH(乙醇)
 (4)聚合反应:
(4)聚合反应:
(乙烯制聚乙烯)①
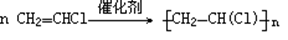 (氯乙烯制聚氯乙烯)② 3、苯的主要化学性质:
(氯乙烯制聚氯乙烯)② 3、苯的主要化学性质:
(1)氧化反应(与O2的反应):2C6H6+15O2 12CO2+6H2O
12CO2+6H2O
(2)取代反应:

 ① 与Br2的反应: + Br2
① 与Br2的反应: + Br2 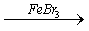 + HBr
+ HBr
② 苯与硝酸(用HONO2表示)发生取代反应,生成无色、不溶于水、有苦杏仁气味、密度大于水的油状液体——硝基苯。反应方程式:
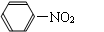
 + HONO2
+ HONO2  + H2O
+ H2O
(3)加成反应

 用镍做催化剂,苯与氢发生加成反应: + 3H2
用镍做催化剂,苯与氢发生加成反应: + 3H2 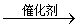
4、乙醇的重要化学性质
(1)乙醇与金属钠的反应:2CH3CH2OH+2Na 2CH3CH2ONa+H2↑
2CH3CH2ONa+H2↑
(2)乙醇的氧化反应
①乙醇的燃烧:CH3CH2OH+3O2 2CO2+3H2O
2CO2+3H2O
②乙醇的催化氧化反应: 2CH3CH2OH+O2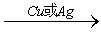 2CH3CHO+2H2O
2CH3CHO+2H2O
③乙醇在常温下的氧化反应:
CH3CH2OH CH3COOH
CH3COOH
5、乙酸的重要化学性质
(1)乙酸的酸性
①乙酸能使紫色石蕊试液变红
②乙酸能与碳酸盐反应,生成二氧化碳气体
利用乙酸的酸性,可以用乙酸来除去水垢(主要成分是CaCO3):
2CH3COOH+CaCO3 (CH3COO)2Ca+H2O+CO2↑
(CH3COO)2Ca+H2O+CO2↑
乙酸还可以与碳酸钠反应,也能生成二氧化碳气体:
2CH3COOH+Na2CO3 2CH3COONa+H2O+CO2↑
2CH3COONa+H2O+CO2↑
上述两个反应都可以证明乙酸的酸性比碳酸的酸性强。
(2)乙酸的酯化反应
①反应原理(与乙醇的反应):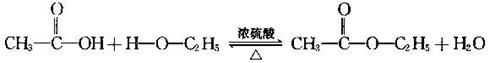
乙酸与乙醇反应的主要产物乙酸乙酯是一种无色、有香味、密度比水的小、不溶于水的油状液体。
6、①蔗糖水解反应:C12H22O11+H2O→C6H12O6+C6H12O6
②淀粉(纤维素)水解反应: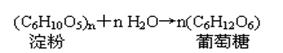
③油脂的重要化学性质——水解反应:
a)油脂在酸性条件下的水解:油脂+H2O 甘油+高级脂肪酸
甘油+高级脂肪酸
b)油脂在碱性条件下的水解(又叫皂化反应):
油脂+H2O 甘油+高级脂肪酸
甘油+高级脂肪酸
蛋白质+H2O 各种氨基酸
各种氨基酸
第四章 化学与可持续发展
1、HgO受热分解:2HgO 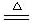 2Hg + O2↑
2Hg + O2↑
Ag2O受热分解:2Ag2O 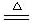 4Ag + O2↑
4Ag + O2↑
2、CO还原Fe2O3:Fe2O3 + 3CO  2Fe +3CO2 (高炉炼铁)
2Fe +3CO2 (高炉炼铁)
① C 还原ZnO :2 ZnO + C  2 Zn +CO2↑
2 Zn +CO2↑
② C 还原MgO : MgO +C  Mg + CO↑
Mg + CO↑
③ Al 还原Fe2O3(铝热反应): Fe2O3 + 2Al  2Fe + Al2O3
2Fe + Al2O3
④ Fe还原CuSO4:CuSO4 + Fe ==== FeSO4 +Cu (湿法炼铜)
3、电解
①电解NaCl:2NaCl(熔融)  2Na +Cl2↑
2Na +Cl2↑
②电解MgCl2: MgCl2(熔融)  Mg +Cl2↑
Mg +Cl2↑
③电解Al2O3:2Al2O3(熔融)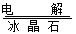 4Al+ 3O2↑
4Al+ 3O2↑
4、石油的催化裂化
例如:C4H10 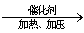 C2H4+ C2H6
C2H4+ C2H6
C16H34 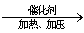 C8H18+C8H16
C8H18+C8H16
C8H18 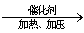 C4H10 +C4H8
C4H10 +C4H8
C4H10 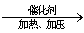 CH4+C3H6
CH4+C3H6
第二篇:化学必修一,第三单元方程式总结
第三章 金属及其化合物化学方程式总结
完成下列反应方程式,如果是离子反应的,写出离子反应方程式,如果有化合价升降的,标出双线桥。
1、镁与氧气的反应
2、*钠在氯气中燃烧
3、铁与单质硫共热
4、镁与盐酸溶液的反应
5、铁与稀硫酸的反应
6、铝与硫酸铜溶液的反应
7、铜与硝酸银溶液的反应
8、钠与氧气在常温下的反应
9、钠与氧气在加热条件下的反应
10、钠与水的反应
11、过量钠放入盐酸溶液中能发生的两个反应
12、少量钠放入硫酸铜溶液中发生的两个反应
13、氧化钠与水的反应
14、过氧化钠与水的反应
15、氧化钠与二氧化碳的反应
16、过氧化钠与二氧化碳的反应
17、氢氧化钠溶液中通入少量的二氧化碳
18、*氢氧化钠溶液中通入过量的二氧化碳
19、氧化钠与稀盐酸的反应
20、过氧化钠与稀盐酸的反应
21、*碳酸钠与少量稀盐酸的反应
22、碳酸钠与过量稀盐酸的反应
23、碳酸氢钠与稀盐酸的反应
24、碳酸钠与石灰水的反应
25、*少量碳酸氢钠与石灰水的反应
26、*过量碳酸氢钠与石灰水的反应
27、碳酸氢钠与氢氧化钠溶液的反应
28、碳酸钠溶液与氯化钙溶液的反应
29、碳酸钠溶液中通入足量的二氧化碳气体
30、碳酸氢钠固体受热分解
31、铝在放入空气中发生的反应
32、铝与稀盐酸的反应
33、铝与氢氧化钠溶液的反应
34、氧化铝与稀盐酸的反应
35、氧化铝与氢氧化钠溶液的反应
36、氢氧化铝与稀盐酸的反应
37、氢氧化铝与氢氧化钠溶液的反应
38、硫酸铝与氨水的反应
39、氢氧化铝受热反应
40、*偏铝酸钠与稀盐酸的反应
41、*偏铝酸钠溶液中通入过量的二氧化碳
42、偏铝酸钠与氯化铝溶液的反应
43、铁在纯氧气中点燃
44、铁与高温水蒸气的反应
45、*氧化亚铁在空气中被氧化为四氧化三铁
46、氧化铁与盐酸溶液的反应
47、氧化亚铁与稀盐酸的反应
48、四氧化三铁与稀盐酸的反应
49、氯化铁与氢氧化钠溶液的反应
50、硫酸亚铁与氢氧化钠溶液的反应
51、氢氧化亚铁被氧化为氢氧化铁
52、氢氧化亚铁与盐酸溶液的反应
53、氢氧化铁与稀盐酸的反应
54、氢氧化铁受热分解
55、*氢氧化亚铁隔绝空气受热分解
56、氯化铁溶液中加入铁粉
57、氯化铁溶液中加入铜片
58、氯化亚铁溶液中加氯水
