ʵ��һ ����������ϰ
һ��������ƽ������ϰ
��һ��ʵ��ԭ��
�ܸ�ԭ��
������ʵ�鲽��
��ȡ0.5-0.6g NaCl���ݡ�
1������������ྻ��С�ձ�����̨���ϴֳ���������������ƽ��ȷ�Ƴ����������ֱ��¼��������m0��m0�� ��
2��ȡһ������ྻ�ij���ƿ����̨���ϴֳ���������Ȼ�����Լ1.5g����������ƽ��ȷ�Ƴ�����������¼��������m1��
3��ת��0.5-0.6g NaCl����һ���ѳ�����С�ձ��У���������¼����ƿ��ʣ������������m2������ͬ�ķ������ٳƳ�0.5-0.6g��NaCl�ڵڶ����ѳ�����С�ձ��У���������¼����ƿ��ʣ������������m3��
4���ֱ�ȷ������������������С�ձ����ֱ��¼������Ϊm01��m02��
������ʵ�����ݼ�¼�ʹ���
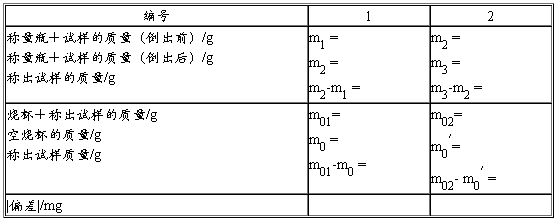
�����ζ���������������ϰ
��һ��ʵ��ԭ��
����ͬ��ǡ��ָʾ���£���Ũ��һ����NaOH��HCl��ζ�ʱ�������ĵ������VHCl/VNaOH�ǹ̶��ġ���ˣ���ѵ��ѧ���ĵζ�����������������ȷ�ж��յ��������
������ʵ�鲽��
1��������Һ������
��1��0.1mol/L NaOH��Һ������
��̨�ӳ�ȡ2g NaOH�������ձ��У���ˮ�ܽ��ϡ����Լ500mL�����ȡ�
��2��0.1mol/L HCl��Һ������
����Ͳ��ȡ6 mol/L HClԼ8.5mL����500mL�Լ�ƿ�У���ˮϡ����Լ500mL��ҡ�ȡ�
2�� HCl��NaOH��Һ�����VHCl/VNaOH�IJⶨ
����ʽ�ζ��ܻ����ų�20mLHCl����ƿ�У���1��2�η�̪����NaOH��Һ�ζ�����Һ����ɫ����Ӳ���ɫΪ�յ㡣��ȡ��ȷ��¼HCl��NaOH�������ƽ�вⶨ���Σ�����VHCl/VNaOHֵ��
������ʵ�����ݼ�¼�ʹ���
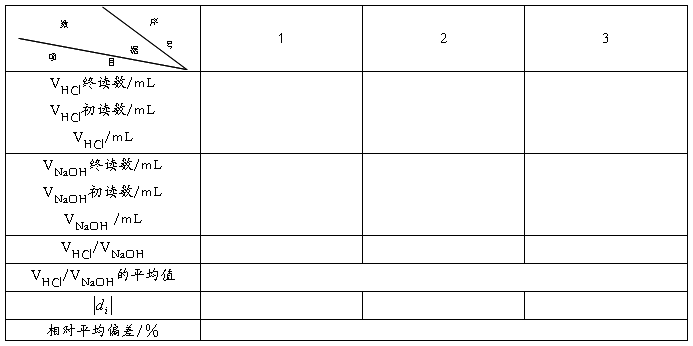
ʵ��� �л���Ħ�������IJⶨ
һ��ʵ��ԭ��
���л������cKa>10-8ʱ������NaOH����Һȷ�ζ�����ӦʽΪ��
nNaOH + HnA=NanA + nH2O
��ѧ������ʱ����Һ�������ԣ���ѡ�÷�̪��ָʾ�����յ㣺��ɫ����ɫ����Ӳ��ʡ�
����ʵ�鲽��
1��0.1mol/L NaOH��Һ�����ƺͱ궨
��̨�ӳ�ȡ1g NaOH�������ձ��У���ˮ�ܽ��ϡ����Լ250mL�����ȡ�
�ò����ȷ��ȡ1.8~2.2g�ڱ����������1����С�ձ��У���ˮ�ܽ���ݳ�100mL��ҡ�ȡ�
��25mL��Һ����ȡ1���ڱ������������Һ����ƿ�У�����1��2�η�̪���ô��궨��NaOH��Һ�ζ�����ɫ����Ӳ���ɫΪ�յ㣬��¼���ĵ�NaOH�����ƽ�б궨3�Σ�����NaOHŨ�Ⱥ����ƽ��ƫ�
2������Ħ�������IJⶨ
ȷ����AR H2C2O4·2H2O 0.6~0.8g 1����С�ձ��У���ˮ�ܽ���ݳ�100mL��ҡ�ȡ�
��25mL��Һ����ȡһ�ݲ�����Һ����ƿ�У�����1��2�η�̪����NaOH��Һ�ζ�����ɫ����Ӳ���ɫΪ�յ㣬��¼���ĵ�NaOH�����ƽ�еζ�3�Σ��������Ħ�����������ƽ��ƫ�
����ʵ�����ݼ�¼�ʹ���
���ڰ��������ġ���������ʵ�鱨�����塱
ʵ���� �Ȼ���е������IJⶨ����ȩ����
һ��ʵ��ԭ��
NH4+ Ka=5.6×10-10��������NaOH��Һֱ�ӵζ�������ȩ������������¶�����Ӧ��
4 NH4+ + 6 HCHO ==== (CH2)6 N4 H+ + 3 H+ + 6 H2O
�������ӻ������Ǽ��İ���(CH2)6 N4 H+��Ka==7.1×10-6���������H+��������NaOH��Һ�ζ���������ʱ����Ϊ(CH2)6 N4����Һ�����ԣ���ѡ�÷�̪Ϊָʾ����
����ʵ�鲽��
1����ȩ��Һ�Ĵ���
��ʵ�����ṩ�ļ�ȩ�Լ��м���2�η�ָ̪ʾ������0.10mol/L NaOH�к�����ɫ��
2��0.1mol/LNaOH��Һ��������궨
��̨�ӳ�ȡ1g NaOH�������ձ��У���ˮ�ܽ��ϡ����Լ250mL�����ȡ�
ȷ��ȡ1.8~2.2g�ڱ����������1����С�ձ��У���ˮ�ܽ���ݳ�100mL��ҡ�ȡ�
��25mL��Һ����ȡһ���ڱ������������Һ����ƿ�У�����1��2�η�̪���ô��궨��NaOH�ζ�����ɫ����Ӳ���ɫΪ�յ㣬��¼���ĵ�NaOH�����ƽ�б궨3�Ρ�
3�������к������IJⶨ
��1��ȷ��ȡNH4Cl����0.5~0.75g 1����С�ձ��У���ˮ�ܽ������100 mL��ҡ�ȡ�
��2����ȡ25.00mL��Һ1������ƿ�У�����1~2�μ���ָʾ������0.1mol/L NaOH�к�����ɫ����ԭ��Ϊ��ɫ���ؼ�NaOH������8mL 1:1��ȩ��Һ���ټ�1-2�η�ָ̪ʾ�������ҡ�ȡ�����1min����0.1 mol/L NaOH��Һ������Һ����ɫΪ�յ㣬��¼���ĵ�NaOH��������������е��İٷֺ�����ƽ�вⶨ3�Ρ�
ʵ���� ����ˮӲ�ȵIJⶨ
һ��ʵ��ԭ��
��pH=10�İ��Ի�����Һ�У��Ը���T(EBT)Ϊָʾ����ָʾ����ơ�þ�����γɺ�ɫ��������EDTA��Һ�ζ���þ����������ˮ����Ӳ�ȣ��յ�ʱ��ָʾ����ȡ������Һ������ָʾ������ɫ����
�ζ�ǰ�� EBT + Mg = Mg-EBT��
(��ɫ) (��ɫ)��
�ζ�ʱ�� EDTA + Ca = Ca-EDTA ��EDTA + Mg = Mg-EDTA
(��ɫ)�� (��ɫ)
�յ�ʱ�� EDTA + Mg-EBT = Mg-EDTA + EBT��
(��ɫ) (��ɫ)��
ˮ���д���Fe3+��Al3+ʱ���������Ҵ����ڱΣ�Cu2+��Pb2+��Zn2+����Na2S��KCN�ڱΡ�
ˮ����Ӳ�ȱ�ʾ�����ж��֣���ʵ����m mol·L-1 (CaCO3)��ʾ
����ʵ�鲽��
1��0.02mol·L-1EDTA����Һ�����ƺͱ궨
��1����ȡEDTA������2g���ձ��У���ˮ�ܽ��ϡ����Լ250 mL��
��2��ȷ��ȡ��CaCO3 0.2~0.25g 1����С�ձ��У���Լ2~3mLˮʪ����ϱ����������μ�1��1 HCl ��CaCO3�ܽ���ȫ��������100mL��ҡ�ȡ�
��3����ȡ25.00mLCa2+��Һ����ƿ�У��������Ҵ���2mL�����Ի�����Һ15mL��2��3�θ���T����0.02mol·L-1EDTA�ζ�����Һ���Ϻ��ɴ���ɫΪ�յ㣬��¼���ĵ�EDTA�����ƽ�б궨���Σ�����EDTA��Һ��ȷŨ�ȡ�
2��EDTA��Һ��ϡ��
ȷ��ȡ�ѱ궨���˵�EDTA��Һ25.00mL��250mL����ƿ�У�ϡ�����̶ȣ�������ȷŨ�ȡ�
3������ˮӲ�ȵIJⶨ
ȡˮ��25.00mL����ƿ�У�����5mL 1:1���Ҵ�����10mL���Ի�����Һ��2��3�θ���T������ϡ�͵�EDTA��Һ�ζ�����Һ���Ϻ�ɫ��ɴ���ɫΪ�յ㣬��¼���ĵ�EDTA�����ƽ�еζ����Σ�����ˮ����Ӳ�ȡ�
ʵ���� �������⺬���IJⶨ
һ��ʵ��ԭ��
Na2C2O4�DZ궨KMnO4��õĻ����ʡ��ζ���ӦΪ��
5C2O42- + 2MnO4- + 16H+ = 10CO2 + 2Mn2+ + 8H2O
��ΪKMnO4��Һ������������������Ϻ�ɫ��ͨ���ݴ�ָʾ�յ㡣�˵ζ���Ҫ�������˵��¶ȣ�75-85�棩����ȣ�0.5~1 mol·L-1�����ζ��ٶȺ���ɫά�ֵ�ʱ�䣨0.5 min����
H2O2��ҽҩ�ϵ������������ø�����ط��ⶨ�京�����ζ���ӦΪ��
5 H2O2 + 2MnO4- + 6H+ = 2Mn2+ + 8H2O + 5O2
����KMnO4��Һ��Ũ�Ⱥ͵ζ������õ���������������Һ�й�������ĺ�����
����ʵ�鲽��
1��0.02mol·L-1KMnO4��Һ�����ƺͱ궨
��1����̨���ϳ�ȡ0.8g KMnO4����������ˮʹ���ܽ⣬ϡ�͵�250mL��
��2��ȷ��ȡ0.6~0.8g������Ļ�Na2C2O4һ���� 100 mL С�ձ��У���ˮ�ܽ������100 mL��ҡ�ȡ�
��3����ȡ25.00mL Na2C2O4��Һ����ƿ�У�����40mL����ˮ��15mL 3mol/L H2SO4������ֱ������ð����Լ75-85�棩�������ô��궨��KMnO4��Һ���еζ�����ʼ�ζ�ʱ���ٶ�����������Һ����Mn2+�����ζ��ٶȿ��ʵ��ӿ졣�ӽ��յ�ʱ��Ӧ�����ζ��ٶȣ�ֱ����ɫ������ڱ��ֲ���Ϊ�յ㣬��¼���ĵ�KMnO4�����ƽ�б궨���Σ�����KMnO4��Һ��ȷŨ�ȡ�
2��H2O2�����IJⶨ
ȷ��ȡ1.00mLŨ��Լ3% H2O2���ں�60mLˮ����ƿ�У���15mL 3mol/L H2SO4��Һ����KMnO4����Һ�ζ�����Һ����ɫ�ڰ�����ڲ���ɫΪ�յ㣬��¼���ĵ�KMnO4�����ƽ�еζ����Σ�����������⺬����mg/mL����
ʵ���� ��ӵ������ⶨͭ����ͭ����
һ��ʵ��ԭ��
����������Һ�У�pH=3��4����Cu2+�������KI���ã�����CuI������I2��������I2�Ե���Ϊָʾ������Na2S2O3����Һ�ζ���
2Cu2+ + 4I- = 2CuI�� + I2
I2 + 2S2O32- = 2I- + S4O62-
CuI����ǿ������I3-���ֻ�ʹ���ƫ�͡�ͨ���İ취���ڽ��յ�ʱ�����������Σ���CuIת��Ϊ�ܽ�ȸ�С��CuSCN�������ڳ�����ת�������У������ĵⱻ�ͷų�������
��������Ӧ�ڽӽ��յ�ʱ���룬����SCN-�ỹԭ�������ڵ�I2����ʹ�ⶨ���ƫ�͡���Һ��pHֵӦ������3.0��4.0֮�䡣��ȹ��ͣ�Cu2+��ˮ�⣻��ȹ��ߣ���I-�ױ������е�������ΪI2��
����ʵ�鲽��
1��Na2S2O3����Һ�����ƺͱ궨
��1����̨���ϳ�ȡ7.5g Na2S2O3·5H2O��5g Na2S2O3����������ˮʹ���ܽ⣬����Լ0.1gNa2CO3���ܽ⣬ϡ�͵�300mL��
��2��ȷ��ȡ������Ļ�K2Cr2O7 0.4~0.6gһ�����ձ��У���ˮ�ܽ������100ml��
��3��ȷ��ȡ25.00mL K2Cr2O7����Һ�ڵ���ƿ�У���5mL 3mol/L H2SO4��15mL 10% KI������ҡ���ڰ�������5min����ˮ��ϴ������ƿ�ڣ��ټ�100mLˮϡ�͡���Na2S2O3��Һ�ζ���dz����ɫ�����2mL����ָʾ������������������ζ�����Һ��ɫ��ʧ����Ϊ��ɫΪ�յ㡣ƽ�б궨3�Σ�����Na2S2O3��Һ��Ũ�ȡ�
2��ͭ����ͭ�����IJⶨ
��1��ȷ��ȡ2.2~3g CuSO4·5H2O��С�ձ��У�������ˮ�ܽ⣬����3 mol/L H2SO4 4mL����ˮ���ݳ�100 mL��
��2��ȷ��ȡͭ����Һ25.00 mL�ڵ���ƿ�У���ˮԼ50 mL��10%KI��Һ10 mL��ҡ�ȣ�������Na2S2O3 ��Һ�ζ���dz��ɫ������������ټ�3mL����ָʾ�����ζ���dz��ɫ����10mL NH4SCN��Һ��ҡ��2 min�������ζ�����ɫ��ʧ�ʻҰ�ɫ������ɫΪ�յ㡣ƽ�вⶨ3�Σ�����������ͭ������������
ʵ���� �������Ȼ������Ⱥ����IJⶨ��Ī������
һ��ʵ��ԭ��
�����Ի���������Һ�У���K2CrO4Ϊָʾ������AgNO3����Һ�ζ���ש��ɫ AgCrO4����Ϊ�յ㡣����AgNO3����Һ���������������е��Ⱥ�����
����ʵ�鲽��
1��0.05 mol/L AgNO3����Һ��������궨
��1����̨�Ƴ�ȡ2.5 g AgNO3���ձ��У���ˮ�ܽ��ϡ����300 mL��ҡ�ȡ�
��2��ȷ��ȡ������Ļ�NaCl 0.5~0.6gһ�����ձ��У���ˮ�ܽ������100ml��
��3��ȷ��ȡ10.00mL NaCl����Һ����ƿ�У���ˮ40 ml��5%K2CrO4ָʾ��1 mL���ھ������£���AgNO3��Һ�ζ�����ɫΪ�յ㡣ƽ�б궨3�Σ�����AgNO3��Һ��Ũ�ȡ�
2����������
��1��ȷ��ȡʳ������ 0.5~0.6gһ�����ձ��У���ˮ�ܽ������100ml��
��2��ȷ��ȡ10.00mL ������Һ����ƿ�У���ˮ40 ml��5%K2CrO4ָʾ��1 mL���ھ������£���AgNO3��Һ�ζ�����ɫΪ�յ㡣ƽ�еζ�3�Σ�������Ʒ���ȵ�����������
ע�⣺ʣ���AgNO3����Һ������ָ���������У��ζ��ܺ���ƿ�Ȳ�������Ӧ����Na2S2O3��Һ��ϴ����������ˮ��ϴ��
ʵ��� �ڶ����������ȷ��ⶨ��
һ��ʵ��ԭ��
�ڶ�����(o-ph)��pH��2��9 ����Һ����Fe2+�����ȶ��ĺ�ɫ����lg K ��21.3�����Ħ������ϵ���� =1.1×104���䷴Ӧʽ���£�
Fe2+ + 3(o-ph) = Fe(o-ph)3
��ɫ������������շ�λ��510nm������Fe3+�����������ǰ����Ƚ��仹ԭ��Fe2+����������ѡ���Ժܸߣ��൱�ں�����40����Sn2+��Al3+��Ca2+��Mg2+��Zn2+��SiO32-��20��Cr3+��Mn2+��V(V)��PO43-��5��Co2+��Cu2+�Ⱦ������Ųⶨ����ʵ����ñ����߷��ⶨ����
����ʵ�鲽��
1������ϵ����Һ������
��6��100mL������ƿ�У��������ֱܷ����0.0��1.0��2.0��3.0��4.0��5.0mL 100��g/mL������Һ���ֱ����2mL10%�����ǰ���4mL0.15% Phen��8mL10% NaAc��Һ��ÿ��һ���Լ���ҡ�ȡ���ˮϡ�����̶ȣ�ҡ�Ⱥ����10min��
2���������ߵIJⶨ
ȡ����ϵ����Һ3�ţ���1cm��ɫ�����Լ��հף�1�ţ�Ϊ�α���Һ����440��500nm��520��560nm֮�䣬ÿ��10nm��һ������ȣ���500��520nm��ÿ��5nm�ⶨһ������ȡ�����A-���������ߡ��������������ҵ�������ղ�����max��
3�������ߵ�����
��1cm��ɫ�����Լ��հף�1�ţ�Ϊ�α���Һ����������ղ�����510nm���£���������Һ������ȡ��Ժ���������g��Ϊ�����ꡢ�����AΪ�����꣬���Ʊ����ߡ�
4�����������IJⶨ
ȷ��ȡ��Һ����ҵ���ᣩ2ml��100 mL����ƿ�У�������������ɫ������ͬ�����²�������ȣ��ɱ������ϲ���������൱�������������������������ĺ���(g/l)��
�ڶ�ƪ����ѧ������Ҫʵ�齲��
ʵ��һ ������ƽ������ϰ
[ʵ��Ŀ��]
1��ѧϰ������ѧ���Լ��ij���������
2������ȷ���������淶�ؼ�¼ʵ��ԭʼ���ݵķ�����
[ʵ��ԭ��]
1��������ƽ�Ĺ���
������ƽ������һ������ƽ���Ǹ��ݵ����ƽ��ԭ����ֱ�ӳ�����ȫ���̲������롣���ϳ�������ڼ������ڼ��ﵽƽ�⣬��ʾ�����������ٶȿ죬���ȸߡ�������ƽ��֧�е��õ��Ի�Ƭ��ȡ����е��ƽ����觵��ڣ��ò��ѹ��ȡ��������װ�ã���������ʾ����ָ��̶�ʽ��
2��������ƽ��ʹ�÷���
��1��ˮƽ���ڡ��۲�ˮƽ�ǣ���ˮƽ��ˮ��ƫ�ƣ������ˮƽ���ڽţ�ʹˮ��λ��ˮƽ�����ġ�
��2��Ԥ�ȡ���ͨ��Դ��Ԥ�����涨ʱ�������ʾ�����в�����
��3��������ʾ�����ᰴON������ʾ��ȫ���������ֳ���ģʽ0.0000 g�ɳ���������ʱӦ������ƽ�š�
��4��У����ƽ��װ��һ��ʹ��ǰ��Ӧ����ƽ����У������ʱ��ϳ���λ���ƶ��������仯��δ��þ�ȷ��������ƽ��ʹ��ǰһ�㶼Ӧ����У������һ�������У���еĵ�����ƽ������У���ܣ���ɡ�
��6�������������������ʾΪ����ó������ڳ����ϣ�������ƽ�ţ��������ȶ����ɶ��������������ֵ��
��7��ȥƤ����������������������ڳ����ϣ���ƽ��ʾ�����������ٰ����������ʾ�㣬��ȥ��Ƥ�ء����ó������������У��������ĩ״���Һ�壩����������ֱ���ﵽ�����������������ȶ�����ʱ��ʾ���dz�����ľ��������������ϵ�������Ʒ�ÿ�����ƽ��ʾ��ֵ�������������ƽ��ʾ0.0000 g�������������г����ϵ���������������غ�ʱ����ƽ����ʾ�ϲ��߶Σ���ʱӦ������С�غɡ�
��8���������������϶�ʱ���ڻ�ʹ����ƽ���������˻�ʹ����ƽ��һ�㲻�ð�OFF���ر���ʾ����ʵ��ȫ�������ر���ʾ�����жϵ�Դ������ʱ���ڣ�����2 h�ڣ���ʹ����ƽ���ɲ����жϵ�Դ������ʱ��ʡȥԤ��ʱ�䡣
�����첻��ʹ����ƽ��Ӧ���µ�Դ��ͷ��
3����������
���õij���������ֱ�ӳ��������̶������������͵ݼ����������ֱַ�������¡�
��1��ֱ�ӳ�����
ֱ�ӳ�����ֻ�ܳ�����ֱ�ӷ�����ƽ�ϵ���Ʒ����С�ձ��������������ȡ�
��2���̶�����������
�˷��ֳ������������ڳ�����Ҫijһ�̶��������Լ������������ֳ����������ٶȺ��������ڳ��������������ڿ��������ȶ����ڵķ�ĩ״��С��������С����ӦС��0.1 mg���Ա�����������������Ʒ��
�̶�������������ͼ2-3��ʾ��ע�⣺�����������Լ�����ָ��������Ӧ��ţ�dz�ȡ�������Լ����ظ�����������ֱ���Լ���������ָ��Ҫ��Ϊֹ���ϸ�Ҫ��ʱ��ȡ���Ķ����Լ�Ӧ��ȥ����Ҫ�Ż�ԭ�Լ�ƿ�С�����ʱ���ܽ��Լ�ɢ������ƽ�̵���������ĵط����ƺõ��Լ����붨�����ɱ���������ֽ������ֱ��ת������������˼���ν������ת�ơ���

ͼ2-3 �̶����������� ͼ2-4�ݼ�������
��3��������
�ֳƵݼ���������������������ͼ2-4��ʾ���˷����ڳ���һ��������Χ����Ʒ���Լ����ڳ�����������Ʒ����ˮ��������������CO2�ȷ�Ӧʱ����ѡ��˷������ڳ�ȡ�����������������γ���֮����ã���Ҳ�Ʋ�����������������������£�
�ٴӸ���������ֽ������ֽƬ����ס����ƿ��ȡ������ƿ��ע�⣺��Ҫ����ֱָ�Ӵ�����ƿ��ƿ�ǣ���
����ֽƬ��ס����ƿ�DZ�����ƿ�ǣ�����������������Ʒ���Լ���һ��Ϊ��һ����Ʒ������������������ƿ�ǡ�
�۹������ƽ�ţ�������ƿ������ƽ�����룬������ƽ�ţ���������ƿ���������ȷ����m1��
�ܽ�����ƿ����ƽ��ȡ�����ڽ����������Ϸ���бƿ�����ó���ƿ������ƿ���ϲ�ʹ�����������������У�ƿ��ʼ�ղ�Ҫ�뿪�������Ϸ���
�ݵ�����������ӽ����������ɴ�����Ϲ��ƻ����ص�֪��ʱ��һ������ƿ������ƿ�ڣ�һ����ƿ����ֱ��ʹճ����ƿ���ϵ�������س���ƿ��Ȼ��Ǻ�ƿ�ǣ��Ż���ƽȷ��������m2����������֮��(m1-m2)����Ϊ����������m����ʱһ�κ��ѵõ��Ϻ�������ΧҪ������������ظ�������������1��2�Ρ�
�ް��������������ݼ����ɳ������������
[�Լ�������]��
CuSO4�q5H2O
����ƿ��������
������ƽ��220g/0.0001g�����֮һ����150g/0.01(�ٷ�֮һ)
[ʵ�鲽��]
�١�ȡ�������������ڵ�����ƽ�ϳ���0.1mg����¼Ϊm0��m0��
�ڡ�ȡһ��װ���㹻�����Ľྻ������ij���ƿ���ڵ�����ƽ�ϴ��Գ�����������Ȼ�����Լ1g CuSO4�q5H2O���ڷ�����ƽ�Ͼ�ȷ����ʢ��CuSO4�q5H2O�ij���ƿ����¼Ϊm1����ƿ������ƿ�����أ�ת�Ƴ�0.3-0.4g��Ʒ����һ�������У������������Ʒ���㹻��ʱ���ٱ���ƿ�ڣ��߷���ƿ�����Ǻ�ƿ�Ǻɽ�����ƿ�ƿ������Ϸ���ȷ��������¼����ƿ��ʣ����m2����ͬ���ķ�����ת�Ƴ�0.3-0.4g��Ʒ����������¼����ƿ��ʣ������m 2��
�ۡ��ֱ�ȷ��������ʢ��CuSO4�q5H2O�Ĵ���������¼������Ϊm1����m2��
�����±��ĸ�ʽ��¼ʵ�����ݲ�����ʵ������
��1.������ϰ��¼��ʽʾ��

Ҫ�����ƫ��С�ڵ���ǧ��֮�塣
[ע������]
1��������ƽ������������ʹ��ʱע��ϸ�IJ�����
2������ʱ��ϸ�Ľ���Ʒ���Լ�������������У�����������ƽ�ϡ��������������������˱��밴Ҫ�����ã��������ۺ�ʴ������������ʵ��ָ����ʦ��
3��ʵ������Ҫ����ʵ�鱾�ϣ������������ֽƬ�ϡ�
ʵ��� ���ζ�ʵ��
[ʵ��Ŀ��]
1. ��ϰ���ζ��Ļ�������
2. ѧϰ���������ζ��յ���жϷ���
[ʵ��ԭ��]
�ζ������ǽ�һ����֪ȷŨ�ȵı���Һ�μӵ�������������Һ�У�ֱ����ѧ��Ӧ��ȫΪֹ��Ȼ����ݱ���Һ��Ũ�Ⱥ������ñ�����������ݺ�����һ�ַ������ڽ��еζ�����ʱ��һ����Ҫ�����Ƶζ�����Һ����ȷ�ⶨ��Ũ�ȣ���һ����Ҫȷ�����ζ������������ĵζ����������Ϊֹ�������˴˻�������ʵ�顣
�ζ������������ζ�����������ԭ�ζ����������ζ�������ϵζ�������ʵ����Ҫ�������ζ��������ζ�������Һ�����ƺͲ����ζ����������Ϊ��������ϰ�ζ������Ļ���������
���ζ��г������������������Һ��Ϊ�ζ���������Ũ�����ӷ����������������տ����е�ˮ�ֺͶ�����̼���ʴ˵ζ�����ֱ������ȷ��ֻ�������ƽ���Ũ�ȵ���Һ��Ȼ���û����ʱ궨��Ũ�ȡ�
ǿ��HCl��ǿ��NaOH��Һ�ĵζ���Ӧ��ͻԾ��ΧpHԼΪ4~10������һ��Χ�пɲ��ü��ȣ���ɫ��ΧpH3.1-4.4�������죨��ɫ��ΧpH4.4-6.2������̪����ɫ��ΧpH8.0-9.6������������ͼӺ�����ˮ��Һ����ɫ���pHΪ8.3����ָʾ����ָʾ�յ㡣Ϊ���ϸ�ѵ��ѧ���ĵζ���������������ѡ�ü��ȡ���̪����ָʾ����ͨ������������������Һ����ȵIJⶨ��ѧ���������ζ�����Һ�ķ�������ζ��յ�ķ�����
[ʵ���Լ�]��
1��0.1mol/L NaOH 1000mL
2��0.1mol/L HCl 1000mL
3����̪ 0.2%ˮ��Һ
4������ 0.2%ˮ��Һ
5������+�������Һ 0.2%ˮ��Һ
[ʵ�鲽��]
1����0.1mol/L NaOH��Һ��ϴ��ʽ�ζ���2-3�Σ�ÿ����5-10 mL ��Һ��ϴ��Ȼ�ζ��������ʽ�ζ����У��ζ���Һ�������0.00�̶ȡ�
2����0.1mol/L ������Һ��ϴ��ʽ�ζ���2-3�Σ�ÿ����5-10 mL ��Һ��ϴ��Ȼ��������Һ������ʽ�ζ����У��ζ���Һ�������0.00�̶ȡ�
3�����ζ��ܵIJ���: �ɼ�ʽ�ζ����з�NaOH��Һ10-15mL��ƿ�У��ų�ʱ��ÿ����Լ10ml���ٶȣ���ÿ���ӵ���3-4����Һ���ټ�1-2�μ���ָʾ������0.1mol/L ������Һ�ζ�����Һ�ɻ�ɫת��Ϊ��ɫ���ɼ�ʽ�ζ������ٵ�������NaOH��Һ����ʱƿ����Һ�ɳ�ɫ��ת��Ϊ��ɫ��������ʽ�ζ����е���HCl��Һ��ֱ�����ζ���Һ�ɻ�ɫ��ת��Ϊ��ɫ����Ϊ�յ㣬��˷�����ϰ3~5�Ρ�
4���ɼ�ʽ�ζ���ȷ�ų�NaOH��Һ10.00������ƿ�У�����1-2�μ���ָʾ������0.1 mol/L HCl��Һ�ζ���Һ�ɻ�ɫǡ��Ϊ��ɫ��ƽ�вⶨ���ݣ����ݰ�����¼������VHCl/VNaOH�������Լ���%��±1%��Χ�ڣ�����ϸ�
5������Һ����ȡ10.00����0.1 mol/L HCl��Һ��ƿ�У���2-3�η�ָ̪ʾ������0.1 mol/L NaOH��Һ�ζ���Һ����ɫ���˺�ɫ����30���Ӳ���ɫ��Ϊ�յ㡣���ƽ�вⶨ���ݣ�����VNaOH/VHCl�������Լ���%��±1%��Χ�ڣ�����ϸ�
6���ɼ�ʽ�ζ���ȷ�ų�NaOH��Һ10.00������ƿ�У�����1-2�μ���+����̻��ָʾ������0.1mol/L HCl��Һ�ζ���Һ����ɫ����ɫ��Ϊ��ɫ��ƽ�вⶨ���ݣ����ݰ�����¼������VHCl/VNaOH�������Լ���%��±1%��Χ�ڲ���ϸ�
(ע����Լ���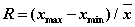 )
)
Ҫ��������ʵ��������һ��ʵ��������Լ�����±1%��Χ�ڡ�
[�����¼]
1��HCl��Һ�ζ�NaOH��Һ��ʵ�鲽��Ϊ4��ָʾ��Ϊ���ȣ�
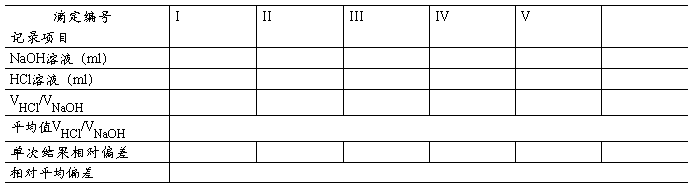
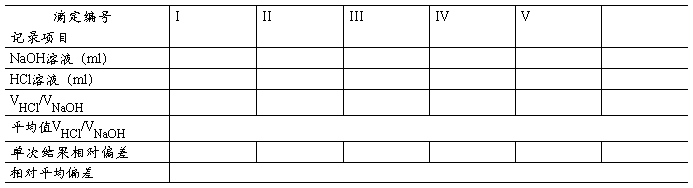
2��NaOH��Һ�ζ�HCl��Һ��ʵ�鲽��Ϊ5��ָʾ��Ϊ��̪��
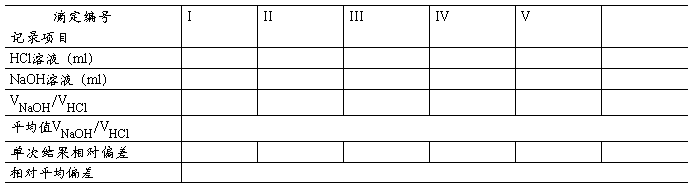
3. HCl��Һ�ζ�NaOH��Һ��ʵ�鲽��Ϊ6��ָʾ��Ϊ����+����̣�
[ע������]
��ʽ�ζ��ܺͼ�ʽ�ζ��ܵ�ʹ�÷�����
