华 南 师 范 大 学 实 验 报 告
学生姓名 学 号
专 业 化学(师范) 年级、班级
课程名称 物理化学实验 实验项目 磁化率的测定
实验类型 :□验证□设计□综合 实验时间 2013 年 10 月 8 日 实验指导老师 彭 彬 实验评分
一、实验目的
①掌握古埃(Gouy)磁天平测定物质磁化率的实验原理和技术。
②通过对一些配位化合物磁化率的测定,计算中心离子的不成对电子数,并判断d电子的排布情况和配位体场的强弱。
二、实验原理
(1)物质的磁性
物质在磁场中被磁化,在外磁场强度H的作用下产生附加磁场,该物质内部的磁感应强度B为:
B=H+4πI=H+4πκH (3-87)
式中,I称为体积磁化强度,物理意义是单位体积的磁矩。式中的κ=I/H称为物质的体积磁化率。I和κ分别除以物质的密度ρ可以得到σ和χ,σ= I/ρ称为克磁化强度;χ=κ/ρ称为克磁化率或比磁化率。χm=κM/ρ称为摩尔磁化率(M是物质的摩尔质量)。这些数据都可以从实验测得,是宏观磁性物质。在顺磁、反磁性研究中常用到χ和χm,铁磁性研究中常用到I、σ。
不少文献中按宏观磁性物质,把物质分成反磁性物质、顺磁性物质和铁磁性物质以及亚铁磁性物质、反铁磁性物质几类。其中,顺磁性物质的χm>0而反磁性物质的χm<0。
(2)古埃法(Gouy)测定磁化率
古埃法是一种简便的测量方法,主要用在顺磁测量。简单的装置包括磁场和测力装置两部分。调节电流大小,磁头间距离大小,可以控制磁场强度大小。测力装置可以用分析天平。为了测量不同温度的数据,要使用变温、恒温和测温装置。
样品放在一个长圆柱形玻璃管内,悬挂在磁场中,样品管下端在磁极中央处,另一端则在磁场强度为零处。
样品在磁场中受到一个作用力。
dF=κHAdH
式中,A表示圆柱玻璃管的截面积。
样品在空气中称量,必须考虑空气修正,即
dF=(κ-κ0)HadH
κ0表示空气的体积磁化率,整个样品的受力是积分问题:
F=∫(κ-κ0)HAdH=1/2(κ-κ0)A(H2-H02) (3-88)
因H0<<H,且忽略κ0,则
F=1/2κAH 2 (3-89)
式中,F可以通过样品在有磁场和无磁场的两次称量的质量差来求出。
F=(△m样-△m空) g (3-90)
式中,△m样为样品管加样品在有磁场和无磁场时的质量差;△m空为空样品管在有磁场和无磁场时的质量差;g为重力加速度。
则有,κ= AH
而χm=ρ=,h为样品高度,A为样品管截面积,m样品为样品质量。 ρAh
M 2χm=== (3-91) ρ m样品 m样品H2
只要测量样品重量的变化、磁场强度H以及样品高度h,即可根据式(3-91)计算样品的摩尔磁化率。
在实际工作中是采用已准确知道磁化率数值的校准样品来标定磁场,根据式(3-91)
=× × × χ校准剂 (△m校准剂-△m空) m样品 M校准剂 h校准剂
△-△mm校准剂 M样品 h样品 χ校准剂 (3-92) 空) χ样品 = (m样品(△m校准剂-△m空)m样品 M校准剂 h校准剂
常用的校准样品有(NH4)2SO4FeSO4·6H2O(莫氏盐),HgCo(CNS)4、Ni(en)3S2O3。其中,(NH4)2SO4FeSO4·6H2O的磁化率符合公式
χ = ×10-4 (3-93) T+1
式中,T是绝对温度。
(3)简单络合物的磁性与未成对电子
对于第一过渡系列元素络合物,它们的磁矩实验值大多符合
μm=(n+2) μB (3-94)
式中,n是分子中未成对电子数;μB是电子磁矩的基本单位,称为玻尔磁子。
eh -24μB = =9.274×10J/T 4πmc
而磁矩与摩尔顺磁磁化率之间有如下关系:
NAμm2 -7χm = ×4π×10 (3-95)
3KT
式中,NA为阿伏伽德罗常数;K为波兹曼常数;T为绝对温度。
根据式(3-95)可以利用测量出的物质的摩尔顺磁化率χm计算出μm,然后根据式(3-94)计算样品的未成对电子数。若测得的则表示物质是反磁性物质χm<0,未成对电子数为零。
三、仪器与试剂
(1)仪器:磁天平1台,样品管1支,直尺1把,温度计1支。
(2)试剂:莫尔氏盐(NH4)2SO4FeSO4·6H2O,分析纯;硫酸亚铁FeSO4·7H2O,分析纯;亚铁氰化钾K4Fe(CN)6·3H2O,分析纯。
四、实验步骤
标定磁场强度方法如下。
①取一支清洁干燥的样品管悬挂在磁天平的挂钩上,称质量得m空。 ②调节磁天平电流开关,由小至大调节至指定位置1(1A),测质量得m空1。 ③继续调大电流开关,至位置2(3A),测质量得m空2。
④继续升高电流至位置3(4A),停留一定时间,然后调小电流从位置3回到位置2,测质量得m空2’。
⑤继续调小电流回到位置1,测质量得m空1’。 ⑥关闭电流测质量得m空’。
表3-26 数据记录表(空管)
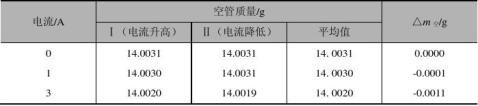
⑦装入已经研细的莫氏盐,装样尽量填实,样品要装至距离管口约1~2cm处,用直尺测量装样的高度,将样品管放入磁天平,按照控管的测量方法测量样品管的重量。
表3-27 样品:莫氏盐,装样高度: 13.41
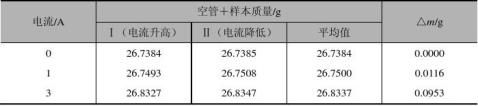
cm
⑧倒出样品管中的莫氏盐,将样品管清洗干净,吹干。装入研细的硫酸亚铁,装样高度和莫氏盐尽量相同,用同样的方法测量硫酸亚铁的数据。
表3-28 样品:硫酸亚铁,装样高度: 13.45 cm
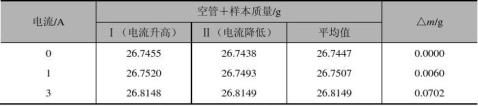
⑨导出样品观众的硫酸亚铁,将样品管清洗干净,吹干。装入研细的亚铁氰化钾,装样高度和莫氏盐尽量相同,用同样的方法测量亚铁氰化钾的数据。
表3-29 样品:亚铁氰化钾,装样高度: 13.`12 cm
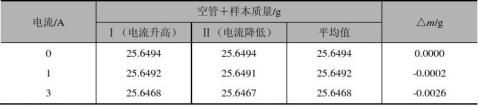
五、数据处理
①计算校准样品的磁化率:根据式(3-93)计算实验温度下莫氏盐的磁化率。 t =30.4℃ M校准剂(莫氏盐)=392.17×10-3 kg/mol 根据式(3-93),实验温度下莫氏盐的质量磁化率为:
χ = ×10-4 = 10-4 = 3.9199×10-7 m3/kg
(30.4+273.15)+1T+1
因此,实验温度下莫氏盐的摩尔磁化率为:
χ校准剂=χ·M校准剂=3.9199×10-7 m3/kg ×392.17×10-3 kg/mol=1.5372×10-7 m3/mol ②计算待测样品的摩尔磁化率χm:由式(3-89)计算各样品的的磁化率,取平均值。
(△m样品-△m空) m校准剂 M样品 h样品
χ样品 = ×××χ校准剂 (△m校准剂-△m空) m样品 M校准剂 h校准剂 设当电流等于1A时,摩尔磁化率为χ1;当电流等于3A时,摩尔磁化率为χ2 Ⅰ.硫酸亚铁FeSO4·7H2O
× ×1.5372×10-7 χ1 = × ×0.0116-(-0.0001) 26.7507-14. 0030 392.17 13.41
=0.5698×10-7 m3/mol
× χ2 = × × ×1.5372×10-7
0.0953-(﹣0.0011) 26.8149-14.0020 392.17 13.41
=0.7342×10-7 m3/mol
χm(硫酸亚铁)=1/2(χ1+χ2) ×278.03 =1/2(0.5698+0.7342)×10-7 ×278.03×10-3 kg/mol=1.813×10-7 m3/mol
Ⅱ.亚铁氰化钾K4Fe(CN)6·3H2O
﹣0.0002 × 26.7500 422.39 13.12χ1 =-(-0.0001) -14. 0030 × ××1.5372×10-7 0.0116-(-0.0001) 25.6492- 14.0030 392.17 13.41
=﹣0.0152×10-7 m3/mol
26.8337 × 13.12χ2 =﹣0.0026-(﹣0.0011) ×-14.0020 422.39 × ×1.5372×10-7 0.0953- (﹣0.0011) 25.6468-14.0020 392.17 13.41
=﹣0.02842×10-7 m3/mol
χm(亚铁氰化钾)= (χ1+χ2) =[﹣0.0152+(﹣0.02842)]×10-7 =﹣0.0462×10-7 m3/mol
③根据χm计算样品的未成对电子数:由式(3-95)计算磁矩μm,再由式(3-94)计算样品分子重金属离子的未成对电子数。
因为χm(硫酸亚铁)=0.6520×10-7 m3/mol>0,表明其为顺磁性,硫酸亚铁存在未成对电子。
NAμm2 根据 χ m = × 4 π × 10 -7
3KT
可得
μm(硫酸亚铁)= = =4.656×10-23 μm=eh -24n +2 ) μ B 且 μB = =9.274×10J/T 又因为 μ m n ( 4πmc
22 所以 n+2n-(μm/μB)
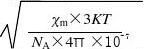
=0
即
2 n2+2n-
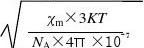
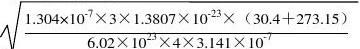
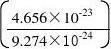
=n2+2n-25.205=0
﹣2±22-4×1×(﹣25.205) n= 2×1解得 n=4(舍掉负值)
即硫酸亚铁的未成对电子数为4
而χm(亚铁氰化钾) =﹣0.0420×10-7 m3/mol<0,表明其为反磁性,
故亚铁氰化钾没有未成对电子。
实验结果的理论分析:
[Fe(II)(H2O)6]2+,其中心原子Fe2+提供6个3d电子,周围6个水
分子配体共提供12个配位电子,6+12=18电子。又因为水分子
是弱配体,根据晶体场理论,此时电子分裂能小于电子成对能,
电子成对所需能量更大,d电子将尽量减少成对,因此在 (t2g) 和
(e*g) 轨道上各有2个未成对电子,共有n=4 ;另外按照杂化轨
道理论称之为sp3d2型配键。所以FeSO4·7H2 O是弱场高自旋的
配合物。 e*g t2g
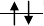
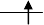
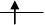

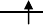
. (t2g)4(e*g)2
[Fe(II)(CN)6]4-,其中心原子Fe2+提供6个3d电子,周围6个氰根
配体共提供12个配位电子,6+12=18电子。又因为氰根离子是强
配体,[Fe(II)(CN)6]4-的配位场结构与上述的不同,此时,电子成对
能小于电子分裂能,电子进入(e*g)轨道所需能量更大,d电子将先
成对充满(t2g)轨道,因此在所有轨道上都没有未成对电子,n=0 ;
另外按照杂化轨道理论称之为d2sp3型配键。所以
K4Fe(CN)6·3H2O是强场低自旋的配合物。
六、提问与思考
①实验操作中应该注意的问题。
答:1.所测样品应研细。
2.天平称量时,必须关上磁极架外面的玻璃门,以免空气流动干扰称量。
3.通电和断电前,务必将电源旋钮调到最小或励磁电流为零,励磁电流的升降应平稳。
4.样品管一定要干净。装样时应使样品均匀填实,测量样品的装填高度应尽量一致。装样时不
要一次加满,应分次加入,边加边碰击填实后,再加再填实,尽量使样品紧密均匀。
5.样品管应悬于两磁极之间,底部与磁极中心线齐平。
6.挂样品管的悬线不要与任何物体接触。
7.外加磁场后,应检查样品管是否与磁极相碰,若相碰,应轻轻旋转样品管的木塞,调整样品
管的位置。
②实验误差的来源。
答:1.材料性质会影响古埃磁天平测定物质磁化率的精密度: 古埃磁天平只能测量弱磁性物质。
对于强磁性物质,将样品管悬于磁极的中心位置时,样品管立即被吸附在磁极上,无法进行测量。
2.磁场强度的影响: 对于弱磁性物质,如果磁场强度过大,将样品管悬于磁极的中心位置时,
样品管也有被磁极吸附而倾斜的现象,给测量带来困难,或者天平显得极不灵敏而无法进行测量。因此实验电流的大小很重要。
3.实验操作的影响:由于弱磁性物质在加磁场前后质量差异较小,因此测量时应细心操作,正
确读数,否则将产生巨大的实验误差。
第 6 页 共 7 页 e*g t2g
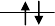

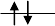
(t2g)6(e*g)0
4.不可能保证每一个样品装样的紧密度一样,因此测量得到的高度h具有一定误差。
5.本实验并未对样品进行干燥,会造成一定误差。
③被测样品是顺磁性物质还是反磁性物质?为什么?
答:已知:顺磁性物质χm>0,反磁性物质χm<0,
χm(硫酸亚铁)=1.304×10-7 m3/mol>0
χm(亚铁氰化钾)=﹣0.0420×10-7 m3/mol<0
所以:硫酸亚铁FeSO4·7H2O是顺磁性物质,
亚铁氰化钾K4Fe(CN)6·3H2O是反磁性物质。
第二篇:磁化率的测定(完成)
实验报告
学生姓名 学 号
专 业 年级、班级
课程名称 实验项目 磁化率的测定
实验类型 ?验证 ?设计 ?综合 实验时间 年 月 日
实验指导老师 实验评分
一、目的要求
1.掌握Gouy磁天平测定物质磁化率的实验原理和技术。
2.通过对一些配合物磁化率的测定,计算中心离子的不成对电子数.并判断d电子的排布情况和配位体场的强弱。
二、实验原理
(1)物质的磁性
物质在磁场中被磁化,在外磁场强度H(A·m-1)的作用下,产生附加磁场H'。这时该物质内部的磁感应强度B为外磁场强度H与附加磁场强度H'之和:
B=H十4πI=H十4πкH=μH (1)
式中I称为体积磁化强度,物理意义是单位体积的磁矩。式中的 к 称为物质的体积磁化率、表示单位体积物质的磁化能力,是无量纲的物理量。I 和 к 分别除以物质的密度ρ可以得到 σ 和 χ ,σ = I/ρ 称为克磁化强度;χ = к/ρ 称为克磁化率或比磁化率。χm = кM/ρ 称为摩尔磁化率(M是物质的摩尔质量)。这些数据都可以从实验测得,是宏观磁性质。在顺磁、反磁性研究中常用到 χ 和 χm ,铁磁性研究中常用到I、σ 。
不少文献中按宏观磁性质,把物质分为反磁性物质、顺磁性物质和铁磁性物质以及亚铁磁性物质、反铁磁性物质几类。其中,顺磁性物质的χm >0,而反磁性物质的χm <0。
(2)古埃法测定磁化率
古埃法是一种简便的测量方法,主要用在顺磁测量。简单的装置包括磁场和测力装置两部分。调节电流的大小,磁头间距离大小,可以控制磁场强度大小。测力装置可以用分析天平。为了测量不同温度的数据,要使用变温、恒温和测温装置。
样品要放在一个长圆柱形玻璃管内,悬挂在磁场中,样品管下端在磁极中央处,此处磁场强度最强;另一端则在磁场强度为零处,即处在磁场强度可忽赂不计的位置。
样品在磁场中受到一个作用力。
dF = κHAdH ①
式中,A表示圆柱玻璃管的截面积。
样品在空气中称量,必须考虑空气修正,即
dF =(κ-κ0)HAdH ②
表示空气的体积磁化率,整个样品的受力是个积分问题:
F=∫ (κ-κ0)HAdH = 1/2(κ-κ0)A(H2-H20) ③
因H0<<H,且忽略κ0,则
F = 1/2 κAH2 ④
式中,F可以通过样品在有磁场和无磁场的两次称量的质量差来求出。
F =(?m样 - ?m空)g ⑤
式中,?m样为样品管加样品在有磁场和无磁场时的质量差; ?m空为空样品管在有磁场和无无磁场时的质量差;g为重力加速度。
则有,κ = ⑥
而χm = ,ρ = ,h为样品高度,A为样品管截面积,m样品为样品质量。
χm = = (M)/ = ⑦
只要准确测量样品重量的变化、磁场强度H及样品高度h,即可根据式⑦来计算样品的摩尔磁化率。
在实际工作中是采用已准确知道磁化率数值的校准样品来标定磁场,根据式⑦
= ×××
χ样 = ×××χ校准剂 ⑧
常用的校准样品有(NH4)2SO4·FeSO4·6H2O(莫氏盐)、HgCo(CNS)4、Ni(en)3S2O3。其中,(NH4)2SO4 FeSO4·6H2O的磁化率符合公式
χ = × 10-4
式中,T是绝对温度。
(3)简单络合物的磁性与未成对电子
对于第一过渡系列元素络合物,它们的磁矩实验值大多符合
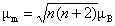 ⑨
⑨
式中,n是未成对电子数;μB是电子磁矩的基本单位,称为波尔磁子。
μB = = 9.274×10-24J/T ⑩
而磁矩μm 与 摩尔顺磁磁化率χm之间有如下关系:
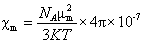 ?
?
式中,NA为阿弗加德罗常数;K为波兹曼常数;T为绝对温度。
根据式 ?可以利用测量出的物质的摩尔顺磁化率χm计算出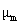 ,然后根据式⑨计算样品的未成对电子数。若测得的χm则表示物质是反磁性物质,未成对电子数为零。
,然后根据式⑨计算样品的未成对电子数。若测得的χm则表示物质是反磁性物质,未成对电子数为零。
三、仪器与试剂
仪器:
磁天平一台(上方加配一台电光分析天平);玻璃样品管一支;装样品工具一套(包括研钵、角匙、小漏斗、不锈钢针或竹针、脱脂棉、玻璃棒、橡皮垫等);直尺一把,温度计一支。
试剂:
莫氏盐(NH4)2SO4·FeSO4·6H2O(分析纯);
亚铁氰化钾K4Fe(CN)6·3H2O(分析纯);
硫酸亚铁FeSO4·7H2O(分析纯)。
四、实验步骤
标定磁场强度方法如下。
① 取一只清洁干燥的样品管悬挂在磁天平的挂钩上,称质量得m空。
② 调节磁天平电流开关,由小至大调节至指定位置1(1A),测质量得
m空1 。
③ 继续调大电流开关,至位置2(3A),测质量得 m空2 。
④ 继续升高电流至位置3(4A),停留一定时间,然后调小电流从位置3回到位置2,测质量得m空2'。
⑤ 继续调小电流回到位置1,测质量得m空1'。
⑥ 关闭电流测质量得m空'。
⑦ 装入已经研细的莫氏盐,装样尽量填实,样品要装在距离管口1~2cm处,用直尺测量装样的高度,将样品管放入磁天平,按照空管的测量方法测量样品管的质量。
⑧ 倒出样品管中的莫氏盐,将样品管清洗干净,吹干。装入研细的硫酸亚铁,装样高度和莫氏盐尽量相同,用同样的方法测量硫酸亚铁的数据。
⑨ 倒出样品管中的硫酸亚铁,将样品管清洗干净,吹干。装入研细的亚铁氰化钾,装样高度和莫氏盐尽量相同,用同样的方法测量亚铁氰化钾的数据。
五、数据记录及处理
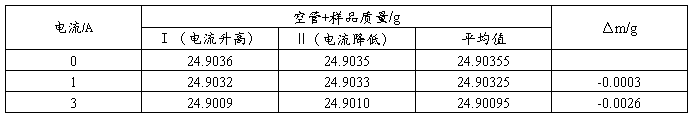
1. 数据记录表
空管:
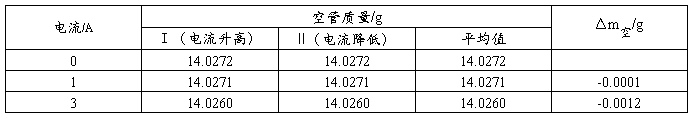
样品:莫氏盐 装样高度:13.4cm
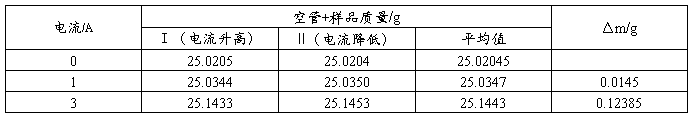
样品:硫酸亚铁 装样高度:14.2cm
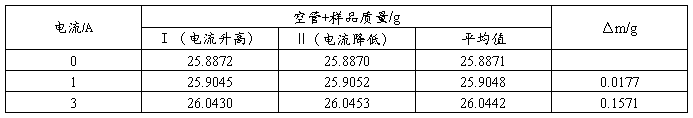
样品:亚铁氰化钾 装样高度:13.4cm
2. 数据处理
① 计算校准样品的磁化率 根据式⑤计算实验温度下莫氏盐的磁化率。
χ 莫氏盐= × 10-4=4.0989× 10-7(m3/kg)
=1.6068× 10-7(m3/mol)
② 计算待测样品的摩尔磁化率χm 由式④计算各样品的磁化率,取平均值。
1.硫酸亚铁:
χ1= ×××χ校准剂
=1.3649×10-7(m3/mol)
χ2= ×××χ校准剂
=1.4172×10-7(m3/mol)
硫酸亚铁的摩尔磁化率χm(平均值)=1.39105×10-7(m3/mol)
2.亚铁氰化钾:
χ1= ×××χ校准剂
=-2.3972×10-9(m3/mol)
χ2= ×××χ校准剂
=-1.9592×10-9(m3/mol)
亚铁氰化钾的摩尔磁化率χm(平均值)==-2.1782×10-9(m3/mol)
③ 根据χm计算样品的未成对电子数 由式⑥计算磁矩μm,再由式⑨计算样品分子中金属离子的未成对电子数。
1.硫酸亚铁:
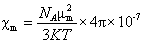
μB= 9.274×10-24J/T
μm=4.7006×10-23
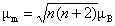
n=4
2.亚铁氰化钾:
因为μm<0,表示亚铁氰化钾是反磁性物质,没有未成对电子.
六、实验注意事项
1.天平称量时,必须关上磁极架外面的玻璃门,以免空气流动对称量的影响。
2.励磁电流的变化应平稳、缓慢,调节电流时不宜用力过大。加上或去掉磁场时,勿改变永磁体在磁极架上的高低位置及磁极间矩,使样品管处于两磁极的中心位置,磁场强度前后一致。
3.装在样品管内的样品要均匀紧密、上下一致、端面平整、高度测量准确。
七.提问与思考
