ʵ��ʮ�� �������Һ���ϵ���IJⶨ
һ��ʵ��Ŀ��
�ⶨ��ͬŨ��������Һ�е�ƽ�����ӻ��ϵ����������������Һ�еĻ�ȡ�
����ʵ��ԭ��
������Һ��������һ���B�Ļ�ѧ�Ʊ�ʾʽ�е�Ħ������ ��֮�Ի�ȣ����ɱ�ʾ��ʵҺ�����������B�Ļ�ѧ�ơ�
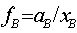
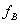 Ϊ��ʵҺ�����������B�Ļ�����ӡ���ʵ��Һ������B�����¶�T��ѹ��P�£�����B�Ļ��ϵ��Ϊ��
Ϊ��ʵҺ�����������B�Ļ�����ӡ���ʵ��Һ������B�����¶�T��ѹ��P�£�����B�Ļ��ϵ��Ϊ�� 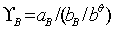
���� Ϊ������ӣ���ƻ��ϵ������
Ϊ������ӣ���ƻ��ϵ������
��أ�Ag��AgCl| HCL| ���� | ��Һ || KCL�����ͣ�| 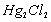 ��g����
��g����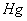
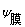
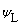 ��Һ�ӵ��ƣ�
��Һ�ӵ��ƣ�



 �����缫 | | �ʹ��缫
�����缫 | | �ʹ��缫
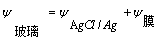
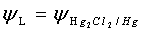
������صĵ綯�ƣ�
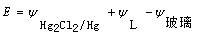 ��1��
��1��
���У�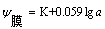 ��K�Dz���Ĥ�缫�⡢��Ĥ�������ʾ����ij�����
��K�Dz���Ĥ�缫�⡢��Ĥ�������ʾ����ij�����
��ʵ���¶�Ϊ25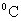 ʱ
ʱ 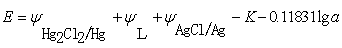
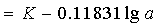
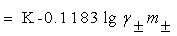 ��2��
��2��
��ʽ�ɸ�дΪ�� 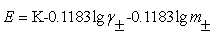
��
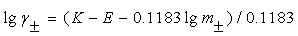
���ݵðݡ����ݿ˶�����ʽ����1����1���͵���ʵ�ϡ��Һ��˵�����ϵ����������ϵʽ 
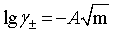
���� 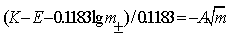
�� 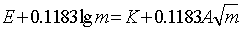
��ͬŨ�ȵ�HCl��Һ���ɵ�Һ��أ����ֱ�������Ӧ�ĵ綯��Eֵ����0.11831gmΪ�����꣬��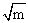 Ϊ��������ͼ���ɵ�һ���ߣ������������ƣ��������K�����K���ٽ�����ͬŨ��mʱ����õ���ӦEֵ���루2��ʽ���Ϳ���������ֲ�ͬŨ���µ�ƽ�����ӻ��ϵ����±��ͬʱ����
Ϊ��������ͼ���ɵ�һ���ߣ������������ƣ��������K�����K���ٽ�����ͬŨ��mʱ����õ���ӦEֵ���루2��ʽ���Ϳ���������ֲ�ͬŨ���µ�ƽ�����ӻ��ϵ����±��ͬʱ����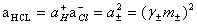 ֮��ϵ���������Һ��HCl��Ӧ�Ļ�ȡ�
֮��ϵ���������Һ��HCl��Ӧ�Ļ�ȡ�
��������ҩƷ
���������ӻ�ȼơ��ɵ�ء���Һ������֧��
ҩƷ��0.1mol/L������Һ
�ġ����鲽��
1����Һ����
�ֱ�����0.005mol/L��0.01mol/L��0.02mol/L��0.05 mol/L��0.1 mol/L��Һ50mL
2����ͬŨ�ȵ�������Һ�ĵ綯�Ʋⶨ
�ⶨ��ͬŨ��HCl��Һ��E��
�塢ע������
1����ʵ���е�صĵ綯�ƣ�����һ��ƽ������⣬�綯����С����Ҳ��15min���Ҳ����ȶ����䣬��ʼʱ���Խϴ���������ٰѹ�·�еĿ������������Ӧ���ȶ���������������й�������
2�����ڵ缫�н�ǿ���������ܣ��ڲⶨ��ϡ����Һʱ�������ô���Һ��ϴ��������ܸı��ص�Ũ�ȡ�
�������ݼ�¼

�ߡ����ݴ���
1����E��
����ͬŨ�ȵ�HCl��Һ�ֱ�������Ӧ�ĵ綯��Eֵ����0.11831gmΪ�����꣬��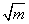 Ϊ��������ͼ�������������ƣ���K��
Ϊ��������ͼ�������������ƣ���K��
2����������ֲ�ͬŨ���µ�ƽ�����ӻ��ϵ��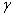 ��
��
3�����ݹ�ʽ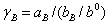 ��
��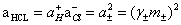 ֮��ϵ���������Һ��HCl��Ӧ�Ļ�ȡ�
֮��ϵ���������Һ��HCl��Ӧ�Ļ�ȡ�
1�����ݴ�������
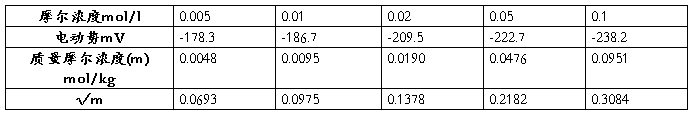
��Ҫ����ͼ��

��ͼ��֪K��=-0.468
2����K�����빫ʽ��2���ɵ�

3�����ݹ�ʽ����ɵã�

�ˡ�˼����
1�������綯�Ʒ��ⶨƽ�����ӻ��ϵ���Ļ���ԭ����
�ѵ�ص綯�ƵĹ�ʽ ��°ݡ��ݿ˶��ļ���ʽ
��°ݡ��ݿ˶��ļ���ʽ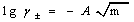 ���ϵõ�
���ϵõ�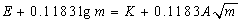 ������ֱ��֮�������Ƶõ�K��,�ٽ�K�������綯�ƹ�ʽ�����ƽ�����ӻ��ϵ����
������ֱ��֮�������Ƶõ�K��,�ٽ�K�������綯�ƹ�ʽ�����ƽ�����ӻ��ϵ����
2����ʵ���¶Ƚӽ�25��ʱ��Ϊ�ο������Ʒ���ȷ�����綯�ƣ�
��Ϊ�ӽ�25ʱ�°ݡ��ݿ˶���ʽ�е�A��������ȷ���ij���Ϊ0.509����������Ũ�ȱ仯��ֵ�����������Ʒ���
�š�������
1��ÿ�β���ǰ��Ҫ�ô���Һϴ�ɾ������⽫��Һϡ�͡�
2���������ӻ�ȼƵĶ������ϵ���Ծ�����ն������ȶ���ֵ����ƫ�

�� �� �� ѧ
ʵ�鱨��
ʵ�����ƣ��������Һ���ϵ���IJⶨ
�� ����������
�� ����12��Ӧ�û�ѧ
ѧ �ţ�1220405005
ָ����ʦ���ܺ��
ʵ�����ڣ�20##/3/13
�ڶ�ƪ���������Һ���ϵ���IJⶨ

������ѧʵ�鱨��
ʵ�����ƣ� �������Һ���ϵ���IJⶨ
ѧ �ţ�
�� ���� ��ɫұ��
�� ����
ʵ�����ڣ� 20##-3-13
һ��ʵ��Ŀ��
�ⶨ��ͬŨ��������Һ�е�ƽ�����ӻ��ϵ����������������Һ�еĻ�ȡ�
����ʵ��ԭ��
������Һ��������һ���B�Ļ�ѧ�Ʊ�ʾʽ�е�Ħ������ ��֮�Ի�ȣ����ɱ�ʾ��ʵҺ�����������B�Ļ�ѧ�ơ�

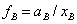
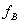 Ϊ��ʵҺ�����������B�Ļ�����ӡ���ʵ��Һ������B�����¶�T��ѹ��P�£�����B�Ļ��ϵ��Ϊ��
Ϊ��ʵҺ�����������B�Ļ�����ӡ���ʵ��Һ������B�����¶�T��ѹ��P�£�����B�Ļ��ϵ��Ϊ�� 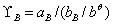
����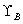 Ϊ������ӣ���ƻ��ϵ������
Ϊ������ӣ���ƻ��ϵ������
��أ�Ag��AgCl|HCL|����|��Һ||KCL�����ͣ�| 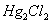
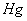
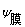
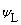 ��Һ�ӵ��ƣ�
��Һ�ӵ��ƣ�


 �����缫 | | �ʹ��缫
�����缫 | | �ʹ��缫
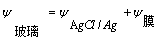
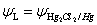
������صĵ綯�ƣ� 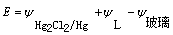 ��1��
��1��
���У�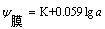 ��K�Dz���Ĥ�缫�⡢��Ĥ�������ʾ����ij�����
��K�Dz���Ĥ�缫�⡢��Ĥ�������ʾ����ij�����
��ʵ���¶�Ϊ25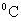 ʱ
ʱ 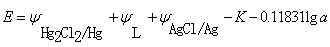
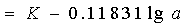
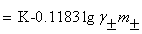 ��2��
��2��
��ʽ�ɸ�дΪ�� 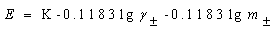
��
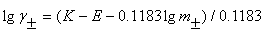 ��1��
��1��
���ݵðݡ����ݿ˶�����ʽ����1����1���͵���ʵ�ϡ��Һ��˵�����ϵ����������ϵʽ
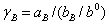
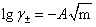
���� 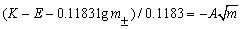
�� 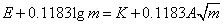
��ͬŨ�ȵ�HCl��Һ���ɵ�Һ��أ����ֱ�������Ӧ�ĵ綯��Eֵ����0.11831gmΪ�����꣬��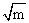 Ϊ��������ͼ���ɵ�һ���ߣ������������ƣ��������K�����K���ٽ�����ͬŨ��mʱ����õ���ӦEֵ���루2��ʽ���Ϳ���������ֲ�ͬŨ���µ�ƽ�����ӻ��ϵ����±��ͬʱ����
Ϊ��������ͼ���ɵ�һ���ߣ������������ƣ��������K�����K���ٽ�����ͬŨ��mʱ����õ���ӦEֵ���루2��ʽ���Ϳ���������ֲ�ͬŨ���µ�ƽ�����ӻ��ϵ����±��ͬʱ����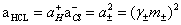 ֮��ϵ���������Һ��HCl��Ӧ�Ļ�ȡ�
֮��ϵ���������Һ��HCl��Ӧ�Ļ�ȡ�
��������ҩƷ
����: ���ӻ�ȼơ��ɵ�ء���Һ������֧��
ҩƷ: 0.1mol/L������Һ��
�ġ����鲽��
1����Һ����
�ֱ�����0.005mol/L��0.01mol/L��0.02mol/L��0.05 mol/L��0.1 mol/L��Һ50mL
2����ͬŨ�ȵ�������Һ�ĵ綯�Ʋⶨ
�ⶨ��ͬŨ��HCl��Һ��E��
�塢���ݼ�¼
1�����ò�ͬŨ�ȵ�������Һ����0.1 mol/L HCl��Һ���£�
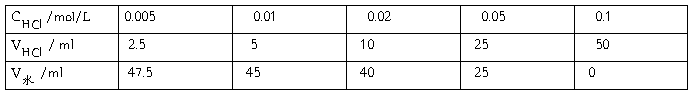
2����ͬŨ�ȵ�50mL������Һ�ĵ綯�ƵIJⶨ

�������ݴ���
1������Eֵ������Ħ��Ũ��m������ֵ����������K��ֵ��
����һ��ϡ��Һ��˵�����ܶȽ��Ƶ���ˮ���ܶȣ����Խ�����Ϊ
C��mol/L��=m��mol/kg�������ֽ��Ƴ����ڼ����С�
��m = CHCl /��ˮ������ ��ˮ = 1.0 Kg/m3 ���ɼ���� E+0.1183lgm��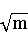 ���������±���
���������±���
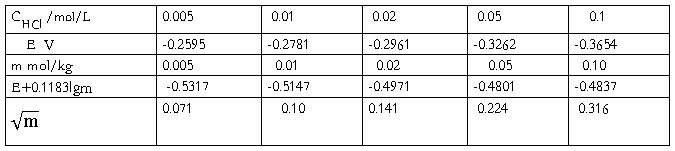
����ͬŨ�ȵ�HCl��Һ�ֱ�������Ӧ�ĵ綯��Eֵ����
E +0.11831gmΪ�����꣬��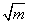 Ϊ��������ͼ�������������ƣ���K����
Ϊ��������ͼ�������������ƣ���K����
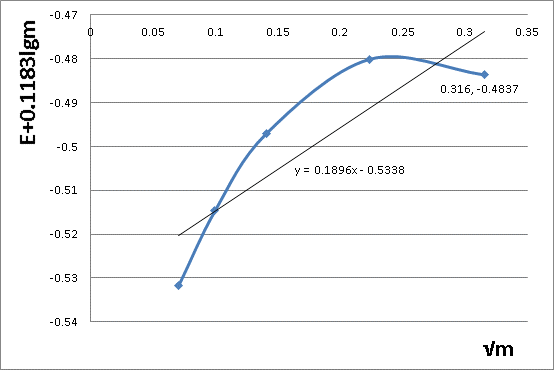
��ͼ�����K��= -0.5338
2����������ֲ�ͬŨ���µ�ƽ�����ӻ��ϵ�� ��
��
������ͬŨ�ȵ�mʱ����õ���ӦEֵ����
lg =1/0.1183 (k��- E �C 0.1183lgm)
=1/0.1183 (k��- E �C 0.1183lgm)
�ɼ�������ֲ�ͬŨ���µ�ƽ�����ӻ��ϵ�� ��
��
lg 1 =1/0.1183 (k��- E1 �C 0.1183lgm)
1 =1/0.1183 (k��- E1 �C 0.1183lgm)
=1/0.1183 {-0.5338 + 0.2595 �C 0.1183lg0.005}
= -0.0177
 1 =0.9600
1 =0.9600
lg 2 =1/0.1183 (k��- E2 �C 0.1183lgm)
2 =1/0.1183 (k��- E2 �C 0.1183lgm)
=1/0.1183 {-0.5338 + 0.2781 �C 0.1183lg0.01}
=-0.1614
 2 =0.6896
2 =0.6896
lg 3 =1/0.1183 (k��- E3 �C 0.1183lgm)
3 =1/0.1183 (k��- E3 �C 0.1183lgm)
=1/0.1183 {-0.5338 + 0.2961 �C 0.1183lg0.02}
=-0.3103
 3 =0.4894
3 =0.4894
lg 4 =1/0.1183 (k��- E4 �C 0.1183lgm)
4 =1/0.1183 (k��- E4 �C 0.1183lgm)
=1/0.1183 {-0.5338 + 0.3262 �C 0.1183lg0.05}
=-0.5438
 4 = 0.2829
4 = 0.2829
lg 5 =1/0.1183(k��- E5 �C 0.1183lgm)
5 =1/0.1183(k��- E5 �C 0.1183lgm)
=1/0.1183{-0.5338 + 0.3654 �C 0.1183lg0.1}
=-0.4235
 5 = 0.3771
5 = 0.3771
3�����ݹ�ʽ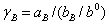 ��
��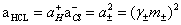 ֮��ϵ���������Һ��HCl��Ӧ�Ļ�ȡ�
֮��ϵ���������Һ��HCl��Ӧ�Ļ�ȡ�
�ɹ�ʽ�ɼ���� B
B
 B1 = (
B1 = ( 1m1)2 = (0.9600 * 0.005)2 = 2.304 * 10-5
1m1)2 = (0.9600 * 0.005)2 = 2.304 * 10-5
 B 2 = (
B 2 = ( 2m2)2 = (0.6896 * 0.01)2 = 7.562 * 10-5
2m2)2 = (0.6896 * 0.01)2 = 7.562 * 10-5
 B3 = (
B3 = ( 3m3)2 = (0.4894 * 0.02)2 = 9.580 * 10-5
3m3)2 = (0.4894 * 0.02)2 = 9.580 * 10-5
 B4 = (
B4 = ( 4m4)2 = (0.2829 * 0.05)2 = 2.000 * 10-4
4m4)2 = (0.2829 * 0.05)2 = 2.000 * 10-4
 B5 = (
B5 = ( 5m5)2 = (0.3771 * 0.1)2 = 2.304 * 10-4
5m5)2 = (0.3771 * 0.1)2 = 2.304 * 10-4
�ߡ�˼������
1�������綯�Ʒ��ⶨƽ�����ӻ��ϵ���Ļ���ԭ����
��ƽ�����ӻ��ϵ��  ±�IJⶨ���ⶨ ±�ķ������ܽ�ȷ��������Է����綯�Ʒ��������Ե綯�Ʒ����㡣�õ綯�Ʒ����������ӵ�
±�IJⶨ���ⶨ ±�ķ������ܽ�ȷ��������Է����綯�Ʒ��������Ե綯�Ʒ����㡣�õ綯�Ʒ����������ӵ� ±ʱ�������øõ������Һ��Ƴ�һ��ԭ��ء���ƴ�ԭ��ص������ǣ����ĵ�ط�Ӧ��ֻ���õ������Һ����������Һ����ⶨHClˮ��ҺHCl��
±ʱ�������øõ������Һ��Ƴ�һ��ԭ��ء���ƴ�ԭ��ص������ǣ����ĵ�ط�Ӧ��ֻ���õ������Һ����������Һ����ⶨHClˮ��ҺHCl��  ±������Ƶ�ԭ���ͬǰ����ǰʽ�ɵã�ln =F/2RT�� Emf - + ���ɴ�ʽ�ɼ����õ�ص�Nernst��ʽ��ֻ��HCl�Ļ�ȶ�������������Һ�Ļ�ȡ�
±������Ƶ�ԭ���ͬǰ����ǰʽ�ɵã�ln =F/2RT�� Emf - + ���ɴ�ʽ�ɼ����õ�ص�Nernst��ʽ��ֻ��HCl�Ļ�ȶ�������������Һ�Ļ�ȡ�
2����ʵ���¶Ƚӽ�25��ʱ��Ϊ�ο������Ʒ���ȷ�����綯�ƣ�
����Ϊ��25��ʱ�綯��E��K�������Թ�ϵ�����Կ��������Ʒ���ȷ�����綯��
