实验八 摩尔折射度的测定
一、实验目的
1. 测定氯仿在环己烷中的介电常数和偶极矩,了解偶极矩与分子电性质的关系。
2. 测定某些化合物的折光率和密度,求算化合物,基团和原子的摩尔折射度,判断化合物的分子结构。
3. 了解克劳修斯-德拜方程的意义及公式的适用范围。
二、实验原理
摩尔折射度是由于在光的照射下分子中电子云(主演是价电子云)相对于分子骨架的相对于分子骨架的相对移动结果,可作为分子中电子极化率的量度.R有体积的因次.若以钠光D线为光源,所得的折射率以m表示,相应的摩尔折射度以 实验结果表明R有加和性,即R等于分子中的各原子折射度及形成化学键时折射度的增量之和.利用R的加和性可根据物质的化学式算出其各种同分异构体的折射度与实验结果相比较,从而探讨原子间的键型与分子结构.
实验结果表明R有加和性,即R等于分子中的各原子折射度及形成化学键时折射度的增量之和.利用R的加和性可根据物质的化学式算出其各种同分异构体的折射度与实验结果相比较,从而探讨原子间的键型与分子结构.
对于共价化合物,偶尔折射度的加和性还可表现为:分子的摩尔折射度等于分子中各个化学键摩尔折射度之和.例如乙酸甲酯和乙酸乙酯的摩尔折射度之差为CH2基团的折射度即为两个Cl原子的折射度.分子中若有共轭键存在,电子活动性提高,会产生超加折射度.若某化合物的摩尔折射度的实验值远超过于原子加和所得的理论值.则可以判断分子中有共轭体系,复健或成环的可能性.
三、主要试剂和仪器
1. 阿贝折光仪,密度管
2. 氯仿,乙酸乙酯,二氯,丙酮,苯,乙醇,乙酸丁酯,乙酸异戊酯
四、实验步骤
1. 折光率的测定
使用阿贝折光仪测定上述物质的折光率.
2. 密度的测定
用密度管测定上述物质的密度.
用循环水溶液控制折光仪和密度管在相同温度条件下进行试验测定.控温精度要求:±0.1k。
五、实验数据及其处理
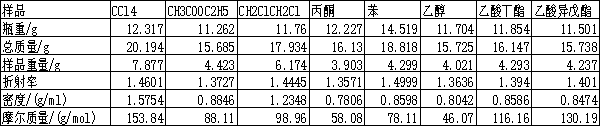
实验计算见手写页
六、实验误差处理分析
1.误差来源
(1)容量瓶干燥不充分,称量结果不准确
(2)测量密度时采用5ml容量瓶,容量瓶误差在±0.01ml左右,因此最终的结果存在误差.
(3)容量瓶理论上应该在25℃使用,但实际测量温度低于25℃,使得体积不准确
(4)密度的测量与折射率的测量理论上应该在相同温度下进行,实际中折射率的测量恒温在20℃,但密度测量在室温不断变化中.
(5)阿贝折射仪用纯水矫正和读数时,调节敏感交界处造成的误差使得折射率的测量不准确
(6)在进行密度测量过程中,称质量过程中依照易挥发样品溶剂如乙酸乙酯,丙酮等会由于挥发造成溶剂质量测量不准确,进而密度测量不准确
2.双键及特殊的官能团因摩尔折射度的讨论
根据理论值
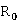 (H)=1.028
(H)=1.028 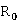 (c)=2.591
(c)=2.591
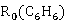 =(1.028+2.591)×6=21.714<
=(1.028+2.591)×6=21.714<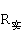 =26.715
=26.715
实验值远超原子加和所得的理论值 因为苯是一个巨大的离域体系
七.实验反思与总结
1.摩尔折射度通常以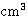 表示,它决定于分子中电子云(主要是价电子云)受外电场的影响对核产生相对移动的结果。实验结果表明,摩尔折射度等于分子中各原子折射度及形成化学键时折射度的增量之总和,这种性质称为摩尔折射度的加和性。典型的离子化合物其摩尔折射度可根据晶体中离子折射度加和而得。于是,可根据物质的化学式算出某物质的各种同分异构体的折射度,与实验测定结果相比较,这对于探讨原子间的键型,分子的结构提供很有意义的数据。
表示,它决定于分子中电子云(主要是价电子云)受外电场的影响对核产生相对移动的结果。实验结果表明,摩尔折射度等于分子中各原子折射度及形成化学键时折射度的增量之总和,这种性质称为摩尔折射度的加和性。典型的离子化合物其摩尔折射度可根据晶体中离子折射度加和而得。于是,可根据物质的化学式算出某物质的各种同分异构体的折射度,与实验测定结果相比较,这对于探讨原子间的键型,分子的结构提供很有意义的数据。
2.折射法的优点:快速,精确度高,样品用量少且设备简单.摩尔折射度在化学上除了可鉴别化合物确定化合物结构外,还可以分析混合物的成分,测定浓度纯度,计算分子大小,测定摩尔质量,研究氢键和测定配合物结构.
3.一些化合物理论计算值与实际值存在差别的原因可能是一些理论值只考虑了相邻原子之间的相互作用.忽略了分子之间各化学键的相互作用.分子中若有共轭键存在 ,电子活动性提高,会产生超加折射度.若化合物的摩尔折射度的实验值远大于原子加和所得的理论值,则可以判断分子中,有共轭体系,复键或成环的可能性.
第二篇:实验报告
精馏塔效率的测定
北京理工大学 化学学院 董婧 1120102745
一、实验目的
1、熟悉板式精馏塔和填料精馏塔的结构、性能与操作。
2、掌握板式塔全塔效率及填料塔等板高度的测定方法。
3、了解精馏操作中各项操作因素之间的关系与相互影响。
二、实验原理
板式精馏塔连续稳态操作时涉及的基本参数有:F、D、W、xF、xD、xW、α、R、q、E、Np共计11个,操作中必然满足的基本关系有以下几方面:
①物料平衡:包括总物料与各组分的平衡,基本衡算式为:
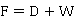
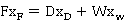
式中:F、D、W— 进料,塔顶、塔底产品的摩尔流率,mol/ s
 、
、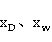 — 进料,塔顶、塔底产品中轻组分的摩尔分率,无因次
— 进料,塔顶、塔底产品中轻组分的摩尔分率,无因次
上述参量中,只有4个独立变量,通常F、 、D、W确定,则
、D、W确定,则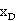 、
、 唯一确定。
唯一确定。
②相平衡:采用相对挥发度,则平衡方程为:

式中:α— 平均相对挥发度,无因次
③在分离效率E,分离程度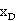 、
、 确定的前提下,操作回流比R与实际塔板数Np的对应;若人为改变操作参数从而引起回流比的改变,在分离效率与塔板数固定的前提下,必然引起塔两端产品浓度的改变。
确定的前提下,操作回流比R与实际塔板数Np的对应;若人为改变操作参数从而引起回流比的改变,在分离效率与塔板数固定的前提下,必然引起塔两端产品浓度的改变。
④进料参数的固定,进料参数包括进料量F与进料浓度 ,进料的热状态参数q以及引入进料的位置
,进料的热状态参数q以及引入进料的位置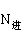 ,人为改变上述参数,必然破坏精馏塔已有的平衡,引起相应操作参数的改变,最终使塔建立新的平衡,从而改变分离效果。
,人为改变上述参数,必然破坏精馏塔已有的平衡,引起相应操作参数的改变,最终使塔建立新的平衡,从而改变分离效果。
除上述平衡外,精馏操作中还要满足热量的平衡,即塔底加热量与塔顶冷凝量的对应以及冷、热物料热量交换的平衡,在恒摩尔流假定的前提下,热量平衡与物料平衡是相互关联、相互制约的,在数学描述中可以不再单独考虑。
常用的精馏塔效率分为单板效率和全塔效率。
单板效率亦称作默弗里效率,反映塔板实际增浓度与理论板增浓度的差距,可分别以气相浓度和液相浓度表示,气相默弗里效率的定义为:
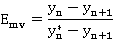
式中: — 分别为离开和进入第n块板的气流浓度
— 分别为离开和进入第n块板的气流浓度
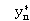 — 与离开第n板的液流浓度成平衡的气相浓度
— 与离开第n板的液流浓度成平衡的气相浓度
全塔效率E可看作精馏塔中各单板效率的平均值,是理论塔板数Nt与实际塔板数的比值:
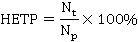
(3-24)
精馏塔操作中,抽样测定某塔板上下方的气、液流浓度,则可确定该板的单板效率,测定塔顶、塔底产品浓度,并依据操作参数计算达到该分离程度所需的理论板数,则可确定该塔的全塔效率。
填料塔操作与板式塔存在相似之处,按照传质单元的概念,将板式塔一块塔板的分离作用当量为某一段填料层,则可仿照板式塔对填料塔进行计算。填料层高度的等板高度HETP定义为填料层高H和理论板数Nt的比值:

对确定的分离,得到理论板数 ,测出实际填料层高,即可得到等板高度。
,测出实际填料层高,即可得到等板高度。
三、实验内容
1、完成精馏塔的操作,实现对乙醇―正丙醇混合液的分离。
2、测定在全回流和部分回流条件下板式精馏塔的全塔效率或填料精馏塔的等板高度。
四、 实验装置与流程
参见图3-5(以板式塔为例)
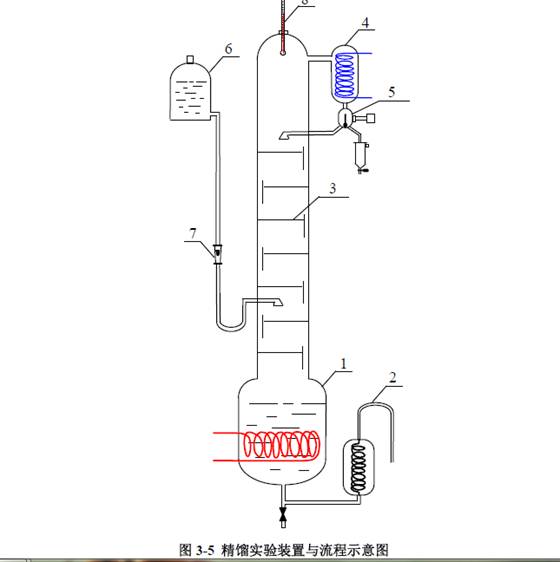
1―蒸馏釜2―液封管 3―塔板 4―冷凝器 5―回流控制器 6―加料高位槽 7―加料流量计 8―塔顶温度计
五、实验方法及步骤
1、准备好阿贝折光仪,调整超级恒温水浴使折光仪处在所需温度。
2、利用进料阀向塔内加料至排出口接近溢流流出为止。
3、打开冷凝器的冷却水。
4、打开塔釜加热电源开关,缓慢加热。注意加热过程中釜内必须有足够的料液(液位应保持在塔釜2/3高度之上),否则立即停止加热。建议升温电压不大于70V,待塔板上开始鼓泡时,可适当加大电压到不大于100V,若出现液泛现象时,可将电压下调到不大于80V。接通塔身保温电源,电压不高于50V并保持不变,实现全回流运行。
5、观察全塔传质情况,稳定后在塔顶、塔釜用注射器同时取样后利用折光仪进行样品浓度分析。
6、调整为部分回流操作,方法是调节进料转子流量计阀门,以的流量0.5-2.0l/h向塔内加料,打开数显时间继电器开关,控制回流比为4:1 。
7、观察全塔传质情况,稳定后记录塔顶、塔底及进料温度,在塔顶、塔釜和进料三处用注射器取样,利用折光仪分析;可连续三次取样分析,重复性达到要求后即为有效结果。
8、测试结束将加热功率调节旋钮复位到零,关闭电源开关,待塔冷却后(塔内不再有气液流动)再关冷却水。
9、将塔顶、塔底收集的料液倒入原料瓶中。
六、实验注意事项
1、折光仪在每次进样分析后,都要擦拭样品池,注射器取样前应注意利用样品进行清洗。
2、严禁直接接触玻璃塔身,塔身上面镀有一层金属膜,用作电阻加热,容易发生触电事故。
3、本实验设备由玻璃制成,在加热时应注意不要过快以免发生玻璃破裂。
4、实验开始应先开冷却水再加热,停止时则反之,加热过程中若釜中液位不够高,塔釜排空管上连接的软胶管中可能会有料液喷出,应予注意。
5、开加热前塔釜内一定要有足够的料液,否则不得加热。
七、阿贝折射仪使用说明
1、每次测定之前须将进试样池的镜面用无水酒精擦拭干净,以免影响成相清晰度和测量准确度。
2、调节恒温水浴,开通循环水,时折光仪温度达到所需测量温度并稳定后即可测量。
3、测量时,将被测样品利用针头从棱镜组侧面小孔中加入,要求液层均匀,充满视场,无气泡。打开遮光板,合上反光镜,调节目镜视度,时十字线成相清晰,此时旋转手轮并在目镜视场中找到明暗分界线的位置,再旋转手轮时分界线不带任何彩色,微调手轮,时分界线位于十字线的中心,在适度转动聚光镜,此时目镜视场下方显示的示值即为被测液体的折射率。
建议测试时选择温度为30℃,该温度下的浓度换算公式为:
W=58.844116-42.61325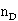
式中:W—样品的质量分率
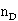 —样品的折光率读数
—样品的折光率读数
八、实验数据记录及处理
本组实验所用的精馏塔为填料塔,填料塔高H=0.383m,等板高度为
故只需求出理论塔板数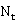 即可求得等板高度HETP。
即可求得等板高度HETP。
1、全回流
实验数据记录:
室温:21℃ 塔顶温度:86℃ 塔底温度:94℃

相平衡方程为

变形得到
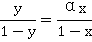
已知在101.3Ka下乙醇-正丙醇的相平衡数据如下:
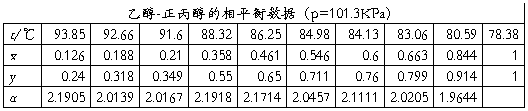
则可知:
塔顶 ℃时,
℃时,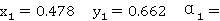 2.1467
2.1467
塔底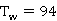 ℃时,
℃时,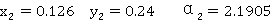
所以有:
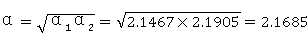
则相平衡方程为
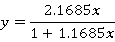
① 计算全回流条件下各组分的摩尔分率
在全回流条件下,回流比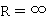 ,理论塔板数最小。
,理论塔板数最小。
利用阿贝折光仪测出的折光度n求出样品的质量分率w,从而求得摩尔分率x.
30℃时,折光率与液相组成之间的关系:
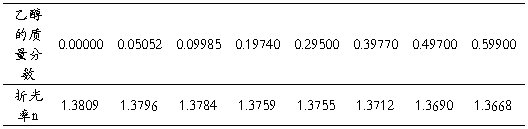
续表

又知:在30℃下,折光度和质量分率满足关系式:
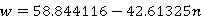
则有
塔顶: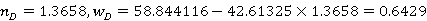
塔底: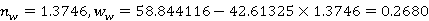
样品的摩尔分率与质量分率满足关系式
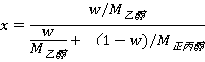
又知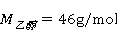 ,
,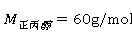
将以上数据代入即可得塔顶和塔底样品的摩尔分率分别为:
塔顶: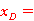 0.7013
0.7013
塔底: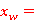 0.3237
0.3237
② 计算理论塔板数
塔顶是全凝器,第一块板的蒸汽组成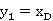 ,分别通过相平衡方程及精馏段、提馏段方程求出x1,x2,…,直至
,分别通过相平衡方程及精馏段、提馏段方程求出x1,x2,…,直至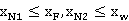 ,则精馏段所需理论塔板数为N1-1,不包括再沸器的理论塔板数N2-1。
,则精馏段所需理论塔板数为N1-1,不包括再沸器的理论塔板数N2-1。
全回流操作中,精馏段、提馏段方程均为y=x,相平衡方衡为
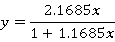
变形,得到
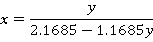
则有
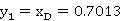

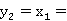 0.5199
0.5199 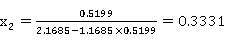
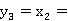 0.3331
0.3331 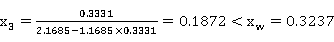
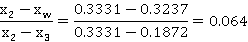
故理论塔板数为

等板高度

2、部分回流条件下
(1) 实验数据记录
塔顶温度:88℃ 塔底温度:94℃
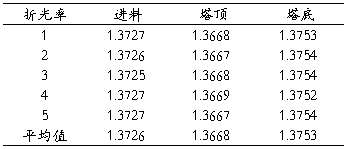
对流比为R=4:1;
(2)计算各组分摩尔分率
① 塔顶各组分
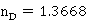 ,
,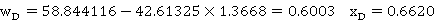
② 塔底各组分
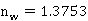 ,
,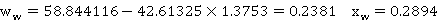
③ 进料组分
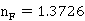 ,
,
故得精馏段方程为
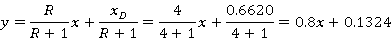
(3)求q线方程
根据乙醇-正丙醇平衡数据可以得到:
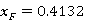 ,泡点
,泡点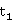 =87.15℃
=87.15℃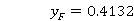 ,露点
,露点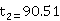 ℃
℃
查课本附录15得:
乙醇在87.15℃时的气化潜热为860kJ/kg,正丙醇在90.51℃下的气化潜热为720kJ/kg。
查课本附录13得:
在进料温度21~87.4℃范围内,乙醇的平均比热为3.72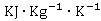 ,正丙醇的为2.34
,正丙醇的为2.34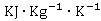 。
。
进料的平均摩尔质量为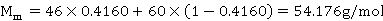
平均比热容为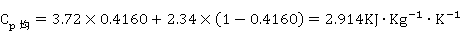
料液由21℃升到87.4℃需热量为
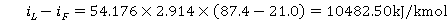
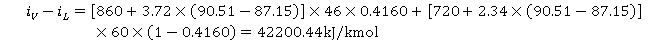
故有
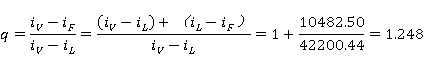
q线方程为
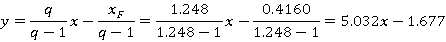
Q线方程与精馏段方程联立点(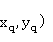 ,即(0.4276,0.4744)。
,即(0.4276,0.4744)。
提馏段线过点(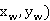 ,即(0.2894,0.2894)和点(0.4276,0.4744),则可求得提馏段方程为
,即(0.2894,0.2894)和点(0.4276,0.4744),则可求得提馏段方程为
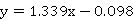
(4)用逐板法计算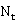
精馏段
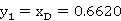
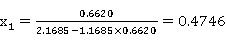
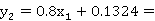 0.5120
0.5120
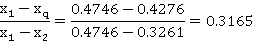
故精馏段理论塔板数
进入提馏段:
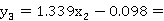 0.4746
0.4746 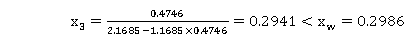
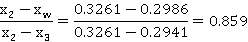
故提馏段的理论塔板数为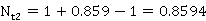
综合得总的理论塔板数为
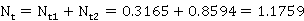
等板高度为
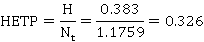
九、结果分析与讨论
1、从上述结果可以看出,全回流条件下塔顶轻组分浓度较高,即产品纯度高。因为随着回流比的增大,所需塔板数减少,而已知塔板数不变,就会导致超过原来的分离要求。故在操作中因意外而产品纯度低于要求时,可进行一段时间的全回流,以尽快达到正常操作。
2、部分回流条件下的等板高度应小于全回流条件下的等板高度,因为在全回流下回流比R无限大,精馏操作线斜率R/(R+1)趋于1,与对角线重合,此时理论塔板数最少。
3、从实验结果可以看出,该填料塔的分离效率非常低,无论是全回流还是部分回流的理论塔板数都非常低。我认为可能的原因有①填料塔的填料因长时间使用而比较脏,而使得分离能力降低。②冷却水开的比较小,导致气体不能完全冷凝,使得测量出现偏差。
4、本实验的误差来源主要是取样及阿贝折光仪对样品进行遮光度测定所带来的误差。
十、思考题
1、如何判断精馏塔操作已稳定?
答:当塔顶和塔底温度保持不变,且阿贝折光仪的读数恒定时则说明精馏塔操作已经稳定。
2、数据处理时,进行效率计算时,塔釜应如何对待?
答:塔釜若为再沸器,说明气液相在塔釜又经历了一次平衡,分离计算的理论塔板数应减1,若不是再沸器,则不减1.
3、影响效率的因素有哪些,操作中应注意哪些问题?
答:影响效率的因素有:进料组成,进料状态,回流比,塔的结构,塔的稳定性,进料流量,挥发度等。
操作时应注意:①实验开始时先开冷却水,停止时则相反;②要注意检查进料组分浓度;③要等塔稳定后再取样测定;④加热不能过快;⑤折光仪在每次用完后都要用酒精擦拭干净后再用。
4、计算理论塔板数的过程中,进料热状态参数应如何确定?
答:进料参数热状态参数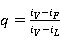 ,即为进料的液相分数,只要取得进料温度、泡点和露点三个温度值,并查阅相关的资料即可得相应温度下进料的相关参数,从而进行计算。
,即为进料的液相分数,只要取得进料温度、泡点和露点三个温度值,并查阅相关的资料即可得相应温度下进料的相关参数,从而进行计算。
