s����d����ds����ҪԪ�ؼ��仯����
(s Block, ds Block, d Block Elements and Compounds)
9.1 s��Ԫ��
s��Ԫ�����(Lithium)����(Sodium)����(Potassium)���(Rubidium)���(Cesium)����(Francium)����Ԫ�ر���Ϊ�����(alkali��Metals)Ԫ�ء��루Beryllium����þ(Magnesium)����(Calcium)����(Strontium)����(Barium)����(Radium)����Ԫ�ر���Ϊ��������(alkaline earth metals)Ԫ�ء�ﮡ�﨡�嵐�����ϡ�н���Ԫ�أ��պ����Ƿ�����Ԫ�ء�
������ͼ�������ԭ�ӵļ۲���ӹ��ͷֱ�Ϊns1��ns2�����ǵ�ԭ���������1��2�����ӣ�������õĽ���Ԫ�ء�
9.1.1 ͨ��
������ͼ��������Ļ������ʷֱ����ڱ�9-1�ͱ�9-2�С�
��9-1�����������
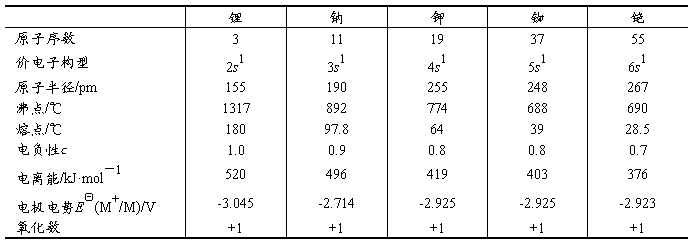
�����ԭ�������ֻ��1��ns���ӣ����������8���ӽṹ(Li�Ĵ������2������)�����ǵ�ԭ�Ӱ뾶��ͬ����Ԫ����(ϡ���������)�����ģ����˵����ͬ����Ԫ��������С�ģ������ڲ���ӵ��������ý�����������ЩԪ�غ�����ʧȥ������1��s���ӣ��Ӷ�ʹ������ĵ�һ��������ͬ����Ԫ������͡���ˣ��������ͬ����Ԫ���н�������ǿ��Ԫ�ء����������ĺ˵�ɱȼ������ԭ�Ӱ뾶�ȼ����С�������Աȼ�����Բ�һЩ��
s��ͬ��Ԫ�����϶������ź˵�ɵ����ӣ�������ԭ�Ӱ뾶�����Ӱ뾶�����ǵ����ܡ��縺���Լ���ԭ�Ե����ʵı仯������˵���й��ɵģ����ڶ����ڵ�Ԫ�ر��ֳ�һ���������ԡ�����﮵�E��(Li+/Li)������С��
��9-2��������������
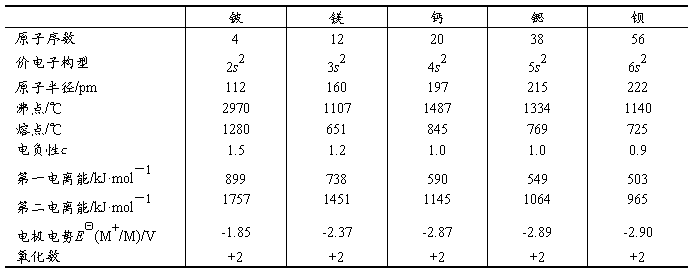
s��Ԫ�ص�һ����Ҫ�ص��Ǹ���Ԫ��ͨ��ֻ��һ���ȶ�������̬��������ĵ�һ�����ܽ�С��������ʧȥһ�����ӣ���������Ϊ��1�����������ĵ�һ���ڶ������ܽ�С������ʧȥ2�����ӣ����������Ϊ��2��
���������ʷ��棬s��Ԫ�ص��ʵ���Ҫ�ص��ǣ��ᡢ�������۵㡣�ܶ���͵���ﮣ�0.53g·cm-3����������Ľ�������ʹ�ܶ������أ����ܶ�ҲС��5���ܶ�С��5�Ľ���ͳ��Ϊ��������������������������Ӳ�ȳ����þ��Ҳ��С�����м�����ơ��ȡ��������õ��У���������⣬��Ӳ�����Ի��Ʋ��������ۡ��е���������������ۡ��е�ϵͣ���������������ԭ�Ӱ뾶��С������2���۵��ӣ���������ǿ�ȱȼ������ǿ�����ۡ��е���Խϸߡ�
s��Ԫ��������õĽ���Ԫ�أ����ǵĵ��ʶ����������ǽ�����Ӧ�����缫���ڿ�����ȼ�ա������롢þ�⣬��������ˮ��Ӧ��s��Ԫ���γ��ȶ������������Щ������������ǿ�
s��Ԫ�����γɵĻ��������������͵ġ��ڶ����ڵ�﮺�������Ӱ뾶С���������ý�ǿ���γɵĻ�����������ǹ����͵ģ�����þ�Ļ�����Ҳ�ǹ����͵ģ�Ҳ��һ����﮵Ļ������������͵ġ�������s��Ԫ�ص�������ˮ��Һ�д�����ˮ�ⷴӦ��
9.1.2 s��Ԫ�ص���Ҫ������
(1)������
(1.1)�������������Ʊ�
����������������������γɶ������͵����������������������������������������O3�����Լ������������ǰ���ֵ���Ҫ�γ���������9-3��
��9-3 s��Ԫ���γɵ�������

���������е���ڿ�����ȼ��ʱ����������������Li2O��
4Li + O2 2Li2O
2Li2O
�����������������Ҳ�����ý��������ǵĹ�����������������ö��õ��ġ�
������
Na2O2 + 2Na 2Na2O
2Na2O
2KNO3 + 10K 6K2O + N2��
6K2O + N2��
����������̼���Ρ������Ρ�����������ȷֽ�Ҳ�ܵõ�������MO�����磺
MCO3 MO + CO2��
MO + CO2��
�����þ�⣬���м�����ͼ����������ֱܷ��γ���Ӧ�Ĺ�������M2��O2��M��O2�����й�������������ļ������������������������������м��ȵ�300�棬��ͨ�벻��������̼�ĸ���������õ�����ɫ��Na2O2��ĩ��
2Na + O2 2Na2O2
2Na2O2
�ơ��ȡ�����������������������ã��õ���Ӧ�Ĺ���������
MO + H2O2 + 7H2O MO2 · 8H2O
MO2 · 8H2O
��ҵ�ϰ�BaO�ڿ����м��ȵ�600������ʹ��ת��Ϊ����������
2BaO + O2 2BaO2
2BaO2
����ﮡ��롢þ�⣬������ͼ����������ֱ����γɳ�������MO2��M(O2)2��һ��˵���������Ժ�ǿ��Ԫ�������γɺ����϶���������˼ء�﨡���ڿ�����ȼ����ֱ�����ɳ�������MO2��������
K + O2  KO2
KO2
(1.2)�������ȶ���
�����������������������������ೣ��������ֱ���O2����O22����O2�����ӡ�
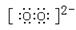 ���������еĸ������ǹ�������O22������ṹʽ������
���������еĸ������ǹ�������O22������ṹʽ������
�� �ۡ�O��O ��ۣϣ��ϣ���2��
���շ��ӹ�����ۣ�O22-�ķ��ӹ�������Ų�ʽΪ��
(��1s)2(��*1s)2(��2s)2(��*2s)2(��2p)2(��2p)4(��*2p)4
����ֻ��һ���Ҽ�������Ϊ1�����ڵ��Ӿ��ɶԣ����O22��Ϊ�����ԡ�
���������еĸ������dz�������O2������ṹʽ������
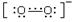
���շ��ӹ�����ۣ�O2���ķ��ӹ�������Ų�ʽΪ��
(��1s)2(��*1s)2(��2s)2(��*2s)2(��2p)2(��2p)4(��*2p)3
O2������һ���Ҽ���һ�������Ӽ�������Ϊ3/2�����ں���һ��δ�ɶԵ��ӣ����O2������˳���ԡ�
��ϵO2��O22����O2���Ľṹ���Կ�����O22����O2���ķ�������ϵĵ��ӱ�O2�࣬������O2С������(�ֱ�Ϊ142��398kJ·mol-1)��O2(498kJ·mol-1)С�����Թ�������ͳ��������ȶ��Բ��ߡ�
(1.3)����
(1.3.1)�۵㼰Ӳ��
����Li+�����Ӱ뾶�ر�С��Li2O���۵�ܸߡ�Na2O�۵�Ҳ�ܸߣ������������δ���۵�ʱ�㿪ʼ�ֽ⡣���������������У�Ψ��BeO��ZnS�;��壬���������ﶼ��NaCl�;��塣��M+��ȣ�M2+��ɶ࣬���Ӱ뾶С�����Լ���������������нϴ�ľ����ܣ��۵㶼�ܸߣ�Ӳ��Ҳ�ϴ�(���ʯӲ��Ϊ10�Ļ���BeO��Ӳ�ȵ���9)����BeO�⣬��MgO��BaO���۵����ν��͡�
BeO��MgO�������²��ϣ�CaO����Ҫ�Ľ������ϣ�Ҳ�������Ƶü۸���˵ļ�Ca(OH)2��
(1.3.2)��ˮ��ϡ��ķ�Ӧ
�������������ˮ�������ɼ�����������MOH��Li2O��ˮ��Ӧ������Rb2O��Cs2O��ˮ�������ҷ�Ӧ�����������������ﶼ��������ˮ�İ�ɫ��ĩ��BeO��������ˮ��Ӧ��MgO��ˮ������Ӧ������Ӧ�ļ
M2O + H2O 2MOH
2MOH
MO + H2O M(OH)2
M(OH)2
����������ˮ��ϡ���������·�Ӧ���ɹ���������
Na2O2 + 2H2O 2NaOH + H2O2
2NaOH + H2O2
Na2O2 + H2SO4(ϡ) Na2SO4 + H2O2
Na2SO4 + H2O2
����������ˮ��Ӧ�������������������⡣������
2KO2 + 2H2O 2KOH + H2O2 + O2��
2KOH + H2O2 + O2��
��ˣ�����������ǿ��������
(1.3.3)�������̼������
���������������̼��Ӧ���ų�������
2Na2O2 + 2CO2 2Na2CO3 + O2��
2Na2CO3 + O2��
���������������̼���÷ų�������
4KO2 + 2CO2 2K2CO3 + 3O2��
2K2CO3 + 3O2��
KO2�����Ʊ��������ڼ������У�����������Ӧ�ṩ������
���⣬��������Ҳ��һ��ǿ����������ҵ������Ư����Ҳ����������Ϊ�Ƶ���������Դ��Na2O2������ʱ�������ֽ⣬����������ľ̿�����۵Ȼ�ԭ������ʱ���ͻᷢ����ը��ʹ��Na2O2ʱӦ��ע�ⰲȫ��
(2) ��������
������ͼ������������������ڿ���������ˮ�����⣬�ʹ���NaOH��Ca(OH)2�������������
(2.1)�ܽ���
�����������������ˮ�ж������ܵģ��ܽ�ʱ���ų��������ȡ���������������������ܽ�����С������Be(OH)2��Mg(OH)2�����ܵ����������������������������ܽ�������9-4�С��ɱ������ݿɼ����Լ���������˵����Be(OH)2��Ba(OH)2���ܽ���������������������Ž������Ӱ뾶����������������֮�����������С������Ϊˮ�����������Ե�ʡ�
��9-4������������������ܽ��(20��)
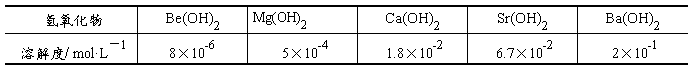
(2.2)�����
��������������������������У���Be(OH)2Ϊ�������������⣬�������������ﶼ��ǿ�����ǿ�������Ԫ������������Եݱ�Ĵ���������
LiOH��NaOH��KOH��RbOH��CsOH
��ǿ�� ǿ�� ǿ�� ǿ�� ǿ��
Be(OH)2��Mg(OH)2��Ca(OH)2��Sr(OH)2��Ba(OH)2
���� ��ǿ�� ǿ�� ǿ�� ǿ��
�����������������Եݱ���ɣ��������µ�ROH���ɼ��Խ��͡�
�����������������������ļ��Ժ��ܽ�ȵݱ���ɿ��Թ���������
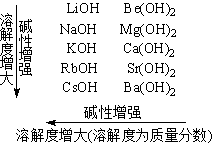
(3) ��Ҫ������
Ӧ��ע�⣬�����������������ܶ�������Ҳ�ܶ���
(3.1)�����������ۡ��е�
��������δ�����������;��壬���ǵ��۵㡢�е�ϸߡ�����Li+���Ӱ뾶��С����������ǿ������ijЩ��(��±����)�б��ֳ���ͬ�̶ȵĹ����ԡ������������Ӵ���������ɣ������Ӱ뾶����Ӧ�ļ����С�������ǵļ�������ǿ����˼��������ε����Ӽ������ϼ�����IJ�����Ž������Ӱ뾶��������������Ҳ��ǿ�����磬���������Ȼ�����۵��Be��Ba����������
�Ȼ��� BeCl2 MgCl2 CaCl2 SrCl2 BaCl2
�۵㣯�� 405 714 782 876 962
���У�BeCl2���۵����Եصͣ���������Be2+�뾶С����������ǿ������Cl-��Br-��I-�ȼ����ʽϴ���������γɵĻ������ѹ���Ϊ���ۻ����
(3.2)�ܽ��
�����������������������ˮ���������̼���Ρ������ε��ܽ�ȴ�Li��Cs�������������������������ˮ������LiF��LiCO3��Li3PO4��NaZn(UO2)3(CH3COO)9·6H2O��KClO4��K2��PtCl6�ݵȡ����������������У���±������������⣬����������������ֻ�нϵ͵��ܽ�ȣ��������ǵ�̼���Ρ��������Լ������εȶ���������(BeC2O4����)�������ж��������ܵģ�þ���в����ܣ����ơ��ȡ����������Ϊ���ܣ���������CaC2O4���ܽ��Ϊ��С����˳������ɰ�ɫCaC2O4�ij�����Ӧ������Ca2+��������Щ�ε��ܽ�Ⱥ�С����Щ����������Ȼ���оͻ����Ϊ��ʯ����Ҫ�Ŀ�ʯ����þ��(CaCO3)������ʯ(MgCO3·CaCO3)������ʯ�ʹ���ʯ(CaCO3)���ؾ�ʯ(BaSO4)��ʯ��(CaSO3·2H2O)�ȡ�
(3.3)���ȶ���
��������γ������μ�̼�����һ�㶼���н�ǿ���ȶ��ԣ���800�����¾����ֽ⡣
2NaNO3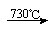 2NaNO2 + O2
2NaNO2 + O2
��ˣ�����������Na2CO3���۽������������ʡ�
BaSO4(�ؾ�ʯ) + 2NaNO3 BaCO3 + 2Na2SO4
BaCO3 + 2Na2SO4
���������ε��ȶ�����Խϲ���ڳ����»����ȶ��ģ�ֻ���������⡣���磬BeCO3���Ȳ���100��ͻ�ֽ⡣
(4) Li��Be�������Լ��Խ��߹���
(4.1)Li��Mg��Be��Al��������
�ֻ���������Ӳ㣬Li+�뾶�ر�С��ˮ�����ر����ʹ﮺�ͬ������Ԫ����Ƚ��������������ʣ����͵ڶ���Mg�������ԡ�����Li��ͬ��Ԫ���нϸߵ��ۡ��е��Ӳ�ȣ�Li�����ɹ��������Mg3N2һ����Li3N���ȶ��Ļ����Li�͵ڶ���һ���ܺ�ֱ̼������Li2C2��Li���γ��ȶ����������Li(NH3)4��I��Li2CO3��Li3PO4��LiF�ȽԲ�����ˮ��LiOH�ܽ�ȼ�С�������ֽ⣬���ȶ���Li�Ļ������й����ԣ����������л��ܼ��еȡ�
�뼰�仯��������ʺ�ͬ����������Ԫ�ؼ��仯����Ҳ�����ԵIJ��졣����۵㡢�е���������������ߣ�Ӳ��Ҳ�Ǽ������������ģ������д��ԡ����н�ǿ���γɹ��ۼ�����������BeCl2�����ڹ����ͻ������������������������������϶��������͵ġ�����͵���������������ԡ�������������Խ��������������ᣬҲ������ǿ�������ı��缫���������E��(Be2+/Be)��-1.70V��E��(Al3+/Al)��-1.66V��������������ܱ����Ũ����ۻ��������������������۵�ߡ�Ӳ�ȴ�����ʣ����������������Be(OH)2��Al(OH)3������������������Ҷ�������ˮ��������ķ����ﶼ���������ķ������γ�������Na2��BeF4�ݡ�Na3��AlF6�ݣ����ǵ��Ȼ���廯��⻯�ﶼ������ˮ����������Ȼ��ﶼ�ǹ����ͻ�������������ۺϡ��������л��ܼ���
(4.2)�Խ��߹���
�����������Լ����Ƶġ��Խ��ߡ������ԡ���s����p��Ԫ���У�����ͬ��Ԫ�ص����������⣬����һЩԪ�ؼ��仯��������ʳ��ֳ����Խ��ߡ����ơ���ν�Խ������Ƽ���A���Li���A���Mg����A���Be���A���Al����A���B������Si������Ԫ�������ڱ��д��ڶԽ���λ����
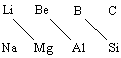
���ڱ��У�ijԪ�ؼ��仯����������������Ϸ������·�Ԫ�ؼ��仯�������ʵ������Ծͳ�Ϊ�Խ��߹���
�Խ��߹����Ǵ��й�Ԫ�ؼ��仯����������������ܽ�����ľ�����ɣ��Դ˿��������Ӽ����Ĺ۵���Դ��Ե�˵����ͬһ�����������ӹ�����ͬ�Ľ������ӣ��������������ӵ�ɵ����Ӷ��������õ���ǿ��ͬһ������ͬ�Ľ������ӣ����϶��������Ӱ뾶�������ʹ�ü������ü�������ˣ��������ڱ����������¶Խ���λ���ϵ��ڽ�����Ԫ�أ����ڵ�ɺͰ뾶��Ӱ��ǡ���෴�����ǵ����Ӽ������ñȽ�������Ӷ�ʹ���ǵĻ�ѧ���ʱȽ����ơ��ɴ˷�ӳ�����ʵĽṹ������֮���������ϵ��
(5) Ӳˮ��������
��ҵ�ϸ���ˮ��Ca2+��Mg2+�ĺ���������Ȼˮ��Ϊ���������н϶���Ca2+��Mg2+��ˮ����Ӳˮ����������Ca2+��Mg2+��ˮ������ˮ��
(5.1)��ʱӲˮ������Ӳˮ
����̼�����Ca(HCO3)2��̼����þMg(HCO3)2��Ӳˮ����к���������ʽ̼���ξͷֽ�Ϊ�����Ե�̼���Ρ�������
Ca(HCO3)2  CaCO3��+ H2O + CO2��
CaCO3��+ H2O + CO2��
2Mg(HCO3)2 Mg2(OH)2CO3��+ H2O + 3CO2��
Mg2(OH)2CO3��+ H2O + 3CO2��
���������״�ˮ�г�ȥCa2+��Mg2+��ˮ��Ӳ�Ⱦͱ���ˣ�������Ӳˮ������ʱӲˮ��
��������þMgSO4�������CaSO4���Ȼ�þMgCl2���Ȼ���CaCl2�ȵ�Ӳˮ��������У�ˮ��Ӳ��Ҳ������ʧ������ˮ��������Ӳˮ��
(5.2)Ӳˮ������
����Ӳˮ��Ca2+��Mg2+�Ĺ��̽���Ӳˮ�����������õ�����������ʯ�Ҵ�������ӽ�����֬����ˮ����
����Ӳˮ�����ô���������������ơ�þ�������κ��Ȼ��ﷴӦ�����������Ե��Σ�ʹ����Ӳˮʧȥ����Ӳ�ԡ���ҵ��������ʯ�Һʹ����һ��������ˮ����������Ϊʯ�Ҵ������Ӧ����ʽ������
MgCl2 + Ca(OH)2 Mg(OH)2��+ CaCl2
Mg(OH)2��+ CaCl2
CaCl2 + Na2CO3 CaCO3��+ 2NaCl
CaCO3��+ 2NaCl
��Ӧ�����ټӳ�����(��������)���������õ���ˮ��ʯ�Ҵ�������Ƚϸ��ӣ�����Ч���ϲ���ɱ��ͣ����ڴ�����������Ӳ�Ƚϴ��ˮ�����磬���糧���ȵ�վ��һ����ø÷���Ϊˮ�����ij���������
9.2 d��Ԫ��
����Ԫ�ذ�����B����B��͵ڢ��干30���Ԫ�ء�ͨ���ְѹ���Ԫ�طֳɵ�һ����ϵ(���ֵ�п)���ڶ�����ϵ(���Ƶ���)�͵�������ϵ(���絽������������ϵԪ��)����һ����ϵ��Ԫ�ؼ��仯����Ӧ�ýϹ㣬����һ���Ĵ����ԡ������ص����۵�һ����ϵ��
9.2.1 ͨ��
(1)�й�ԭ�Ӳ�����������
����Ԫ�ص�һ���������ڱ�9-5��
����Ԫ�صļ۵��Ӳ�������������s���ӣ������������ȫ����d����(Zn��Cd��Hg����)�������ĵ��ӹ���ʹ���������γɶ����������Ļ�������ǵ�������������������s���Ӻʹ����d���������ܺ͡����ڵڢ��塢��B����B������һ���ɲ���ȫ
��9-5 ����Ԫ�ص�һ������
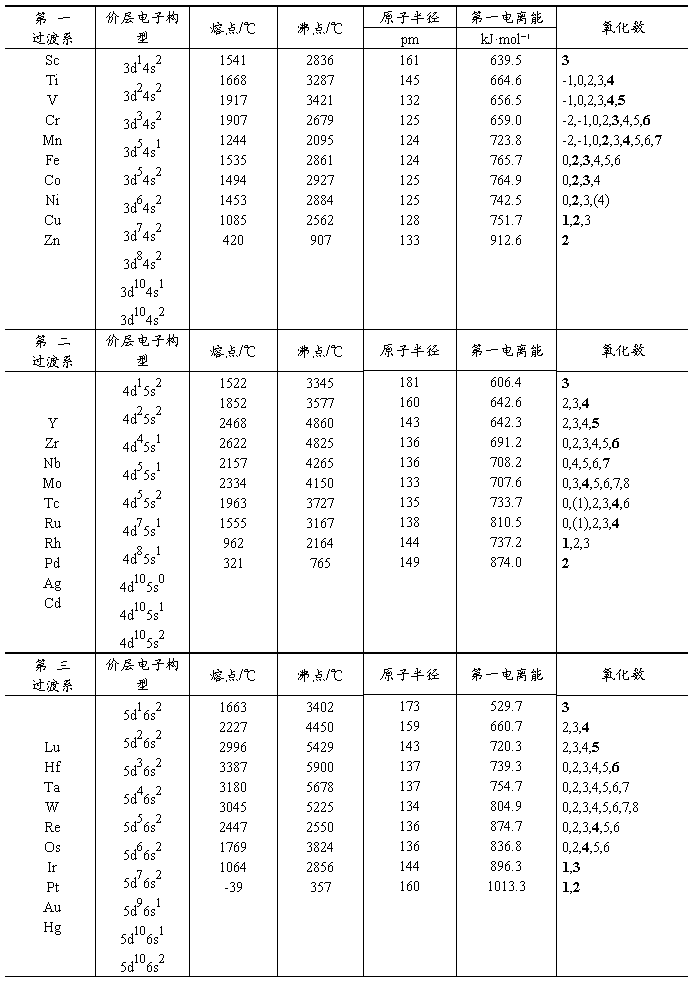
ע�����к�������Ϊ������������������Ϊ0�ı�ʾ����Ԫ���γ��ʺ���ʱ����������
���á����⣬����B����B���е�Zn��Cd�⣬��������Ԫ�ص����������ǿɱ�ġ�
���нϵ��������Ĺ���Ԫ�أ����ԡ�������(M+��M2+��M3+)���ڡ�
(2)��Ҫ��������
����Ԫ�ش��Ǹ��۵㡢�߷е�(Zn��Cd��Hg����)���ܶȴ���͵����������õ��ؽ��������ǹ㷺�ر�����ұ��ҵ������Ͻ�֣����粻���(������)�����ɸ�(����)���̸ֵȡ��۵���ߵĵ������٣�Ӳ�������Ǹ��������ܶ��������(Os)��
(3)��Ҫ��ѧ����
��Sc����Y����La�ǹ���Ԫ��������õĽ��������磬�ڿ�����Sc��Y��La��Ѹ�ٵر���������ˮ���÷ų��⡣���ǵĻ����Խӽ��ڼ���������Sc��Y��La������֮���ԱȽϻ��ã�����Ϊ���ǵ�ԭ�Ӵ����d����н���һ�����ӣ�������Ӷ����ǵ�Ӱ���в��������������ǵ����ʽϻ��ò��ӽ��ڼ���������
ͬһ��Ĺ���Ԫ�س���B���⣬�������嶼�����϶��»����Խ��͡�һ����Ϊ��������ͬ��Ԫ�����϶���ԭ�Ӱ뾶���Ӳ����˵����ȴ���ӽ϶࣬�Ե���������ǿ�����Եڶ���������ϵԪ�صĻ����Լ����½����ر������Ժ�ĵ�������ϵ��Ԫ�أ�������ϵ������Ӱ�죬���ǵ�ԭ�Ӱ뾶��ڶ�����ϵ��Ӧ��Ԫ�ص�ԭ�Ӱ뾶������ȡ���˵ڶ���������ϵ��ͬ��Ԫ�ؼ��仯����������Ϻ����ơ����磬���������Ȼ���б˴˹�����һ�𣬰����ǵĻ�������뿪�Ƚ����ѡ������Ҳ��������ͬһ����ϵ��Ԫ���ڻ�ѧ�������ϣ��ܵ���˵�������Ҽ��������Ǽ����ij̶Ȳ���
����Ԫ�ص�ԭ�ӻ����Ӷ����пյļ۵��ӹ�������ֵ��ӹ���Ϊ������λ��ŶԵ����γ���ۼ�������������������ǵ�ԭ�ӻ����Ӷ����γ�����������
(4)���ӵ���ɫ
����Ԫ�صĴ����ˮ�����ӳ�����һ������ɫ��������������ɫ��ԭ���Ǻܸ��ӵģ�����Ԫ�ص�ˮ������֮���Ծ�����ɫ�������ǵ����Ӿ���δ�ɶԵ�d�����йء�����Ԫ�ص��������Ӿ���δ�ɶԵ�d���ӣ�û��δ�ɶ�d���ӵ�������Sc3+��Zn2+��Ag+��Cu+�ȶ�����ɫ�ģ�������δ�ɶ�d���ӵ���������ֳ���ɫ����Cu2+��Cr3+��Co2+�ȡ�
��������������Ԫ����Ҫ�����¼����ص���
��ͬһ��Ԫ���ж�����������
�ڽ��������ԣ�
�������γɶ�������
��ˮ�����Ӻ�������ӳ�������ɫ��
9.2.2 ������Ҫ������
��������Ư����ɫ�ܸߵ�Ӳ�ȣ���˳���������������������װ�κͱ������á��������γɺϽ��ڸ������͵IJ�����м������нϸ߱����ĸ��������к��и�14%���ң�����Dz���֡�
��ԭ�ӵļ۵�����3d54s1�����������������+6����Ҳ��+5��+4��+3��+2�ġ�����Ҫ����������Ϊ+6��+3�Ļ����������Ϊ+5��+4��+2�Ļ����ﶼ���ȶ���
����Ԫ�ص���ͼ���£�
������Һ��E��A/V
Cr2O72-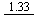 Cr3+
Cr3+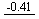 Cr2+
Cr2+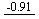 Cr
Cr

������Һ��E��B/V
CrO42-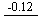 Cr(OH)3
Cr(OH)3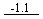 Cr(OH)2
Cr(OH)2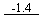 Cr
Cr
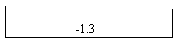
(1)��(��)�Ļ�����
(1.1)�����������������ܽ����������
���������������ܺͼ����ۻ���������֮һ���۵���2275�棬����ˮ�������ᡣ���չ���Cr2O3������ˮ��Ҳ�������ᡣ�ڸ����������뽹����طֽ�ų���SO3���ã��γɿ����Ե������Cr2(SO4)3��
Cr2O3 + 3K2S2O7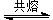 Cr2(SO4)3��3 K2SO4
Cr2(SO4)3��3 K2SO4
Cr2O3�Ǿ��������ȶ��Ե���ɫ���ʣ�������������(����)��������Ҳ���������л��ϳɵĴ�����������ȡ�������������ԭ��֮һ��
��������Cr(OH)3���������ļ������ڸ�����Һ(pHԼΪ5.3)�����ɵĻ���ɫ������
Cr3+ + 3OH- Cr(OH)3��
Cr(OH)3��
Cr(OH)3��������������������ᣬ������ɫ����ɫ��ˮ��������(����Cr3+��ˮ�����������������¶ȡ�Ũ�ȡ���ȵȶ��ı䣬������ɫҲ������ͬ)������Һ�нᾧ���ĸ��δ�Ϊ��ɫ���塣Cr(OH)3��ǿ������������ɫ��������[Cr(OH)4]-(��ΪCr(OH) 63-)��
Cr(OH)3 + OH- Cr(OH)4-
Cr(OH)4-
����Cr(OH)3�����Ժͼ��Զ���������˸�(��)�κ����ǻ��ϸ�(��)����(���Ǹ�����)��ˮ������ˮ�⡣
(1.2)���ε��Ʊ�����������µĻ�ԭ��
���ط�KCr(SO4)2·12H2O����SO2��ԭ�ظ����K2Cr2O7��Һ���Ƶõ�����ɫ������
K2Cr2O7 + H2SO4 +3SO2  2KCr(SO4)2 + H2O
2KCr(SO4)2 + H2O
��Ӧ�������﹤ҵ�ͷ�֯��ҵ��
��Ȼ���д��ڵĸ�(��)���и�����Fe(CrO2) 2���Ѹ������̼�����ڿ��������տɵø����Σ���ҵ�ϰ����ַ����м��۷���
4Fe(CrO2)2 + 8Na2CO3 + 7O2 8Na2CrO4 + 2Fe2O3 + 8CO2
8Na2CrO4 + 2Fe2O3 + 8CO2
�����õ������У���ˮ���Ѹ����ν�ȡ������
�Ӹ���Ԫ�ص���ͼ���Կ������ڼ��������¸�(��)���н�ǿ�Ļ�ԭ�ԣ��ױ������������ڼ��Խ����У�Cr3+�ɱ�ϡ��H2O2��Һ������
2Cr(OH)4- + 2OH�� + 3H2O2  2CrO42- + 8H2O
2CrO42- + 8H2O
(��ɫ) (��ɫ)
�����������¸�(��)���н�ǿ���ȶ��ԣ�ֻ����ǿ��������������K2S2O8������ʹCr3+������
2Cr3+��3S2O82-��7H2O �� Cr2O72-��6SO42-��14H+
(2)��(��)�Ļ�����
(2.1)������ͺ�����
ŨH2SO4�����ڱ��͵�K2Cr2O7��Һ����������(��)�����������������CrO3��
K2Cr2O7��H2SO4(Ũ)  2CrO3����K2SO4��H2O
2CrO3����K2SO4��H2O
CrO3�ǰ���ɫ��״���塣�����״ӿ���������ˮ�֣�����������ˮ���γɸ��ᡣCrO3�����ȳ������۵�(196��)ʱ���ͷֽ�ų�������ΪCr2O3��CrO3�ǽ�ǿ����������һЩ�л�������ƾ��������Ӵ�ʱ���Ż�ͬʱCrO3����ԭΪCr2O3��CrO3�ǵ�Ƹ�����Ҫԭ�ϡ�
CrO3��ˮ�������ɸ���H2CrO4���ظ���H2Cr2O7��
(2.1.1)������ظ����������������
H2Cr2O4��H2Cr2O7����ǿ�ᣬ���������Ը�ǿЩ��H2Cr2O7�ĵ�һ���������ȫ����
HCr2O7-  Cr2O72- + H+ K2q = 0.85
Cr2O72- + H+ K2q = 0.85
H2CrO4 HCrO4- + H+ K1q = 9.55
HCrO4- + H+ K1q = 9.55
HCrO4-  CrO42- + H+ K2q = 3.2×10-7
CrO42- + H+ K2q = 3.2×10-7
�����κ��ظ�����CrO42-��Cr2O72-����Һ�д�������ƽ����
2CrO42- + 2H+  2HCrO4-
2HCrO4- Cr2O72- + H2O
Cr2O72- + H2O
(��ɫ) (�Ⱥ�ɫ)
�ڼ��Ի�������Һ����Ҫ�Ի�ɫ��CrO42-���ڣ���pH��2����Һ�У���Ҫ��Cr2O72- (�Ⱥ�ɫ)��ʽ���ڡ����������ڵ�ƽ���ϵ�Ϳ�������Ϊʲô��Na2CrO4��Һ�м�������ܵõ�Na2Cr2O7������Na2Cr2O7����Һ�м�����̼����ʱ���ֿ��Եõ�Na2CrO4��������
2Na2CrO4 + H2SO4 Na2Cr2O7 + H2O + Na2SO4
Na2Cr2O7 + H2O + Na2SO4
Na2Cr2O7 + 2NaOH  2Na2CrO4 + H2O
2Na2CrO4 + H2O
(2.1.2)�ظ��ἰ���ε�������
�ڼ��Խ����У���(��)�����������ܲ�����Խ��������ǽ�ǿ������������ʹ�������Һ�У�Cr2O72-Ҳ�ܰ�H2S��H2SO3��HI�������������ڼ��ȵ��������������HBr��HCl��
Cr2O72- + 3H2S + 8H+ 2Cr3+ + 3S��+ 7H2O
2Cr3+ + 3S��+ 7H2O
Cr2O72- + 6Cl- + 14H+ �� 2Cr3+ + 3Cl2��+ 7H2O
ʵ���ҳ��õĸ���ϴҺ������Ũ����ͱ���K2Cr2O7��Һ���ƶ��ɣ����ڽ�ϴ����ϴһЩ��������ȥ��ԭ�Ի���Ե�����ر����л������ϴҺ���Է���ʹ�ã�ֱ��ϴҺ���̲�ʧЧ��
�����ظ����(NH4)2Cr2O7�ڼ��ȵ�����£�Ҳ�ܷ���������ԭ��Ӧ��
(NH4)2Cr2O7 �� Cr2O3 + N2 + 4H2O
ʵ���ҳ�������һ��Ӧ����ȡCr2O3��
(2.1.3)�����κ��ظ����ε��ܽ���
һЩ�����ε��ܽ��Ҫ���ظ�����ΪС�������������Һ�м���Ba2+��Pb2+��Ag+ʱ�����γ�������ˮ��BaCrO4(���ʻ�ɫ)��PbCrO4(����ɫ)��Ag2CrO4(ש��ɫ)������
���⣬�Ӹ����κ��ظ����δ��ڵ�ƽ���ϵ�У����з�ӦҲ�ǿ����������
4Ag+ + Cr2O72- + H2O 2Ag2CrO4��+ 2H+
2Ag2CrO4��+ 2H+
������Ϊ+3��+6�ĸ����������е��ת����ϵ���ܽ�������
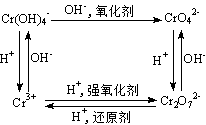
(2.2)��(��)��(��)�ļ���
��Cr2O72-����Һ�м���H2O2����������ɫ�Ĺ�������CrO5��д��CrO(O2)2����ṹΪ��
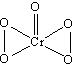
Cr2O72- + 4 H2O2 + 2H+ 2CrO5 + 5H2O
2CrO5 + 5H2O
��2CrO42- + 3H2O2 + 2H+ 2CrO5 + 4H2O
2CrO5 + 4H2O
CrO5�ܲ��ȶ����ܿ�ֽ�ΪCr3+���ų�O2���������ѻ��촼��Һ�н��ȶ�����һ��Ӧ������������CrO42-��Cr2O72-�Ĵ��ڡ�
�����Ǹ�(��)�ļ�������(��)�ļ������ȰѸ�(��)��������(��)���ټ���������������
Cr3+ 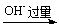 Cr(OH)4-
Cr(OH)4-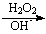 CrO42-
CrO42-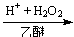 CrO5 (��ɫ)
CrO5 (��ɫ)
�� Cr3+ 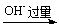 Cr(OH)4-
Cr(OH)4-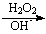 CrO42-
CrO42-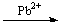 PbCrO4��(��ɫ)
PbCrO4��(��ɫ)
9.2.3 �̵���Ҫ������
�̵������������ƣ�������Ҫ��;������Ͻ𣬼������еĸ��ж������̡�
��ԭ�ӵļ۵�����3d54s2����Ҳ������������̬����Ԫ�أ������γ��������ɣ�3����7�Ļ������������������2����4����7�Ļ��������Ҫ��
�̵�Ԫ�ص���ͼ���£�
������Һ��E��A/V
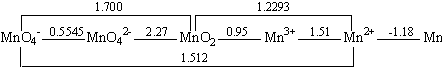
������Һ��E��B/V

(1)��(��)�Ļ�����
(1.1)�����������������ܽ����뻹ԭ��
һ����������ɫ��ĩ��������ˮ���������ᡣ��MnO��Ӧ��ˮ����Mn(OH)2�Ǵ���(��)�������Һ���ö��Ƶõ���
Mn2+ + 2OH-  Mn(OH)2��
Mn(OH)2��
Mn(OH)2�ǰ�ɫ������ˮ�����ʡ��ڿ����кܿ챻�������������ɫ��MnO2��ˮ������
Mn(OH)2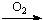 Mn2O3 · xH2O
Mn2O3 · xH2O 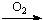 MnO2 · yH2O
MnO2 · yH2O
(1.2)��(��)�ε��ȶ�����Mn2+�ļ���
�ܶ�������������ˮ�ġ�����Һ�нᾧ�����������Ǵ��нᾧˮ�ķۺ�ɫ���塣���磬MnCl2·4H2O��MnSO4·7H2O��Mn(NO3)2·6H2O��Mn(ClO4)2·6H2O�ȡ�
���̵�Ԫ�ص���ͼ���Կ������ڼ�����������(��)���н�ǿ�Ļ�ԭ�ԣ��ױ���������������������(��)���н�ǿ���ȶ��ԣ�ֻ����ǿ��������PbO2��NaBiO3��(NH4)2S2O8�Ȳ���ʹMn2+����ΪMnO4-��������HNO3��Һ�У�Mn2+��NaBiO3��Ӧ������
2Mn2+ + 5NaBiO3 + 14H+  2MnO4�� + 5Bi3+ + 5Na+ + 7H2O
2MnO4�� + 5Bi3+ + 5Na+ + 7H2O
��һ��Ӧ����������Mn2+�Ĵ��ڡ�
(2)��(��)�Ļ�����D�D�������̵��ȶ���
������������(��)���ȶ��Ļ��������Ȼ�����������̿�MnO2·xH2O��ʽ���ڡ�MnO2����ȡ�̵Ļ����P�����̵���Ҫԭ�ϣ����Dz�����ˮ�ĺ�ɫ��̬���ʡ��ڿ����м��ȵ�530��ʱ�ͷų�����
3MnO2 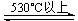 Mn3O4 + O2��
Mn3O4 + O2��
MnO2�н�ǿ����������������Ũ�����ŨH2SO4��MnO2�ڼ���ʱ����ʽ���з�Ӧ��
MnO2 + 4HCl �� MnCl2 + 2H2O + Cl2��
2MnO2 + 2H2SO4 �� 2MnSO4 + 2H2O + O2��
MnO2���̴����м��������������ܱ���ԭΪ��(��)��Ҳ���Ա�����Ϊ��(��)(�ڼ���������)�����磬��MnO2��KOH��K2CO3�ڿ����м��ȹ��ۣ���õ�������ˮ����ɫ���塣����������ˮ�ɴ�������������ɫ�������K2MnO4���塣�ⱻ��Ϊ���۷�������K2MnO4�ķ�ӦʽΪ��
2MnO2 + 4KOH + O2 ���� 2K2MnO4 + H2O
��Ӧ�е���������KClO3��KNO3����������������
3MnO2 + 6KOH + KClO3 ���� 3K2MnO4 + KCl + 3H2O
(3)��(��)�Ļ�����
��(��)�Ļ������У��Ƚ��ȶ����������Σ��������K2MnO4������MnO2��KOH�ڿ����м��ȶ��Ƶá����ἰ��������MnO3���Ǽ����ȶ��Ļ���������δ���������������������ˮ��ֻ���ڼ���(pH��13.5)��Һ�в����ȶ��ģ������������£�MnO42-����ɫ���Խϳ�ʱ�䱣�ֲ��䡣�෴�أ������Ի�������Һ�У���ɫ��MnO42-˲���绯������ɫ��MnO4-����ɫ��MnO2������
3MnO42- + 4H+  MnO2��+ 2MnO4- + 2H2O
MnO2��+ 2MnO4- + 2H2O
����������(������)�����������ε���Һʱ�������ο��Ա�Ϊ����������
2MnO42- +Cl2 2MnO4- + 2Cl-
2MnO4- + 2Cl-
(4)��(��)�Ļ�����
��(��)�Ļ������У��������������ȶ��ġ�Ӧ�����ĸ��������Ǹ������KMnO4��������HMnO4ֻ�ܴ�����ϡ��Һ�У���Ũ������Һ����20��ʱ�����ֽ�����MnO2��O2��������Ҳ��ǿ��֮һ��
(4.1)������ص������Լ��仹ԭ����
��������ǰ���ɫ���壬������Һ���ֳ�MnO4-���е���ɫ��KMnO4���������200������ʱ����ʽ�ֽ���
2 KMnO4 �� K2MnO4 + MnO2 + O2��
��ʵ��������ʱҲ������һ��Ӧ��ȡ����������
KMnO4������Ҫ�ͳ��õ�������֮һ�����������н�ǿ�������������ܽ���ԭ����������������ͬһԪ�صĽϸߺͽϵ��������Ļ�����Ҳ�ܷ���������ԭ��Ӧ���õ�����м��������Ļ��������MnO4-��Mn2+�����Խ���������MnO2��
2MnO4- + 3 Mn2+ + 2H2O  5MnO2��+ 4H+
5MnO2��+ 4H+
����Ϊ������������ԭ�IJ������ʵ�����Բ�ͬ����ͬ�����磬��������������ԭ���������Խ����У��䷴Ӧ������
2MnO4- + 6H+ + 5SO32��  2Mn2+ + 5SO42- + 3H2O
2Mn2+ + 5SO42- + 3H2O
����H2S����ԭ����MnO4-�ɰ�H2S������S�����ɽ�һ����S����ΪSO42-��
2MnO4- + 5H2S + 6H+  2Mn2+ + 5S + 8H2O
2Mn2+ + 5S + 8H2O
6MnO4- + 5S + 8H+  6Mn2+ + 5SO42- + 4H2O
6Mn2+ + 5SO42- + 4H2O
�����Խ�������
2MnO4- + H2O + 3SO32- 2MnO2��+ 3SO42- + 2OH��
2MnO2��+ 3SO42- + 2OH��
�ڽ�Ũ����Һ����
2MnO4- + 2OH�� + SO32- 2MnO42- + SO42- + H2O
2MnO42- + SO42- + H2O
��ԭ���ﻹ�����������뻹ԭ��������IJ�ͬ����ͬ������MnO4- �� SO32-�����������µķ�Ӧ����SO32-������MnO4- �Ļ�ԭ����ΪMn2+����MnO4- �����������յĻ�ԭ����ΪMnO2��
(4.2)���������Һ���ȶ���
��KMnO4��Һ�У�������������ڣ���MnO4-����ʽ���л����ķֽ���
4MnO4- + 4H+  4MnO2��+ 3O2��+ 2 H2O
4MnO2��+ 3O2��+ 2 H2O
�����Ի���Խ�����Ҳ��ֽ⣬����Mn2+�Ĵ��ڣ��Լ��ֽ����MnO2�����յȻ���ٽ��ֽ⡣����MnO4-���ڷ���Ҳ�Ỻ���ط���������Ӧ����һ��ӦҲ˵��HMnO4�Dz��ȶ����ᡣ
��Ũ����Һ�У�MnO4-�ܱ�OH-��ԭΪ��ɫ��MnO42-�����ų�O2��
4MnO4- + 4OH-  4MnO42- + O2��+ 2 H2O
4MnO42- + O2��+ 2 H2O
ǰ���ᵽ���ü��۷����ܰ�MnO2����ΪMnO42-��ȴ����ֱ�Ӱ�MnO2����ΪMnO4-����ԭ�����MnO4-��ǿ���в��ȶ���
9.2.4 �����ܡ�������Ҫ������
�����ܺ���ԭ���������Ӷ���4s2�������3d���ӷֱ���3d6��3d7����3d8�����ǵ���������������+2��+3�������ܺ��������ʱȽ������ͨ����������Ԫ�س�����ϵԪ�ء�
�ӵ��������������ܡ��������ֳ����ԡ��������еȡ����������Ũ�����ж����ɶ�̬�����ڶ�̬�������ܡ���һ�㲻������ϡ�����С����⣬�����ܡ���������������ã������ܱ��ȵ�Ũ������ʴ�����ܺ����ڼ�����Һ���ȶ��Ա����ߣ����ۼ�ʱ���ʹ����������
(1)�����ܡ��������������������
(1.1)������Ļ����������Ʊ�
��ɫ��FeO������ɫ��CoO����ɫ��NiO����������ˮ�ļ�����������ǿ��������ܺ�������Ӧ�������ڸ��������������¼����Ƶá����磬��������������ȡFeO�ķ�ӦʽΪ��
FeC2O4 FeO + CO��+ CO2��
FeO + CO��+ CO2��
����ɫ��Fe2O3������ɫ��Co2O3�Լ��Һ�ɫ��Ni2O3����������ˮ������ƫ��������ʵ�����У�������������Fe(OH)3������ˮ���Ƶýϴ���Fe2O3��С�ļ���Co(NO3)2��Ni(NO3)2�����Ƶ�Co2O3��Ni2O3��
�������γ���ν+2��+3�Ļ�������������������Fe3O4���ɿ�����FeO��Fe2O3�Ļ��������FeO·Fe2O3����X�����о�֤����Fe3O4��һ����(��)���Σ���Fe����Fe��2O4�ݡ����Ǿ��д��ԵĻ�����ܡ���Ҳ�����Ƶ��������Co3O4��Ni3O4��
(1.2) Co2O3��Ni2O3��������
������Ϊ+3���ܺ������������������Һ�о���ǿ�����ԣ���Դ�����߸�ǿ������Co2O3��ŨHCl���÷ų�Cl2��
Co2O3 + 6HCl 2CoCl2 + Cl2��+ 3H2O
2CoCl2 + Cl2��+ 3H2O
(1.3)���������������ԭ�����Ʊ�
��ɫ��Fe(OH)2���ۺ�ɫ��Co(OH)2��Co(OH)2����ʱΪ��ɫ�����û���Ⱥ�ת��Ϊ�ۺ�ɫ����ƻ���̵�Ni(OH)2�ܽ��ԡ����������Ӧ����������������ơ�Fe(OH)2��Co(OH)2��Ni(OH)2������ǿ��������+2�������������ܺ�������Һ���Ƶá�
Fe(OH)2����Һ������ʱ��������ȫ�������Һ�е��������������ò�������Fe(OH)2����ΪFe(OH)2ǿ�ҵ����տ����е�����Ѹ�ٱ�����Ϊ����ɫ������ɫ���м����(���в���+2����������������Ϊ+3������)�������㹻��������ʱ������ȫ��������ΪFe(OH)3��
4Fe(OH)2 + O2 + 2H2O  4Fe(OH)3
4Fe(OH)3
��Co(OH)2��Ƚϻ����ر���������ΪCo(OH)3��Ni(OH)2�ڿ����к��ȶ���ֻ����ǿ������(��NaOCl)����ʱ�����ܰ�Ni(OH)2����ΪNi(OH)3��
����ɫ��Fe(OH)3������ɫ��Co(OH)3�Լ���ɫ��Ni(OH)3�Ļ�������ͬ������Ӧ����������������ơ�ǿ��������+3��������������Һ������Fe(OH)3�����������ΪFe2O3·H2O��ͨ������д��Fe(OH)3��FeO(OH)���ܡ�������������Ҳ��������ɡ�Fe(OH)3���ȵ�Ũ��ǿ����Һ�У����������ܽ⣬����������(��NaFeO2��Na3��Fe(OH)6��)��Co(OH)3�����ǿ���������������ǻ�����(��)����(��K��Co(OH)6��)��
������Ϊ+3������������������ã����ֳ���ͬ�����ʡ�����Fe(OH)3������������кͷ�Ӧ��
Fe(OH)3 + 3HCl  FeCl3 + 3H2O
FeCl3 + 3H2O
��Co(OH)3���������ã��ܰ�Cl-����Ϊ������
2Co(OH)3 + 6HCl  2CoCl2 + Cl2��+ 6H2O
2CoCl2 + Cl2��+ 6H2O
Ni(OH)3�������Ը�ǿ��Ҳ�ܰ���������ΪCl2��
(2)�����ܡ���������
(2.1)��(��)����(��)����(��)����
(2.1.1)��������
��(��)����(��)����(��)���������������Ƶĵط����������ǵ������Ρ������κ��Ȼ��ﶼ������ˮ������Һ�нᾧ����ʱ����������ͬ��Ŀ�Ľᾧˮ��������
FeSO4·7 H2O Fe(NO3)2·6 H2O FeCl2·6 H2O
CoSO4·7 H2O Co(NO3)2·6 H2O CoCl2·6 H2O
NiSO4·7 H2O Ni(NO3)2·6 H2O NiCl2·6H2O
��Щ���������ɫ����Ϊ���ǵ�ˮ�����Ӷ�������ɫ���絭��ɫ��Fe(H2O)62+���ۺ�ɫ��Co(H2O)62+����ɫ��Ni(H2O)62+������Һ�нᾧ����ʱ��ˮ�������е�ˮ��Ϊ�ᾧˮ��ͬ����������������(��)�ζ�������ɫ����(��)�δ��ۺ�ɫ����(��)�δ���ɫ��
�����ܺ����������ζ�����������淋��������γɸ��Ρ������������(NH4)2SO4·FeSO4·6H2O���׳�Ħ���Σ��Ƿ�����ѧ��K2Cr2O7����KMnO4���Ļ�ԭ��֮һ�����е�Fe(��)�������ǿ���ȶ��ԡ�����������ˮ�Ͼ����ֳ��̷����ڿ������绯��ͬʱ��������Ϊ�ƺ�ɫ����(��)�ļ�ʽ�����Ρ�FeSO4������м��ϡH2SO4�����Ƶá������ڱ���ľ�ģ�������īˮ����ֹ����ȡ�NiSO4�ǹ�ҵ�ϵ������ԭ�ϡ�
(2.1.2)Fe2+��Co2+��Ni2+�Ļ�ԭ��
Fe2+��Co2+��Ni2+�Ļ�ԭ��Fe2+��Co2+��Ni2+��˳���������Fe(OH)2�ױ������е���������Fe(OH)3��FeSO4��Һͬ���ױ�������Fe2(SO4)3��Ϊ��ֹFeSO4��Һ���ʣ�ͨ������������
(2.1.3)�Ȼ��ܵĽᾧˮ����ɫ
�Ȼ�����������Ҫˮ������ǵ��ת���¶ȼ�������ɫ������
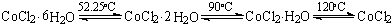
(�ۺ�) (�Ϻ�) (����) (��ɫ)
��ˮ���Ȼ���������ˮ�гʷۺ�ɫ����������õĹ轺�����ж��Ȼ��ܵ�ˮ��Һ�������Ȼ�������ˮ����ˮ����������ɫ�仯������ʾ�轺��ʪ������������¶�ʱ���轺ʧˮ�ɷۺ�ɫ��Ϊ����ɫ����ɫ�����轺��ˮ����Ϊ�ۺ�ɫ��
(2.1.4)��������
NiCl2��CoCl2����ͬ�ľ��Σ���NiCl2�����ѻ��ͪ�е��ܽ�ȱ�CoCl2С�ö࣬������һ���ʿ��Է����ܺ�����������Ϊ+2�������ܺ�����̼���κ����ﶼ��������ˮ�ġ��մ���Һ��������CoS��NiS������ϡ���У����ú�ת��Ϊ��һ�ֱ��壬�Ͳ�������ϡ���ˡ�
(2.2)��(��)����(��)����(��)����
(2.2.1)�ȶ���
��(��)����(��)���ζ��ܲ��ȶ����ʺ��١�������Ϊ���ǵ����������Բ�ͬ����ɵġ�
Fe3+ + e  Fe2+ Eq=0.771V
Fe2+ Eq=0.771V
Co3+ + e  Co2+ Eq=1.84V
Co2+ Eq=1.84V
Ni3+ + e  Ni2+ Eq>1.84V
Ni2+ Eq>1.84V
�����ǵ�Eqֵ���Կ�����������Ϊ+3�����ӵ�������Fe3+-Co3+-Ni3+��˳����ǿ����Fe3+��Co3+��Ni3+�ֱ��븺���ӽ��ʱ����ȡ�����ӵĵ��ӱ���ԭΪ+2�����ӵ�����Ҳ��Fe3+-Co3+-Ni3+��˳����ǿ������������Ϊ+3���ε�������ԭ�ȶ�������һ˳������͡��������ǵ���������֪��Fe2(SO4)3·9H2O��Co2 (SO4)3·18H2O��Fe2 (SO4)3·9H2O�Ǻ��ȶ������Σ���Co2 (SO4)3·18H2O��������Һ�в��ȶ����ڹ���״̬ʱҲ�ܲ��ȶ����ֽ����(��)�������κ������������룬��(��)�������θ����ȶ���������ΪNi3+�������Ը�ǿ��Ե�ʡ�
(2.2.2)FeCl3����������ˮ����
FeCl3����������Ӧ�����л��ϳɺͿ�ʴijЩ�������档���磬��ҵ�ϳ�Ӧ��FeCl3��������Һ�����Ʋ����Ͽ�ʴ��������ӦʽΪ��
2Fe3+ + Fe  3Fe2+
3Fe2+
��һ��Ӧ��ƽ�ⳣ�����ݹ�ʽ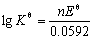 �������
�������
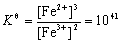
�ɼ��˷�Ӧ���ҽ��еij̶��Ǻܴ�ġ�ͬ����Fe2+����Һ�м�����������ɷ�ֹFe2+������ΪFe3+��
�����ߵ繤ҵ�ϣ�������FeCl3����Һ����ʴͭ������ӡˢ��·���䷴ӦʽΪ��
2Fe3+ + Cu  2Fe2+ + Cu2+ Kq = 1014.7
2Fe2+ + Cu2+ Kq = 1014.7
ͭ������Ҫȥ���IJ��֣���FeCl3��Һ�������£���ΪCu2+���ܽ����
����Fe3+��Fe2+�ĵ�ɶ࣬�뾶С�������ˮ��Һ��Fe3+��Fe2+��������⣬���ǵĵ�һ����ⳣ���ֱ�������
[Fe(H2O)6]3+ [Fe(OH)(H2O)5]2+ + H+ Kq= 10-3.05
[Fe(OH)(H2O)5]2+ + H+ Kq= 10-3.05
[Fe(H2O)6]2+ [Fe(OH)(H2O)5]+ + H+ Kq= 10-9.5
[Fe(OH)(H2O)5]+ + H+ Kq= 10-9.5
Fe3+�����Է���������ⷴӦ��
[Fe(OH)(H2O)5]2+  [Fe(OH)2(H2O)4]+ + H+ Kq= 10-3.26
[Fe(OH)2(H2O)4]+ + H+ Kq= 10-3.26
�ڽ�Ũ��Fe3+��Һ(1mol·L-1)�У�������γɵļ�ʽ���ӿ�����Ϊ��������(˫��������)
2[Fe(H2O)6]3+ [(H2O)4Fe(OH)2Fe(H2O)4]4+ + 2H+ + 2H2O Kq= 10-2.91
[(H2O)4Fe(OH)2Fe(H2O)4]4+ + 2H+ + 2H2O Kq= 10-2.91
��Fe3+��ϡ��Һ(10-4mol·L-1����)�У�����������Ҫ��[Fe(OH)(H2O)5]2+��[Fe(OH)2(H2O)4]+��ͨ����Fe3+��������д��Fe(OH)3ֻ��һ�ֽ��Ƶ�д����
����Fe3+ˮ��̶ȴ�[Fe(H2O)6]3+���ܴ��������Խ�ǿ����Һ�У�ϡ����Һ��������Һ��pH�����н�״������������˽�״��������FeO(OH)��ͨ��Ҳд��Fe(OH)3����ʹ��Һ�ʻ�ɫ���غ�ɫ��FeCl3�ľ�ˮ���ã���������Fe3+������FeO(OH)����ˮ������������������һ��۳�������ʹ���ǵ�ˮ���塣
���������棬FeCl3�ǹ��ۼ�ռ���ƵĻ����������������˫�۷���Fe2Cl6����ṹΪ��
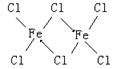
����������+3����ϵԪ�ص����࣬�Ѿ��Ƶõ��и������K2FeO4�������K3CoO4��������������Һ�ж��Ǻ�ǿ����������
(3)�����ܺ����������
(3.1)��±�������γɵ�������Լ�Fe3+���ڱ�
Fe2+��Co2+��Ni2+��ˮ��Һ����±�������γɵ�����ﶼ��̫�ȶ���������
Co(H2O)62+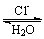 CoCl42-
CoCl42-
Fe3+��Co3+ȴ����F-�γ��ȶ���������K3��FeF6�ݺ�K3��CoF6�ݡ����Ƕ�������͵���������FeF63-�Ƚ��ȶ�(�ȶ�����ԼΪ1014)���ڷ�����ѧ�ϳ��ں���Fe3+�Ļ����Һ�У�����NaFʹFe3+�γ�FeF63-����Fe3+�ڱ��������Ӷ�����Fe3+�ĸ��š�
(3.2)��NH3�γɵ�������Լ�Co2+��Co3+���ȶ���
Fe2+��Co2+��Ni2+�백�γ��������ȶ���Fe2+-Co2+-Ni2+��˳����ǿ����Fe2+������ˮ��Һ���γ��ȶ��İ��������ˮ״̬��FeCl2����NH3�γ�[Fe(NH3)6]Cl2����ˮ����ʽ�ֽ���
[Fe(NH3)6]Cl2 + 6H2O  Fe(OH)2�� + 4NH3·H2O + 2NH4Cl
Fe(OH)2�� + 4NH3·H2O + 2NH4Cl
��Co2+��Ni2+��˵�����ַֽ������С���ڹ��������ڵ���Һ�У�Co2+����NH3�γɽ��ȶ���[Co(NH3)6]2+ (�ȶ�����Ϊ104.39)�����ױ�O2����Ϊ[Co(NH3)6]3+��Ni2+���γɣ�Ni(NH3)4��2+�ͣ�Ni(NH3)6��2+(ǰ���ȶ�����Ϊ107.47�������ȶ�����Ϊ108.01)����Ӧ������
CoCl2 + 6NH3 [Co(NH3)6]2+(����ɫ) + 2Cl-
[Co(NH3)6]2+(����ɫ) + 2Cl-
NiCl2 + 6NH3(����) [Ni(NH3)6]2+(��ɫ) + 2Cl-
[Ni(NH3)6]2+(��ɫ) + 2Cl-
Co3+������ﶼ����λ��Ϊ6�ġ�Co3+��ˮ��Һ�в����ȶ����ڣ���������λ��ֱ���γ�����ͨ����Co(��)����������ϼ�����Һ�У�����������Co(��)�������Ӷ��Ƴ�
Co(��)������������
4Co2+ + 24NH3 + O2 + 2H2O 4[Co(NH3)6]3+ + 4OH-
4[Co(NH3)6]3+ + 4OH-
����ɫ
������
[Co(NH3)6]2+ + H2O2 + 2H+  [Co(NH3)6]3+ + 2H2O
[Co(NH3)6]3+ + 2H2O
����ɫ ����ɫ
4CoCl2 + 4NH4Cl + 20NH3 + O2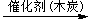 4[Co(NH3)6]Cl3 + 2H2O
4[Co(NH3)6]Cl3 + 2H2O
Co3+�γ�����������Һ�������ȶ��ġ�Ni(��)�������Ƚ��ټ������Dz��ȶ��ġ�
��Fe3+��˵��������ˮ�����ӷ���ǿ�ҵ�ˮ�⣬������ˮ��Һ�м��백ʱ�������γɰ���������γ�Fe(OH)3������
(3.3)��NCS-�γɵ�������Լ�Fe3+��Co2+�ļ���
Fe2+��Cu2+��Ni2+��NCS-�γɵ����������λ��4��6���ࡣ��������ˮ��Һ�ж���̫�ȶ�����ˮ��Һ�в�̫�ȶ�����ɫ������[Co(NCS)4]2-�ܽ��ȶ��ش��������ѡ��촼���ͪ�С��ڼ���Co2+ʱ��������һ���ԡ�Fe3+��NCS-�γ����Ϊ[Fe(NCS)n]3-n(n��1��2��3��4��5��6)�ĺ�ɫ�����ӽ��1��NCS-��[Fe(NCS)(H2O)5]2+�����6��NCS-��[Fe(NCS)6]3-���ʺ�ɫ����һ��Ӧ�dz����������Ǽ���Fe3+�Ƿ���ڵ���Ҫ��Ӧ֮һ��
����Co3+��Fe3+�ļ�����Ӧ�ֱ�Ϊ��
Co2+ + 4NCS-(����)  Co(NCS)42-
Co(NCS)42-
��ɫ
Fe3+ + 6NCS- Fe(NCS)63-
Fe(NCS)63-
Ѫ��ɫ
(3.4)��CN-�γɵ�������Լ�Fe3+��Fe2+��Ni2+�Լ�S2-��SO32-�ļ���
CN-��Fe3+��Fe2+��Co2+��Ni2+�����γ���λ��Ϊ6��4��������Щ����ﶼ���ڹ�����������Һ�ж����ȶ���
��ɫ����K4[Fe(CN)6]·3H2O����ҵ���ƽл�Ѫ�Ρ�Fe3+������KCNֱ������K3[Fe(CN)6]����������������K4[Fe(CN)6]����Һ���Ƶ���
6K4[Fe(CN)6]+ Cl2 2KCl + 2K3[Fe(CN)6]
2KCl + 2K3[Fe(CN)6]
K3[Fe(CN)6]�Ǻֺ�ɫ���壬��ҵ���ƽг�Ѫ�Ρ�[Fe(CN)6]3-�������Բ���Fe3+ǿ����Eqֵ������
[Fe(CN)6]3- + e  [Fe(CN)6]4- Eq=0.36V
[Fe(CN)6]4- Eq=0.36V
Fe3+ + e  Fe2+ Eq=0.77V
Fe2+ Eq=0.77V
[Fe(CN)6]3-��[Fe(CN)6]4-����Һ��ʮ���ȶ�������ں���[Fe(CN)6]3-��[Fe(CN)6]4-����Һ�м�����鲻������Fe3+��Fe2+����[Fe(CN)6]4-����Fe3+����������ɫ���������ֳ����׳���³ʿ�����䷴ӦʽΪ��
4 Fe3+ + 3[Fe(CN)6]4-  Fe4[Fe(CN)6]3��
Fe4[Fe(CN)6]3��
��һ��ӦҲ�Ǽ����Һ���Ƿ����Fe3+��������Ӧ��
[Fe(CN)6]3-��Fe2+����Һ��Ҳ������ɫ���������ֳ����׳����������䷴ӦʽΪ��
3 Fe2+ + 2[Fe(CN)6]3- Fe3[Fe(CN)6]2��
Fe3[Fe(CN)6]2��
��һ��ӦҲ�Ǽ����Һ���Ƿ����Fe2+��������Ӧ��
�������Ѿ���������³ʿ�����������Ľṹ����Fe4��[Fe��(CN)6]3��
Fe3+��[Fe(CN)6]3-����Һ�в����ɳ���������Һ��ɰ���ɫ��Fe2+��[Fe(CN)6]4-���������ɰ�ɫ��Fe2[Fe(CN)6]����������Fe2+�ױ������������������Ҳ�γ���³ʿ����
������������У��������������ֻ�����CN-���ӣ������ٽ��һ���������(��NO2-��SO32-)�����Է���(NO��CO��NH3��H2O)�����бȽ���Ҫ����Na2[Fe(CN)5NOS]������S2-(������HS-)��������Na2[Fe(CN)5NOS]��������ĺ���ɫ������ZnSO4��K4[Fe(CN)6]�Ļ��Һ������SO32-�����ɺ�ɫ����������������������Һ���Ƿ���S2-��SO32-�Ĵ��ڡ�
Ni2+��ƽ����������������[Ni(CN)4]2-��ж�����뿺���(��)������Ϊ�ʺ�ɫ�����������ڶ��Լ���Ni2+��
9.3 ds��Ԫ��
ds��Ԫ��(ds��Block��Elements)����ͭ��Ԫ�ص�ͭ(Copper)����(Silver)����(Gold)��п��Ԫ�ص�п(Zinc)����(Cadmium)����(Mercury)��������Ԫ��ԭ�ӵļ۵��Ӳ㹹�ͷֱ�Ϊ(n-1)d10ns1��(n-1)d10ns2��
9.3.1 ͨ��
ͭ���п��Ԫ�صĴ���㶼��18���ӽṹ�����Ե����Ƿֱ��γ���������ͬ���������Ļ�����ʱ����Ӧ�����Ӷ���18���ӹ��ͣ���������������Ӷ���ǿ�ļ����������ʹ���ǵĶ�Ԫ������һ�㶼���ֵػ���ȫ�ش��й����ԡ�
������Ԫ������������Ԫ�����ƣ����γ����������ڢ�B��Ԫ�ص�����M2+d��������������Ӳ��ܷ���d-dԾǨ��������ǵ������һ����ɫ��
9.3.2 ͭ��Ԫ��
(1)���ʼ��仯ѧ������
��Ϊ������˵�������еĽ����У����ĵ�������á�ͭ��֮������ڵ����й㷺����ͭ��Ϊ������ϣ�Ҫ��ߵij��ϣ��紥�㡢�缫�ȿɲ����������⣬ͭ����֮���Լ�����п�������ٵ���������֮��������γɺϽ���ͭ�Ͻ��еĻ�ͭ����п������ͭ������������ͭ���������ȡ�
ͭ��������Ļ�ѧ�����Խϲ�����¿�����������������ˮ���ã����ǣ�����Ӧ�ܲ����������ʻ������ӣ��������O2������Ӧ�������ں���CO2�ij�ʪ�����У�ͭ�ı������������ɫ��ͭ��(�׳�ͭ��)������ʽ̼��ͭCu2(OH)2CO3��
2Cu + O2 + H2O + CO2 Cu2(OH)2CO3
Cu2(OH)2CO3
��������H2S�Ļ����У�
4Ag + O2 + 2H2S  2AgS(��ɫ) + 2H2O
2AgS(��ɫ) + 2H2O
(2)ͭ��Ԫ�صĻ�����
ͭ��Ԫ��+1�����������Ӷ�����ɫ�ģ���������̬���������ڴ����δ��������������ɫ��(Cu2+��ɫ��Au3+���ɫ)��
(2.1)�ܽ����������
Cu+Ϊ18���ӹ��ͣ����н�ǿ�ļ���������˼�������Cu(��)�Ļ����ﶼ������ˮ����Cu(��)�Ļ�������������ˮ�Ľ϶ࡣ
ˮ��ͭ����[Cu(H2O)6]2+����ɫ����Cu2+����Һ�м��������ļ����dz��ɫ������ͭCu(OH)2����������Cu(OH)2����Һ���ӽ�����ʱ�ֽ��CuO��
Cu2+ + 2OH�� Cu(OH)2��
Cu(OH)2��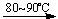 CuO��+ H2O
CuO��+ H2O
��һ��Ӧ��������ȡCuO��
Cu(OH)2�����ڹ���Ũ����Һ�У��������ǻ���ͭ(��)����[Cu(OH)4]2-��
Cu(OH)2 + 2OH- Cu(OH)42-
Cu(OH)42-
����������ﶼ��������ˮ�ġ�±�������ܽ�Ȱ�AgCl-AgBr-AgI˳���С��Ag+ͬ���н�ǿ�ļ������ã������ʴ�Cl-��I-�����������Ӽ����۵���������ļ�������������ǿ����Ϊ���ۼ�ռ���Ƶ�AgI���Ӷ�ʹ������ˮ�е��ܽ����С��Ag+Ϊd10���ͣ����Ļ�����һ��ʰ�ɫ����ɫ����AgBr�ʵ���ɫ��AgI�ʻ�ɫ������±�ظ����Ӻ�Ag+֮�䷢���ĵ��Ǩ���йء�������ˮ��Ag(��)������������������AgClO4��������AgF����������AgBF4��������AgNO3�ȡ�����Ag(��)��һ�㻯����(����������)��������������ˮ�ġ�
(2.2)�ȶ����������
һ��˵�����ڹ�̬ʱ��Cu(��)�Ļ������Cu(��)�Ļ��������ȶ��Ըߡ����磬Cu2O���ȵ�1800��ʱ�ֽ⣬��CuO��1100��ʱ�ֽ�ΪCu2O��O2����ˮCuCl2ǿ��ʱ�ֽ�ΪCuCl����ˮ��Һ��Cu(��)���ױ�����ΪCu(��)����ˮ��Һ��Cu(��)�Ļ��������ȶ��ġ�
���Ļ����������˵�����ȶ���Ag(��)�����������ȵ���̫�ߵ��¶�ʱ�ͻᷢ���ֽ⣬������
2Ag2O 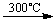 4Ag + O2��
4Ag + O2��
2AgCN 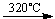 2Ag + (CN)2��
2Ag + (CN)2��
2 AgNO3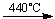 2 Ag + NO2��+ O2��
2 Ag + NO2��+ O2��
����Ag(��)������Թ������еġ�����AgCl��AgBr��AgI���ⶼ����ʽ�ֽ���
AgX 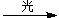 Ag + 1/2X2
Ag + 1/2X2
X����Cl��Br��I�����ҵ�ϳ���AgBr���������Ƭ��ӡ��ֽ�ȡ�
(2.3)������Ϊ���͵����������
(2.3.1)Cu2O����������
����O2���ڣ��ʵ�����Cu2O�����ɺ�ɫ��CuO����������Cu2O����һ��������ȥ��������������
2Cu2O + O2 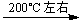 4CuO
4CuO
����ɫ��ĩ״��Cu2O������������ԭCuO�õ���
2CuO + H2 Cu2O + H2O��
Cu2O + H2O��
��CuOֻҪ����Cu(OH)2���ʽ̼��ͭCu2(OH)2CO3���ܻ����
Cu2(OH)2CO3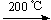 2CuO + CO2 �� + H2O��
2CuO + CO2 �� + H2O��
(2.3.2)��ˮCuSO4����ˮ��
��ˮCuSO4����ˮ����ˮ�����ɫ��������������Һ̬�л����е���ˮ��
(2.3.3)AgNO3��������
AgNO3Ϊһ��ǿ���������ɱ��л��ﻹԭΪ��ɫ��Ag��Ҳ�ɱ�Zn��Cu�Ƚ�����ԭΪAg��
2 AgNO3��Cu ==2Ag����Cu(NO3)2
���⣬AgNO3��ʹ���������̳ɺ�ɫ�ĵ��������ʶ�Ƥ���и�ʴ���á�10����ϡAgNO3��Һ��ҽҩ�Ͽ���Ϊɱ������
(2.3.4)Cu2+�ļ���
�ڽ�������Һ�У�Cu2+��[Fe(CN)6]4-��Ӧ������Cu2[Fe(CN)6]����ɫ������
2Cu2+ + [Fe(CN)6]4�� Cu2[Fe(CN)6]��
Cu2[Fe(CN)6]��
��һ��Ӧ������������Cu2+�Ĵ��ڡ�
��(2)ͭ(��)��ͭ(��)֮����ת��
��ͭ�ĵ���ͼ������Eq (Cu+��Cu)��Eq (Cu2+��Cu+)��
Cu2+ 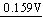 Cu+
Cu+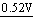 Cu
Cu
����Cu+����Һ�����Զ��绯ΪCu2+��Cu��
2Cu+ = Cu2+ + Cu Kq = 106.12
������ƽ�ⳣ��ֵ��֪��������Cu+��ˮ��Һ���绯��Ӧ�ij̶Ƚϴ�Cu+��ˮ��Һ�в��ȶ�����Cu+�γ����������ܽ��ȶ��ش�������Һ�С�����[CuCl2]-�Ͳ������绯ΪCu2+��Cu������Ӧ�ĵ���������
Cu2+ 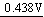 CuCl2-
CuCl2-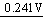 Cu
Cu
Eq( CuCl2-/Cu)��Eq(Cu2+/CuCl2-)������[CuCl2]-����Һ���ǽ��ȶ��ġ�������
Cu2+ + Cu + 2Cl- �� 2CuCl����ɫ
��Cl-������ CuCl(s) + Cl-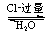 [CuCl2]-�����ɫ��
[CuCl2]-�����ɫ��
���� Cu2+ + Cu + 4Cl-(Ũ) �� 2 [CuCl2]-
������CuSO4��CuCl2����Һ��ŨHCl��Cuм��ϣ��ڼ��ȵ�����£�����ȡ[CuCl2]-����Һ��
CuSO4 + 4HCl + Cu  2H[CuCl2] + H2SO4
2H[CuCl2] + H2SO4
���Ƶõ���Һ���������ˮ��ϡ��ʱ�����а�ɫ�Ȼ���ͭCuCl����������
[CuCl2]- CuCl(s) + Cl��
CuCl(s) + Cl��
��ҵ�ϻ�ʵ�����г������ְ취�������Ȼ���ͭ��
������ĵ���ͼ������CuClҲ�������绯ΪCu2+��Cu��
Cu2+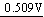 CuCl
CuCl 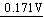 Cu
Cu
CuCl��ˮ�пɱ������е�������������ΪCu(��)���Ρ�����״̬��CuCl��Ƚ��ȶ���
��ˣ���Ҫʹ��Һ�е�Cu(��)ת��ΪCu(��)���ȶ����ڣ�������Ҫ��ԭ����ͬʱҪʹCu+�γ��ѽ�������ʣ�������Һ��Cu+��Ũ�ȡ�
(3)ͭ��Ԫ�ص������
(3.1)Cu(��)�������
Cu+�����������ӻ���Ӷ����γ��ȶ����������ȶ��Խ�����˳����ǿ��
Cl-��Br-��I-��SCN-��NH3��S2O32-��CS(NH2)2��CN-
���������ᵽCuCl�ڹ�����Cl-��Һ���γɵ����ɫ��[CuCl2]-������[CuCl2]-��Һ�м�ˮϡ��ʱ�ֻ����CuCl��ɫ������
Cu(��)������ﳣ�������������������ͬ�����ӵ�����������(����)������Һ�н�ӺϷ�Ӧ���γɡ����磬CuCN����NaCN��Һ���������ܵ�Na[Cu(CN)2]���䷴ӦʽΪ��
CuCN(s) + CN- [Cu(CN)2]-
[Cu(CN)2]-
���෴Ӧ�ܷ���У�ȡ���������ε��ܶȻ����������ȶ������Ĵ�С�����������ε�Ũ���йء���CuCN����[Cu(CN)2]-�ķ�Ӧ����ƽ�ⳣ����ʾʽΪ��

�ɼ���Ӧ���ҽ��еij̶Ƚϴ���Cu(��)��������У�Cu(��)����λ����������2������λ���Ũ������ʱ��Ҳ���γ���λ��Ϊ3��4��������[Cu(CN)3]2-(��3��1028.59)��[Cu(CN)4]3-(��4��1030.30)��
(3.2)Cu(��)�������
��Cu2+��������У�[CuCl4]2-�ȶ��Խϲ�(��4��10-4.6)���ں�Ũ��Cl����Һ���л�ɫ��[CuCl4]2-���ڡ�����ˮϡ��ʱ��[CuCl4]2-�������Ϊ[Cu(H2O)6]2+��Cl-����Һ����ɫ�ɻƱ���(��[CuCl4]2-��[Cu(H2O)6]2+�Ļ��ɫ)������Ϊ��ɫ��[Cu(H2O)6]2+��
��Cu2+�ļ�������У�����ɫ��[Cu(NH3)4]2+���ȶ�������ƽ�������ε������ӣ�����[Cu(NH3)4]2+����ɫ������Cu2+�Ĵ��ڡ�
���ڷ����������У����ʵ�����λ��ʱ��Cu��ʱ�ܴӴ���Һ���û�������������Cu������������CS(NH2)2���������û���������
2Cu + 2HCl + 4CS(NH2)2 2[Cu(CS(NH2)2)2]+ + H2��+ 2Cl��
2[Cu(CS(NH2)2)2]+ + H2��+ 2Cl��
����������������Cu+���ɶ������ͭ(��)����[Cu(CS(NH2)2)2]+��ʹCu��ǿ��ʧȥ���ӵ��������ڿ������ڵ�����£�Cu��Ag��Au���������軯�ػ��軯�Ƶ���Һ����
4M + O2 +2H2O + 8CN- 4[M(CN)2]- + 4OH-
4[M(CN)2]- + 4OH-
M����Cu��Ag��Au����������Ҳ���������ǵ���������CN-�γ�����ʹ���ǵ��ʵĻ�ԭ����ǿ�����¿����е����ܰ�����������������Ӧ�����ڴӿ�ʯ����ȡAg��Au��
�ںϳɰ������в�����ͭ�����Ż�ܵ���������Ϊ�����·�Ӧ��
2Cu + 8NH3 + 2H2O + O2 2[Cu(NH3)4]2+ + 4OH-
2[Cu(NH3)4]2+ + 4OH-
����ͭ���Ա���ʴ��Ҳ�������ϵ�������ΪCu2+��NH3���γ�����ʹͭ���ʵĻ�ԭ����ǿ�������ܰ�ͭ������
(3.3)Ag(��)�������
ˮ��������һ����Ϊ��[Ag(H2O)4]+������ˮ�м�����ˮ�⣬AgNO3��ˮ��Һ�����Է�Ӧ����Ag+��Һ�м���NaOH��Һ��������Ag2O��������ΪAgOH�����ȶ���
2Ag+ + 2OH- Ag2O��+ H2O
Ag2O��+ H2O
�ӵ��Ag+/Ag��Eq��0.799V������Ag+�������Բ�����������Ag+��Һ�м���I-ʱ��Ag+ȴ���ܰ�I-����ΪI2�����Ƿ������з�Ӧ��
Ag+ + I- AgI��
AgI��
��������Ag+��I-����AgI������������Һ��Ag+��Ũ�ȣ�ʹAg+��Ag�ĵ缫���ƴ�ͣ�����Ag+����I-�ķ�Ӧ���ܷ�����ͬ���أ���Ag+��Һ��ͨ��H2S��Ҳ���ᷢ��������ԭ��Ӧ����������Ag2S������
AgI���ڹ�����KI��Һ�У�������AgI2-��������
AgI(s) + I- AgI2-
AgI2-
����ˮϡ��AgI2-��Һʱ��AgI�������������ӷ�Ӧ��ƽ�ⳣ����ʾʽKq��[AgI2-]/[I-]����������Һϡ��ʱ��[I-]��[AgI2-]ͬʱ���٣��ұ�ֵ���䣬�ƺ�ƽ�ⲻ�������ƶ�������Ӧ��AgI����������AgI����Һ�л�����������ƽ����
AgI  Ag+ + I-
Ag+ + I-
�ܵķ�ӦΪ��
AgI2- AgI + I-
AgI + I-  Ag+ + 2I-
Ag+ + 2I-
��ƽ�ⳣ����ʾʽΪ��
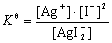
�ɴ˿��Կ���������Һϡ��ʱ�����Ӻͷ�ĸ������Ũ�ȵı�ֵQ��С����Q��Kq�����Ի�ʹƽ��������I-��Ag+�ķ����ƶ�����ϡ�͵�һ���̶ȣ���������Ag+��I-Ũ�ȳ˻��������AgI��Ũ�Ȼ����ͻ���AgI����������
��ˮ��Һ�У�Ag+���������λ���γ���������λ��һ����2������Ag+��������ﶼ��������ˮ�ģ���Ag+��Һ�м�����λ��ʱ���������������ܻ��������λ������ʱ�������ܻ����ォ�γ������Ӷ��ܽ⡣���磬��Ag+����Һ�м��백ˮ����������������ˮ��Ag2O������
2Ag+ + 2NH3 + H2O Ag2O��+ 2NH4+
Ag2O��+ 2NH4+
��Һ�а�ˮŨ������ʱ��Ag2O���ܽⲢ����[Ag(NH3)2]+��
Ag2O(s)��+ 4NH3 + H2O  2[Ag(NH3)2]+ + 2OH��
2[Ag(NH3)2]+ + 2OH��
����[Ag(NH3)2]+����Һ�ܰ�ȩ��ijЩ������������������ԭΪAg��������
2[Ag(NH3)2]+ + HCHO + 3OH- HCOO- + 2Ag��+ 4NH3 + 2H2O
HCOO- + 2Ag��+ 4NH3 + 2H2O
��ҵ���������෴Ӧ���ƾ��ӻ���ůˮƿ�ļв��϶�����
����Ag+��S2O32-�����Ȳ���Ag2S2O3������Ѹ�ٷֽ⣬��ɫ�ɰ�ɫ����ɫ����ɫ�����ɺ�ɫ��Ag2S������S2O32-��������Ӧ���ղ��������ӣ�
2Ag+ ��S2O32- �� [Ag(S2O3)2]3-
[Ag(S2O3)2]3-Ҳ�dz���������һ�����������Ƭ��δ�ع���廯���ڶ�ӰҺ(S2O32-)���γ�[Ag(S2O3)2]3-���ܽ���
AgBr + 2S2O32- [Ag(S2O3)2]3- + Br-
[Ag(S2O3)2]3- + Br-
Ag(��)������������ˮ�Ļ��������ת��Ϊ�����Ӷ��ܽ⣬��������һ���ԣ���Ag+�ӻ��������Һ�з�������������ں���Ag+��Ba2+����Һ�У������������K2CrO4��Һʱ������Ag2CrO4��BaCrO4�����������ټ��������İ�ˮ��Ag2CrO4ת��Ϊ[Ag(NH3)2]+���ܽ���
Ag2CrO4(s) + 4NH3 2[Ag(NH3)2]+ + CrO42-
2[Ag(NH3)2]+ + CrO42-
BaCrO4�����ڰ�ˮ��������ʹ��ϵ�Ba2+��Ag+���롣
������ˮAg2S���ܽ��̫С�����Խ���λ��Ӧʹ���ܽ⣬ͨ��������������ԭ��Ӧʹ���ܽ⡣���磬��HNO3������Ag2S���������·�Ӧ��
3 Ag2S(s) + 8 H+ + 2NO3�� 6Ag+ + 2NO�� + 3S�� + 4H2O
6Ag+ + 2NO�� + 3S�� + 4H2O
�Ӷ�ʹAg2S�ܽ⡣CuSͬ��Ҳ�ɽ�˷����ܽ⡣
9.3.3 п��Ԫ��
п(Zn)����(Cd)����(Hg)ͨ��������Ϊп��Ԫ�ء���������p��Ԫ�����ڵ�d��Ԫ�أ�������d��Ԫ�����Ƶ����ʣ��������γ������ȡ���ijЩ���������������4��5��6���ڵ�p������Ԫ����Щ���ƣ����۵㶼�ϵͣ�ˮ�����Ӷ���ɫ�ȡ�
Zn��Cd��Hg��ԭ�ӵļ۲����Ϊ(n-1)d10ns2�͡�п���ӵĻ������빯�Ļ�������������֮ͬ�������磬�������γ�������Ϊ+2�Ļ������⣬����������Ϊ+1(Hg22+����)�Ļ������п�����ڻ�������ͨ��������Ϊ+2��
(1)����
п�ڱ����������ڿ���������һ�����ܵļ�ʽ̼����ZnCO3·Zn(OH)2��ʹп�п�����ʴ�����ʣ����Գ���п���Ʊ����塣�Ӽ��ʹ�����ʴ���ֶԼ�ͺ�ˮ�нϺõĿ���ʴ�ԣ������õ���չ�ԣ�Ҳ���ں��ӣ����ܳ��ñ��ֽ���������ˣ��㷺Ӧ���ڷɻ��ʹ�������ķ����Ʋ㡣����������Ψһ��Һ̬���������лӷ��ԺͶ������ã�Ӧ�ر�С�ġ�
п���ӡ���֮����������������γɺϽ����繯���ܽ�����γɹ��룬�繯���ƵĺϽ��ƹ��룩��ˮ�Ӵ�ʱ�����еĹ��Ա�������ԣ���������ˮ��Ӧ�ų�����������ͬ���Ľ�����ȣ���Ӧ���еıȽ�ƽ�ȡ����ݴ����ʣ��ƹ������л��ϳ��г�������ԭ����
�������������ʻ�ѧ���ʷ��棬п���Ӷ��Ƚ���������������⡣п�DZȽϻ��õĽ������ӵĻ�ѧ�����Բ���п�����Ļ�ѧ���ʲ����á���ֵ��һ����ǹ�����ۺ������γ������ݴ����ʣ����������乯�ĵط�������ۣ�ʹ��ת���������������������Ķ��ԡ�
(2)п��Ԫ�صĻ�����
(2.1)�������������������������ȶ���
п�����γ�������Ϊ2�Ļ����������������Ϊ+2��+1�Ļ������������Ϊ+1�Ĺ��Ļ������У�����Hg22+ (��Hg��Hg��)��ʽ���ڡ�Hg(��)�Ļ�������ǹ��������������ǹ����������ﶼ��������ˮ�ġ�Hg(��)�Ļ�������������ˮ��Ҳ�϶࣬������ˮ�Ĺ������ﶼ���ж��ġ��ڹ��Ļ������У����������Թ��ۼ���ϵġ�
ZnO��Zn(OH)2�����������ʣ�Cd(OH)2Ϊ����ƫ���ԡ���Zn2+��Cd2+��Һ�м���ǿ��ʱ���ֱ����ɰ�ɫ��Zn(OH)2��Cd(OH)2�������������ʱ��Zn(OH)2�ܽ�����Zn(OH)42-����Cd(OH)2�����ܽ���
Zn2+ + 2OH-  Zn(OH)2��
Zn(OH)2�� [Zn(OH)4]2-
[Zn(OH)4]2-
Cd2+ + 2OH-  Cd(OH)2��
Cd(OH)2��
��Hg2+��Hg22+����Һ�м���ǿ��ʱ���ֱ����ɻ�ɫ��HgO���غ�ɫ��Hg2O��������ΪHg(OH)2��Hg2(OH)2�����ȶ�������ʱ������ˮΪ��������
Hg2+��2OH- HgO����H2O
HgO����H2O
Hg22+��2OH- HgO����Hg����H2O
HgO����Hg����H2O
HgO��Hg2O����������Ũ�����У��������ڼ���Һ�С�
(2.2)HgCl2���Ʊ����ṹ�����백ˮ������
HgCl2����HgSO4��NaCl������������Ƶ���
HgSO4 + 2NaCl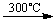 Na2SO4 + HgCl2 (g)
Na2SO4 + HgCl2 (g)
��ʱ�Ƴ�����HgCl2���壬��ȴ���ΪHgCl2���塣����HgCl2���������ʳ�������HgCl2Ҳ����Hg��Cl2ֱ�����ö��Ƶ���
Hg + Cl2 HgCl2
HgCl2
HgCl2�о綾�����Թ��ۼ���ϵķ��ӣ�Hg��sp�ӻ������Cl��ϣ��ռ乹��Ϊֱ������
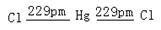
Hg(��)��±����(HgF2����)�Լ�Hg(CN) 2��Hg(SCN) 2���ǹ����ͷ��ӣ�Ϊֱ���ι��ͣ������HgCl2һ����
HgCl2��ˮ��Һ����Ҫ�Է�����ʽ���ڡ���HgCl2��Һ�м��백ˮ�����ɰ����Ȼ���(NH2HgCl)��ɫ������
HgCl2 + 2NH3 NH2HgCl��+ NH4Cl
NH2HgCl��+ NH4Cl
ֻ���ں��й�����NH4Cl�İ�ˮ��HgCl2������NH3�γ��������
HgCl2 + 2NH3 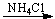 [Hg(NH3)2Cl2]
[Hg(NH3)2Cl2]
(2.3)�ǹ��ε��绯����˹���Լ���NH4+�ļ���
����������ˮ���ǹ��μ�������������绯��Hg(��)�Ļ�����͵��ʹ�(Hg2Cl2����)�����磬��Hg22+��Һ�м���I-ʱ�������������ܵĻ���ɫ��Hg2I2��
Hg22+��2 I- Hg2I2��
Hg2I2��
Hg2I2���������绯Ϊ���ɫ��HgI2�ͺ�ɫ�ĵ��ʹ���
Hg2 I2(s) HgI2��Hg
HgI2��Hg
HgI2�����ڹ�����KI��Һ�У��γ�[HgI4]2-��
HgI2��2I�� [HgI4]2-
[HgI4]2-
HgI42-����������˹��(Nessler)�Լ����������Լ��ڼ�����Һ��������NH4+��
(2.4)���������ε�ˮ������Hg2+�������Լ�Hg2+�ļ���
���ṯHg(NO3)2�������ǹ�Hg2(NO3)2������ˮ��Hg(NO3)2����HgO��Hg��HNO3������ȡ��
HgO + 2HNO3 Hg(NO3)2 + H2O
Hg(NO3)2 + H2O
Hg + 4HNO3(Ũ) Hg(NO3)2 + 2NO2 + 2H2O
Hg(NO3)2 + 2NO2 + 2H2O
Hg(NO3)2��Hg���ÿ���ȡHg2(NO3)2��
Hg(NO3)2 + Hg Hg2(NO3)2
Hg2(NO3)2
Hg(NO3)2��Hg2(NO3)2�������ͻ����
��Hg(NO3)2��Hg2(NO3)2��������Һ�У��ֱ�����ɫ��Hg(H2O)62+��Hg2(H2O)x2+���ڡ�������ˮ�а���ʽ����ˮ�ⷴӦ��
[Hg(H2O)6]2+ [Hg(OH)(H2O)5]+ + H+ Kq��10-3.7
[Hg(OH)(H2O)5]+ + H+ Kq��10-3.7
[Hg2(H2O)x]2+ [Hg2(OH)(H2O)x-1]+ + H+ Kq��10-5.0
[Hg2(OH)(H2O)x-1]+ + H+ Kq��10-5.0
������Һ�����ԣ������������ǵ�ˮ�⡣
��Hg2+����Һ�м���SnCl2�������а�ɫ��Hg2Cl2���ɡ��ټ��������SnCl2��ҺʱHg2Cl2�ɱ�Sn2+��ԭΪHg���˷�Ӧ������������Һ��Hg2+�Ĵ��ڡ�
(2.5)���PCd2+�ļ���
��Zn2+��Cd2+����Һ�зֱ�ͨ��H2Sʱ���������������Һ�г���������
Zn2+ + H2S  ZnS��+ 2H+
ZnS��+ 2H+
Cd2+ + H2S  CdS��+ 2H+
CdS��+ 2H+
����ZnS���ܶȻ��ϴ�����Һ��H+Ũ�ȳ���0.3mol·L-1ʱ��ZnS�����ܽ⡣CdS��������ϡ���С�����Һ��������CdS������ɫ����������һ��Ӧ��������Һ��Cd2+�Ĵ��ڡ�
CdS����Ũ����ķ�Ӧ������
CdS + 2H+ + 4Cl- [CdCl4]2- + H2S
[CdCl4]2- + H2S
ʵ����CdS��6mol·L-1�������о��ܱ��ܽ⡣
��ZnSO4����Һ�м���BaSʱ����ZnS��BaSO4�Ļ�ϳ�����˳�����п����(�׳����·�)��
Zn2+ + SO42- + Ba2+ + S2- ZnS·BaSO4��
ZnS·BaSO4��
п������һ�ֽϺõİ�ɫ���ϣ�û�ж��ԣ��ڿ����бȽ��ȶ���
HgS���ܶȻ���С�������п������������ۡ�
(3)Hg(��)��Hg(��)���ת��
�ɵ���ͼ�ɿ�����Hg22+����Һ�в������绯ΪHg2+��Hg��
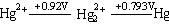
�෴��Hg�ܰ�Hg2+��ԭΪHg22+��
Hg2+ + Hg  Hg22+ Kq��142
Hg22+ Kq��142
ǰ���ᵽ��Hg2(NO3)2����ȡ�����Ǹ�����һ��Ӧ�����еģ����൱��Hg22+�����绯��Ӧ��
�෴�ģ���ҪʹHg22+ת��ΪHg(��)��ʹ֮�ȶ����ڣ��͵�ʹHg2+�γ��ѽ�������ʣ�����Hg2+��Ũ�ȡ�����Hg2Cl2��NH3�ķ�Ӧ��
Hg2Cl2 + 2NH3 NH2Hg2Cl + NH4Cl
NH2Hg2Cl + NH4Cl
NH2Hg2Cl NH2HgCl + NH4Cl + Hg
NH2HgCl + NH4Cl + Hg
����Hg2Cl2 + 2NH3 NH2HgCl�� + Hg�� + NH4Cl
NH2HgCl�� + Hg�� + NH4Cl
Hg2Cl2�ֳƸʹ���Ҳ��һ��ֱ���ͷ��ӣ����������ֽ⡣
���磺Hg22+��S2- == HgS���� Hg��
Hg22+��CO32- == HgO���� Hg����CO2��
(4)п��Ԫ�ص������
(4.1)Zn(��)��Cd(��)�������
��Ũ��ZnCl2ˮ��Һ�У����γ���������
ZnCl2·H2O == H[ZnCl2(OH)]
���������������������ԣ����ܽ������������磺
FeO��2H[ZnCl2(OH)] == Fe[ZnCl2(OH)]2��H2O
���ӽ���ʱ������ZnCl2��Ϊ��ҩ��������������������㣬ʹ���Ӳ������γɼٺ���
пһ�����γ���λ��Ϊ4������������
Zn2+ + 4NH3(����) [Zn(NH3)4]2+
[Zn(NH3)4]2+
�������⣬Zn(OH)2�ڹ���OH-�����µ��ܽ⡢CdS��Ũ�����е��ܽ�Ҳ�����γ�����Ӧ������
(4.2)Hg(��)�������
Hg2+���γɶ�����������λ��Ϊ4��ռ���Զ��������Ƿ����Եġ���������ﳣ��ӺϷ�Ӧ���ɡ����磬������ˮ�İ�ɫHg(SCN)2������Ũ��KSCN��Һ�У����ɿ����Ե�������Ϲ�(��)���K2[Hg(SCN)4]��
Hg(SCN)2 (s) + 2SCN�� [Hg(SCN)4]2-
[Hg(SCN)4]2-
������ǰ���ᵽ������λ�ܽ⡣
����Һ��Hg2+��Cl-����������ƽ����
Hg2+ 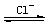 [HgCl]+
[HgCl]+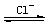 [HgCl2]
[HgCl2]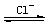 [ HgCl3]-
[ HgCl3]- 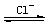 [HgCl4]2-
[HgCl4]2-
������λ��Ũ�ȵIJ�ͬ���γ�һϵ���м��͵�����ʵ��֤�����ڴ��ڹ���Cl-������£���Ҫ���γ�HgCl42-����Cl-Ũ�Ƚ�С����Һ�У�HgCl2��HgCl3-��HgCl42-���ܶ����ڡ�����ɿ�����HgCl2�ɿ�������Ϸ��ӣ�������Һ�в�����ȫ���ΪHg2+��Cl-�������Է�����ʽ���ڵ�HgCl2ռ�������ơ�
HgS������ˮ���������ڹ�����Ũ��Na2S��Һ�����ɶ���Ϲ�(��)����[HgS2]2-��
HgS(s) + S2�� [HgS2]2-
[HgS2]2-
��ʵ������ͨ������ˮ�ܽ�HgS��
3HgS(s) +12Cl- + 8H+ + 2NO3- 3[HgCl4]2- + 3S��+2NO��+ 4H2O
3[HgCl4]2- + 3S��+2NO��+ 4H2O
��һ��Ӧ������HNO3�ܰ�HgS�е�S2-����ΪS�⣬����������[HgCl4]2-Ҳ�Ǵ�ʹHgS�ܽ������֮һ���ɼ���HgS�ܽ��ǽ�������ԭ��Ӧ����λ��Ӧ��ͬ���õĽ����
9.4�ơ�þ���ơ�п�����Ƚ���Ԫ��������������
��ʳ���Ƶ���Ҫ��ԴΪʳ�κͽ��͡��Ʋ�����Һ�����ƽ�⣬����Cl-��HCO3-���ӽ�ϣ�����pH��ά��ϸ����Һһ������ѹ��ʹ֮��ϸ����Һ����ѹƽ�⣬���ͼ�����һ���Թ��������˷����á������������ʱ�������ܼ�����ÿ���ų����������٣�ʹ�������ڴ�����������ˮ���࣬ѪҺ�е������Ӻ�ˮ������ѹ�ĸı䣬���뵽��֯��϶�ж��γ�ˮ�ף���ʹѪѹ���ߣ�������������˥�ߡ���ˣ����ಡ���ڸ����ڼ�Ҫ�ϸ���Ρ�
þ���Ƕ�ֲ������Ӫ��Ԫ�ء�������70����þ�����ڹ����У������30������������֯����Һ�С�þ�����ǹ��ɹ��������ݵ�ԭ�ϣ��������ڻ��������ơ��ء��ƹ�ͬά�����ࡢ������ȵ��������ܡ�þ��Ҷ���ص���ɲ��֣�����������Ĵ�л������������Ҫ�����á��о�֤����ֲ��Ľ�ʵ��������Ҫ�϶��þ��þ�Ĵ��ڶԸƵ����������й�ϵ��ȱþʱ������Ӱ��ƵĴ�л���á�þȱ����֢״�Ǿ�����������������������ѣ�Σ��������Է������ʡ���þ�ḻ��ʳƷ��С�ס�������С���ࡢ����Ͷ���ĸ���ȡ�
���ǹ���ֲ��ϸ���ںͶ����������Ҫ�ɷ֣������ڸƵ�99�������ڹ����������У�������Ҫ�ֲ�����Һ�ڣ�����ijЩ��Ҫ��ø��Ӧ����ά�������������������������˷��ԣ��ٽ���Ѫ�ͱ���ϸ��������������Ҫ���á�ȱ�ٸ�ʱ��������ֲ�������������������ԸƵ������ʵͣ�����������ƿ��γɿ����Ը��Σ���˸ߵ�����ʳ�����ڸƵ����ա�ά����D�����Ƕ��ܴٽ��Ƶ����ա�
����ȱ�Ƶ���Ҫ֢״�������������������ɣ������ֲ���������̬�벽���������ڳ�Ѫ�����������������϶̡���ͯ���Ƶ�;����Ҫ�гԸ�Ƭ������ͣ��Ը��ʱ��ɵȡ���Ϊ��Ҫ���Ƕ�ɹ̫�����Դٽ�ά����D�ĺϳɣ����ƸƵ��������á�
��������ĸƣ����̼�����Ʒ��ã����������ḻ�����������ʸߡ����⣬���ơ����ࡢ�������߲˺���Ҳ�ϸߣ�СϺ��Ƥ�����ر�ḻ��������Ҳ���иơ�
п�������к�����2��3g����Ҫ�����ڹ�����Ƥ��(����ͷ��)�С�п�����ø�����ἰ�����ʵĺϳ��������еĹ�ϵ������Ӱ��ϸ���ķ��ѡ�������������п����ζ�ʺ�ʳ����ֱ��Ӱ�죬ȱп�ɽ���ζ���������Ժ�ʹζ��������쳣����������ʳ�����ˣ�ֱ��Ӱ���������ͯ�����������������Ѱ�ʳ���½���ΪӤ��ȱп�����ڱ��֡��ٴ���Ҳ֤����ȱп��С����ʳ�IJ���֮һ��
����ȱп���ٴ�����������ͣ�ͣ��䵽�˳���Σ�ȴ���İ�С���Է���������ζ����ʳ�����˺ʹ������ϲ����ȡ�
��п�϶���Ƕ��ﵰ�ף����㡢��(����������)���Ρ�����ˮ������ĵ�õȡ�һ����˵��������ʳ���е�п���������ߣ��һ��Դ������ա���Ӥ����˵�������е�п��ţ���е�п�����գ������Ȼţ�̺�п���������̣���п������ȴ�������̺á�
���������ں���Լ3��5g������70����ѪҺѭ���ڡ����뵰���ʽ�ϳ�Ѫ���ء���Ϊ��ϸ����Ҫ�ɷ֣�����ȱ����Ѫ���ؾ����γɣ����ƶѪ��Ѫ���ؿ�Я��������Ӫ����������ѭ����������ϸ��֮��Ҫ��Ȼ��ϸ������֮������̼������������й���٣��ų����⡣��Ϊ����ϸ������֮��Ҫ���ʡ���Ϊ����ø�صijɷ֣���ɻø�ص��������ܡ�ֲ�����ڵ������γ�Ҷ���صı�Ҫ�����������������������Ԫ��֮һ��
��ʳ������������ԴΪ������ࡢ���ơ������ijЩ�߲ˣ��Լ��ں��ǡ����ѡ��ҡ�÷��ʳ���С�һ��˵����������ʳ���е�����ֲ����ʳ���е���������Щ��
ϰ ����
9-1 ��ͬ��Ԫ����ȣ�ﮡ�������Щ������?
9-2 �������ְ�ɫ�����ĩ�����ǿ��ֱܷ�����MgCO3��BaCO3����ˮNa2CO3����ˮCaCl2����ˮNa2SO4�����跨���Լ��𣬲�д����Ӧʽ��
9-3 ��ǿ���Ժ�ǿ���Խ����У���(��)��(��)���Ժ������Ӵ���?�ʺ���ɫ?
9-4 ��K2Cr2O7�ı�����Һ�м���ŨH2SO4�������ȵ�200��ʱ��������Һ����ɫ��Ϊ����ɫ������鷴Ӧ��ʼʱ��Һ�в����κλ�ԭ�����ڣ���˵�������仯��ԭ��
9-5�����չ���Cr2O3��ΪCr(��)��Cr(��)�Ļ��������ʲô�취?д���䷴Ӧ����ʽ��
9-6 ��1.0L0.1mol·L-1Cr3+��Һ�У�Cr(OH)3��ȫ����ʱ������Һ��pHֵ�Ƕ���?Ҫʹ��������Cr(OH)3�պ���1.0LNaOH��Һ����ȫ�ܽⲢ���ɣ�Cr(OH)4��-������Һ��OH-����Ũ���Ƕ���?�����Cr(OH)4��-���ȶ�������4��
��֪�� Cr(OH)3(s) + OH- Cr(OH) 4- Kq��10-0.4��
Cr(OH) 4- Kq��10-0.4��
9-7 ��MnCl2��Һ�м���������HNO3���ټ���NaBiO3����Һ�г����Ϻ�ɫ������ʧ��˵��ԭ��д���йط�Ӧ����ʽ��
9-8���ݼۼ����ۣ���������������γ�ʱ�������ӵļ۲���ӷֲ������������������ȶ���
��Mn(C2O4)3��3- ��Mn(CN)6��3-
��/B·M 4.9 2.8
9-9 ������������ڲ�ͬ�����еĻ�ԭ����Ӧ�ȼӻ�ԭ�������ȼӽ���?Ϊʲô?
9-10 ��Fe2+��Co2+��Ni2+����Һ�м�NaOH������CO2�Ŀ����з��ú��õ����ֲ���?
9-11 �����ᴦ��Fe(OH)3��Co(OH)3��Ni(OH)3������ʲô��Ӧ?д����Ӧ����ʽ���ⷴӳ������ʲô�����ϵIJ���?
9-12 ��0.1mol·L-1��Fe3+��Һ�м����㹻��ͭм�������·�Ӧ�ﵽƽ�⣬��Fe3+��Fe2+��Cu2+��Ũ�ȡ�
9-13 ��0.1mol·L-1Fe3+��Һ�У�������ˮ������Fe(OH)(H2O)5��2+�γɣ������Һ��pHֵ?(��֪Kq1��10-3.05)
9-14 ��Һ�к���Fe3+��Co2+��Ni2+����ΰ����Ƿֱ����?
9-15 д�������йط�Ӧʽ����˵����Ӧ����
��ZnCl2��Һ�м���NaOH��Һ���ټӹ�����NaOH��Һ��
��CuSO4��Һ�Ӱ�ˮ���ټӹ�����ˮ��
��HgCl2��Һ�м�������SnCl2��Һ���ټӹ�����SnCl2��Һ��
��HgCl2��Һ�м�������KI���ټӹ�����KI��Һ��
9-16 �ں��д���NaF��1mol·L-1CuSO4��1mol·L-1��Fe2(SO4)3�Ļ����Һ�У�����1mol·L-1KI��Һ������ʲô������?д���йط�Ӧʽ��
9-17 ������з�Ӧ����ʽ��
(1) Cu2+ + Cu + Cl��
(2) [Ag(NH3)2]+ + HCHO
(3) Ag2S + HNO3(Ũ)
(4) Hg(NO3)2 + NaOH
(5) Hg22+ + H2S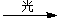
(6) Hg2+ + I��(����)
(7) Cd2+ + HCO3��
(8) HgS +HCl+ HNO3
9-18 ��H2Sͨ��ZnCl2��Һ�У�������������ZnS����������ڴ���Һ�м���NaAc����ʹZnS������ȫ����˵��ԭ��
9-19 ��һ�����Һ����Ag+��Cu2+��Zn2+��Hg2+�������ӣ���ΰ����Ƿ��뿪�����������ǵĴ���?
9-20 ��Hg2Cl2��HgCl2��Һ�У��ֱ���백ˮ��������ʲô����?д����Ӧʽ��
9-21 ��Cu2+��Ag+��Ca2+��Hg22+��Hg2+����Һ�У��ֱ����������NaOH��Һ���ʸ���ʲô��������?д���йص����ӷ�Ӧ����ʽ��
9-22 �ɴ�п�Ƴ���Zn(NO3)2�У����ܺ���Cd2+��Fe3+��Pb2+�����ӣ�����ʲô����֤���������������ӵĴ��ڡ�
9-23 ��֪��ӦZn(OH)2+2OH- Zn(OH)42-��ƽ�ⳣ��Kq��100.68������й����ݣ�����Eq (Zn(OH) 42-/Zn)��ֵ��
Zn(OH)42-��ƽ�ⳣ��Kq��100.68������й����ݣ�����Eq (Zn(OH) 42-/Zn)��ֵ��
9-24 �������е�Ե�Eqֵ������йص�Ե�Eqֵ������[AuCl2]-��[AuCl4]-���ȶ�������
[AuCl2]-+e  Au+2Cl- Eq��1.61V
Au+2Cl- Eq��1.61V
[AuCl4]-+ 2e  [AuCl2]-+ 2Cl- Eq��0.93V
[AuCl2]-+ 2Cl- Eq��0.93V
9-25 ���㷴ӦCu2++Cu+4Br- 2[CuBr2]-��ƽ�ⳣ����
2[CuBr2]-��ƽ�ⳣ����
9-26 ��֪���з�Ӧ�������µ�ƽ�ⳣ����
Cu(OH)2(s)+2OH- [Cu(OH)4]2- Kq��10-2.78
[Cu(OH)4]2- Kq��10-2.78
����й����ݣ���[Cu(OH)4]2-���ȶ�������4����1.0LNaOH��Һ�У���ʹ0.10molCu(OH)2�ܽ⣬��NaOH��Ũ������ӦΪ����?
9-27 ��Ag+��Һ�У��ȼ���������Cr2O72-���ټ���������Cl-���������㹻����S2O32-������ÿһ������ʲô�������?д���йص����ӷ�Ӧ����ʽ��
9-28 ijһ������A����ˮ��һdz��ɫ��Һ����A��Һ����NaOH����ɫ����B��B������HCl��Һ��Ҳ�����ڰ�ˮ��A��Һ��ͨ��H2S���к�ɫ����C���ɡ�C������HCl��Һ����������ŨHNO3�С���A��Һ�м���Ba(NO3)2��Һ������������������AgNO3��Һʱ�а�ɫ����D���ɡ�D���ڰ�ˮ�����ж�A��B��C��DΪ����?
9-29 ��һ��ɫ��Һ���ټ��백ˮʱ�а�ɫ�������ɣ���������ϡ�����л�ɫ�������ɣ������μ�KI��Һ���������ۺ�ɫ��������KI����ʱ���ۺ�ɫ������ʧ�������ڴ���ɫ��Һ�м������ι�����������ʧ����ʱ�ټӰ�ˮ�ûҺ�ɫ�������ʴ���ɫ��Һ�к������ֻ�����?д���йط�Ӧʽ��
