华南农业大学实验报告
专业班次 11农学一班 组别* *
题目 苯甲酸的提纯和测定
姓 名 **
日期
【实验目的】
1、 了解固体有机物的分离和提纯方法;
2、 掌握回流,重结晶,测熔点的操作。
【实验原理】
重结晶:固体物质在溶剂中的溶解度随温度升高而增大,如果把固体物质溶解在热的溶剂中制成饱和或接近饱和的溶液,然后冷却至室温或室温以下,则溶解度下降,溶液过饱和,这时就会有晶体析出;
熔点测定原理:熔点是晶体物质的固相和液相在正常大气压下成平衡的温度,纯净的固态有机化合物都有固定的熔点,而且一般不高,用简单的一起就可以测定,有机化合物的熔点通常用毛细管发测定,纯净的有机化合物固液两相之间的变化非常敏锐,熔点范围很少,当含有杂质的时候,会使熔点变小,并且熔点范围增大。
【实验步骤】
1、 将粗苯甲酸用热水进行重结晶,烘干产品得到纯苯甲酸,
2、 测定产率,
3、 测定苯甲酸的熔点: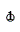 去一直径为1-2mm,长度7-8cm的毛细管,将其一端放在火焰上烧融,使之封闭,将少许的苯甲酸放在洁净的表面皿上,用玻璃棒研成粉末并束成一堆,然后将熔点管的开口端插入到试样中,装取试样后,将端口向上,把熔点管竖起来,在台面上轻顿几下,再取30~40cm的干燥玻璃管,垂直于台面上,让熔点管自由下落,重复几次,使试样落到管的底部,并且结实均匀,
去一直径为1-2mm,长度7-8cm的毛细管,将其一端放在火焰上烧融,使之封闭,将少许的苯甲酸放在洁净的表面皿上,用玻璃棒研成粉末并束成一堆,然后将熔点管的开口端插入到试样中,装取试样后,将端口向上,把熔点管竖起来,在台面上轻顿几下,再取30~40cm的干燥玻璃管,垂直于台面上,让熔点管自由下落,重复几次,使试样落到管的底部,并且结实均匀,
4、 加热,每分钟升温5到6摄氏度,熔点前二十摄氏度前减为每分钟0.3到0.5摄氏度,当试样开始出现塌落,湿润出现小液滴,表示开始融化,记录温度,完全融化后再记录一次温度。
【实验数据记录】
苯甲酸粗产品的质量为1.56-0.7=0.86g,纯产量为0.62,产率为75.6%
熔点测定
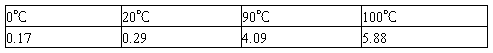

【讨论】
第二篇:苯甲酸的制备实验
苯甲酸的制备实验
一、实验原理
氧化反应是制备羧酸的常用方法。芳香族羧酸通常用氧化含有α- H 的芳香烃的方法来制备。芳香烃的苯环比较稳定,难于氧化,而环上的支链不论长短,在强裂氧化时,最终都氧化成羧基。
制备羧酸采用的都是比较强烈的氧化条件,而氧化反应一般都是放热反应,所以控制反应在一定的温度下进行是非常重要的。如果反应失控,不但要破坏产物,使产率降低,有时还有发生爆炸的危险。
主反应:
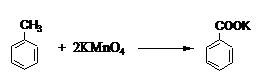

二、反应试剂、产物、副产物的物理常数
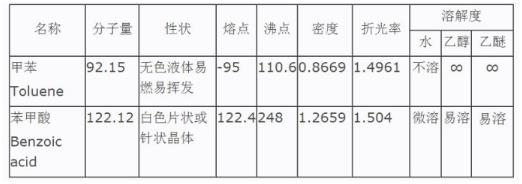
三、药品
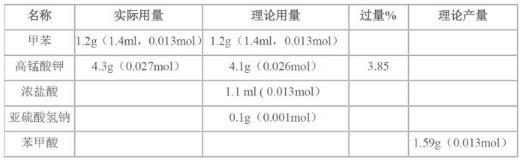
四、实验装置图

图1 电动搅拌器
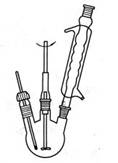
图2 回流搅拌装置
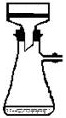
图3 抽滤装置
五、实验流程图

六、实验内容
在安装有电动搅拌器、回流冷凝管的250ml三口圆底烧瓶中放入1.4ml甲苯和70ml水,加热至沸。从冷凝管上口分批加入 4.3g高锰酸钾;粘附在冷凝管内壁的高锰酸钾最后用25ml水冲洗入瓶内。继续煮沸并间歇摇动烧瓶,直到甲苯层几乎近于消失、回流液不再出现油珠(约需4-5h)。
将反应混合物趁热减压过滤,用少量热水洗涤滤渣(MnO2)。合并滤液和洗涤液,于冰水浴中冷却,然后用浓盐酸酸化(刚果红试纸检验),至苯甲酸析出完全。将析出的苯甲酸减压过滤,用少量冷水洗涤,挤压去水分。把制得的苯甲酸放在沸水浴上干燥。产量:约1.0g。若要得到纯净产品,可在水中进行重结晶。
纯净的苯甲酸为白色片状或针状晶体。熔点mp=122.4℃。
(一)制备过程
1.安装制备装置:如图(1)(2),首先放置好电动搅拌器,然后由下往上安装各个仪器,即将控温电热套平放在桌面上,接着固定250ml三口圆底烧瓶(瓶底不能接触电热套),安装搅拌棒(要保证搅拌棒转动时不能接触瓶底)、并将搅拌棒与电动搅拌器电机连接固定、调节(用手转动搅拌棒观察有无摩擦现象,若有摩擦,需调整消除),一侧口连接回流冷凝管(万用夹夹在冷凝管的中部;冷凝管的上口应该是敞口的,不能用塞子),另一侧口安装温度计(水银球要插到液面以下)。
2.加药品:从连有温度计的侧口,依次加入1.4ml甲苯、70ml水和4.3g高锰酸钾(或加药品顺序为4.3g高锰酸钾、100ml水和1.4ml甲苯)(一次性加入高锰酸钾即可)。
3.加热:先打开电动搅拌器电源开关,慢慢旋转调速旋钮使电动搅拌器的搅拌棒逐渐转起来,由小变大,正常搅拌的时候,再开始加热,直至微微沸腾。控制加热速度,使蒸气体不超过冷凝管下面数第二个球部为宜,直到甲苯层几乎近于消失、回流液不再出现油珠(约1-2h)。
【注:因氧化反应是放热反应,故在制备反应的整个过程中,要保证电动搅拌器不能停止,否则可能会发生反应液喷出的现象。一旦出现故障需要调节搅拌器的话,必须先撤去电热套,同时用手转动搅拌棒进行搅拌才行。】
(二)后处理过程
1.加亚硫酸氢钠:因氧化剂高锰酸钾是过量的,反应完后反应液仍呈紫色,可从冷凝管上口分次加入少量饱和亚硫酸氢钠溶液,直到使反应液紫色褪去为止。(除去过量的高锰酸钾)
【注:操作仍在上面的搅拌装置中进行,这时可以停止加热,撤去电热套,但搅拌不能停。在搅拌的同时,慢慢地从冷凝管上口分批加入饱和亚硫酸氢钠溶液,以防止带入大量空气气体而引起爆沸、喷出反应液。饱和亚硫酸氢钠溶液浓度为40%】
【在本实验中,亚硫酸氢钠的最小用量为与过量的高锰酸钾的mol量相当,即0.001mol,为0.10g;最大用量为与4.3g(0.027mol)高锰酸钾的mol量相当,即2.81g,故亚硫酸氢钠的用量范围为0.10-2.81g。亚硫酸氢钠用量不要过量太多,否则在后面的酸化时会与盐酸作用产生太多的亚硫酸而再分解为二氧化硫气体。】
2.趁热减压过滤:拆卸装置,将三口瓶内的反应混合物趁热减压过滤,用少量热水洗涤滤渣(MnO2)。(除去二氧化锰)
3.酸化:将滤液和洗涤液合并倒入烧杯里,于冰水浴中冷却,然后在搅拌下,慢慢加入浓盐酸进行酸化(刚果红试纸检验变蓝或pH=3),至苯甲酸析出完全。
4.减压过滤:将析出的苯甲酸减压过滤,用少量冷水洗涤,挤压去水分。
【注:减压过滤前要将烧杯里的溶液进行充分的冷却。】
5.产品干燥:把制得的苯甲酸放在沸水浴上干燥。
【注:因苯甲酸在100℃左右开始升华,故应特别注意:电热套加热温度不可太高、烧杯里水量应稍多些、干燥时间长短等操作,避免干燥时局部温度过高造成苯甲酸升华而损失或熔化变成液态状。】
6.称重:产量约1.0g。
7.纯化:若要得到纯净产品,可在水中进行重结晶。
纯净的苯甲酸为白色片状或针状晶体。熔点mp=122.4℃。
七、思考题
1、在氧化反应中,影响苯甲酸产量的主要因素是哪些?
答:反应温度、甲苯与氧化剂之间的充分混合等是影响苯甲酸产量的主要因素。
2、反应完毕后,如果滤液呈紫色,为什么要加亚硫酸氢钠?
答:紫色是由过剩的高锰酸钾所致,加入亚硫酸氢钠可使高锰酸钾还原为二价的无色锰盐。否则,用盐酸酸化时会发生盐酸被高锰酸钾所氧化,产生氯气;同时产生的二氧化锰会混杂在析出的苯甲酸中,不易除去,影响苯甲酸的纯度。
3、精制苯甲酸还有什么方法?
答:苯甲酸在 100℃左右开始升华。故除了重结晶方法外,也可用升华方法精制苯甲酸。
4、苯甲酸的制备方法有哪些?
答:
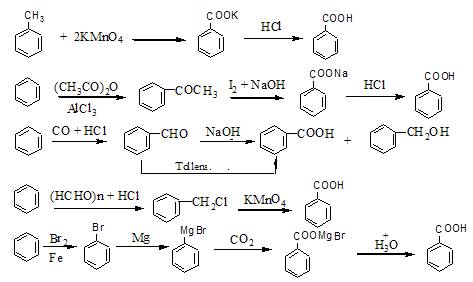
5、亚硫酸氢钠还可以用什么来代替?
答:还可以用草酸、甲醇来代替。
6、用高锰酸钾氧化甲苯制备苯甲酸时,如何判断反应的终点?
答:当反应回流液中无油珠出现时,说明不溶于水的甲苯已经被氧化完全,此时氧化反应即达到反应终点。
7、如果甲苯没有被全部氧化成苯甲酸,问残留在苯甲酸中的甲苯如何除去?
答:可将苯甲酸粗品溶解在5%NaOH水溶液中,用乙醚萃取除去甲苯,水层再用浓盐酸酸化,即析出苯甲酸,然后抽滤、干燥即可。
8、浓盐酸的摩尔浓度是多少?
答:浓盐酸的摩尔浓度是12M(浓硫酸为18M、浓硝酸为18M)
9、怎样安装有电动搅拌器的回流反应装置?
答:安装有电动搅拌器的反应装置,除按一般玻璃仪器的安装要求外,还要求:
(1)搅拌棒必须与桌面垂直。
(2)搅拌棒粗细与搅拌器套管的配合应松紧适当。
(3)搅拌器套管上口处套上一约1-2cm长乳胶管(要比搅拌棒略粗一点),胶管内涂抹一点凡士林(起润滑与密封作用)。
(4)搅拌棒距烧瓶底应保持0.5cm以上的距离。
(5)安装完成后应用手转动搅拌棒看是否有阻力;搅拌棒下端是否与烧瓶底、温度计等相碰。如相碰应调整好以后再接通电源,使搅拌正常转动。

回流搅拌装置

搅拌器套管
玻璃搅拌棒
10、学生实验中经常使用的冷凝管有哪些?各用在什么地方?
答:学生实验中经常使用的冷凝管有:直形冷凝管,球形冷凝管,空气冷凝管及刺形分馏柱等。直形冷凝管一般用于沸点低于140℃的液体有机化合物的沸点测定和蒸馏操作中;沸点大于140℃的有机化合物的蒸馏可用空气冷凝管。球形冷凝管一般用于回流反应即有机化合物的合成装置中(因其冷凝面积较大,冷凝效果较好);刺形分馏柱用于精馏操作中,即用于沸点差别不太大的液体混合物的分离操作中。
八、备注
(1)制备时加热温度不要太高,回流即可。
(2)由于甲苯不溶于高锰酸钾水溶液中,故该氧化反应为两相反应,反应需要较高温度和较长时间,所以反应采用了加热回流装置,同时采用机械搅拌。如果能在反应中再加入相转移催化剂则能够大大缩短氧化反应时间。
(3)氧化反应结束时,在继续搅拌下从球形冷凝管上口分批加入适量的亚硫酸氢钠水溶液以除去未反应的高锰酸钾氧化剂,然后再进行将反应混合物趁热减压过滤。
(4)停止反应时的操作是:先关闭电源,撤去电热套,继续搅拌3-5min,稍微冷却后,再停止搅拌,以防止爆沸、喷液。即在整个氧化反应过程中不要停止搅拌,防止爆沸、喷液。
