ʵ�����ƣ� ����к͵ζ�
ʱ�� ʵ�飨���飩���� ������ ָ����ʦ
һ��ʵ��Ŀ�ģ�����֪Ũ����Һ������Һ������ʵ������Ϊ����Һ���ⶨδ֪��Һ������
��Һ�� Ũ�ȡ���ʵ����������Ϊ������Һ��
����ʵ�������� ��ʽ�ζ��ܡ���ʽ�ζ��ܡ���ƿ������̨�����ζ��ܼУ���
ʵ��ҩƷ�� 0.1000mol/L���ᣨ����Һ����δ֪Ũ�ȵ�NaOH��Һ��������Һ�������ָ
ʾ������̪����ɫ��Χ8~10�������ȣ�3.1~4.4��
����ʵ��ԭ���� c���꣩×V���꣩ = c������×V�����������跴Ӧ������֮��Ϊ1��1��
����ʵ�����Ϊ��c��H+��×V���ᣩ = c��OH-��×V�����
�ģ�ʵ����̣�
��һ���ζ�ǰ������
1����©�����ζ����Ƿ�©ˮ�����巽���� ��ʽ�ζ��ܣ����ζ��ܼ�ˮ���رջ�������ֹ����5
��in�������Ƿ���ˮ©������©�����ڻ�����ͿĨ��ʿ�֣�ע�ⲻҪͿ̫�࣬�����ס�����ڡ� ��ʽ�ζ��ܼ�©�����ǽ��ζ��ܼ�ˮ���رջ�������ֹ����5��in�������Ƿ���ˮ©���������©�����������Ƥ�ܡ���
2��ϴ�ӣ���������ˮϴ�ӵζ��ܣ����ô�װҺ��ϴ2~3�Ρ�
��ƿ������ˮϴ�����ɣ�������ϴ��Ҳ�����ɡ�
3����ȡ���ü�ʽ�ζ�������һ���������20.00ml����δ֪Ũ�ȵ�NaOH��Һ��ע�⣬������ʼ�̶�
��0����0�̶����£�ע����ƿ�С�
����ʽ�ζ�����ȡ��Һ���ᣬ�Ͼ����ݣ�����Һ�棬ʹҺ��ǡ����0�̶Ȼ�0�̶�����ijȷ�̶ȣ���¼����
V1������С�����ڶ�λ ��
���������
1������ƿ������ʽ�ζ��ܵ����棬�����еμ�1��2�η�̪������ɫ�����ԣ��ɽ���ƿ���ڰ״ɰ��ϻ��߰�ֽ�ϣ������ζ�������Һ��ε�����ƿ�У��ζ�ʱ�����ֲ�����ҡ��ƿ�����ֿ��Ƶζ��ܻ������۾�ע����ƿ����Һ��ɫ�ı仯��ֱ������һ���������Һ��Ϊ��ɫ�Ұ�����ڲ��ָ�ԭɫ����ʱ����������ǡ����ȫ�������кͣ��ﵽ�ζ��յ㡣��¼�ζ���Һ��̶�V2��
2������ƿ�ڵ���Һ�����Һ�ף�������ˮ����ƿϴ�ɾ��������������ظ�2~3�Ρ�
������ʵ���¼

���ģ�.ʵ�����ݼ�¼��
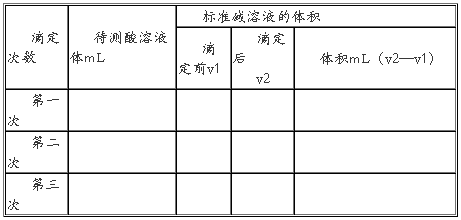
�塢ʵ����������c������=c���꣩×V���꣩/ V������
ע��ȡ����ƽ��ֵ��
����.ʵ��������Ľ����۸��ݣ�c��H+��×V���ᣩ = c��OH-��×V���������
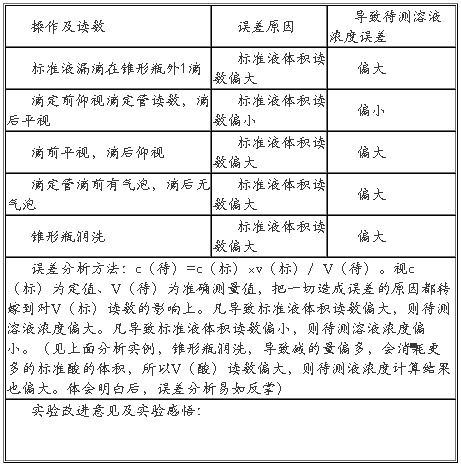
�ڶ�ƪ������к͵ζ�ʵ�鱨���Ͽ���
��NaOH��Һ�ζ�δ֪HCl��ʵ�鱨��
һ��ʵ��Ŀ�ģ� ��
����ʵ����Ʒ��
ʵ�������� ��
ʵ��ҩƷ�� ��
����ʵ��ԭ������1��Ҫʹ2L0.1mol/L��������ȫ��Ӧ������NaOH��Һ�����Ϊ4L�����NaOH��Һ�����ʵ���Ũ��Ϊ���٣�
�ġ�ʵ�鲽��
��һ���ζ�ǰ������1����ʶ���ζ��ܼ����ص㣺
��1���ṹ�ص㣺
��2����������
2���ζ�ǰ����
��1������©�� ��
��2����ϴ�ӣ� ��
3����ȡ������ʽ�ζ�������һ�������δ֪Ũ�ȵ�HCl��Һ��ע����ƿ�У�������ƿ�еμӼ��η�̪������Ϊ��Һ����ɫ���ü�ʽ�ζ�����ȡ��ҺNaOH��ʹҺ��ǡ����0�̶Ȼ�0�̶�����ijȷ�̶ȣ���¼����V1������С�����ڶ�λ��
���������
1���۲죺 �۾��� ������ ��
���֣� ��
2���������μ���Һ���������ߣ���ʼʱ�� �ɵΣ��ӽ��յ�ʱ��
�յ��жϣ�
��
2������ƿ�ڵ���Һ�����Һ�ף�������ˮ����ƿϴ�ɾ��������������ظ�3�Ρ�
���ۣ�1����ʶ���ָʾ����
2���ζ��յ��Ƿ�ΪPH=7��
��2������Σ�ԼΪ0.02ml��1mol/L��������뵽��ˮ��20mL�������Һ��PHΪ���٣�
���������ݴ���
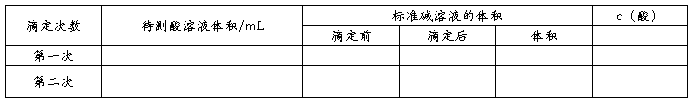
��
�������Һ�����ʵ���Ũ��
���ģ�������

���ò��飺
1���к͵ζ��У�����Ӧע��( )��
A. �ζ�����Һ��仯 B. Һ�εγ��ٶȪ�C. �ζ��̶ܿ� D. ��ƿ����Һ��ɫ�仯
2����25mL�ļ�ʽ�ζ�����ʢ����Һ��Һ��ǡ����20mL�̶ȴ����ֽ��ζ�������Һȫ���ų���������Ͳ�ڣ�������Һ�����Ϊ�� ��
A. 5mL B. 20mL C. ����5mL D. ��5mL
3. �ñ���ζ���ʱ���ζ�ǰ����ʽ�ζ��ܶ���ʱ�����ߵ���ˮƽ�ߣ��ζ�����ʱ������ȷ��������ʹ��õļ���Һ��Ũ�� ��
���¶Ե���ϰ��
֪ʶ��һ �ζ�ʵ�����������
1. �̶ȡ�0�����Ϸ������ڲ���Һ�������������( )��
A. �ζ��� B. ��Ͳ C. ��Һ�� D. ������
2. Ҫȷ��ȡ25.00 mLϡ���ᣬ���õ�������( )��
A. 25 mL��ʽ�ζ��� B. 25 mL��Ͳ�� C. 25 mL��ʽ�ζ���
3. �к͵ζ�ʱ��������ȡ����Һ�����������( )��
A. ��ͷ�ι� B. ��Ͳ�� C. �ζ��� D. ��Һ�ܪ�
4. �����к͵ζ�ʱ�����Ȳ�Ӧ������ʢ��Һϴ�ӵ�������( )��
A. ��ʽ�ζ��� B. ��ʽ�ζ��� C. ��ƿ D. ��Һ�ܪ�
5. ��25mL�ļ�ʽ�ζ�����ʢ����Һ��Һ��ǡ����20mL�̶ȴ����ֽ��ζ�������Һȫ���ų���������Ͳ�ڣ�������Һ�����Ϊ�� ��
A. 5mL B. 20mL C. ����5mL D. ��5mL
6. ȷ��ȡ25.00mL KMnO4��Һ����ѡ�õ������ǣ� ��
A. 50mL��Ͳ B. 10mL��Ͳ C. 50mL��ʽ�ζ��� D. 50mL��ʽ�ζ���
7. ���������У�û�С�0���̶��ߵ��ǣ� ��
A. �¶ȼ� B. ��Ͳ C. �ζ��� D. ����ƿ
8. �ñ�Ũ�ȵ�����������Һ���ζ�δ֪Ũ�ȵ����ᣬ�ڵζ�����ʱ�����ᣨ ��
A. ֻ��ʢ����ƿ�� B. ֻ��ʢ����ʽ�ζ�����
C. Ҳ���ü�ʽ�ζ���ȡ�� D. �ȿ�ʢ����ƿ�У�Ҳ��ʢ����ʽ�ζ�����w.w.w.k.s.5.u.c.o.m
֪ʶ��� ָʾ����ѡ��
1. �ñ�Ũ�ȵ��������ζ�δ֪Ũ�ȵ��������ƣ����ü���Ϊָʾ�����ζ��յ�ʱ����ɫ�仯Ӧ����
A. �ɻ�ɫ��ɺ�ɫ B. �ɻ�ɫ��Ϊ��ɫ C. �ɳ�ɫ��ɺ�ɫ D. �ɺ�ɫ��Ϊ��ɫ
2. �ñ�Ũ�ȵ�����������Һ���ζ�δ֪Ũ�ȵ����ᣬʹ�÷�̪��Ϊָʾ��������������˵��ǡ�ôﵽ�ζ��յ���ǣ� ��
A. �ɺ�ɫ��Ϊ���ɫ B. ����ɫ��Ϊ���ɫ
C. ��dz��ɫ������ɫ D. ����ɫ��Ϊdz��ɫ
3. �ñ�NaOH��Һ�ζ��������ᣬ���ü��ȴ����̪��ָʾ������ʱ����Ũ�ȵIJⶨֵ���̪��ָʾ���IJⶨֵ��Ƚ��ǣ� ��
A. ƫ�� B. ƫС C. ��Ӱ�� D. ���ж�
4. ����֪���ʵ���Ũ�ȵ�NaOH��Һ�ζ�δ֪���ʵ���Ũ�ȵ�HCl��Һ��һ��ѡ��_________��ָʾ��������֪���ʵ���Ũ�ȵ�HCl��Һ�ζ�δ֪���ʵ���Ũ�ȵ�NaOH��Һ��һ��ѡ��_________��ָʾ����
֪ʶ���� �к͵ζ���������
1. ����֪���ʵ���Ũ�ȵ�����ζ�δ֪���ʵ���Ũ�ȵ�����������Һ�����в����ᵼ�²ⶨ���ƫ�ߵ��ǣ� ��
A. �ñ���������Һ��ϴ��ʽ�ζ���2-3�� B. �ô����Һ��ϴ��ʽ�ζ���2-3��
C. �ô����Һ��ϴ��ƿ2-3�� D. ������ˮ��ϴ��ƿ2-3��
2. �ñ�������ζ�δ֪Ũ�ȵ�NaOH��Һ�����и������У���������ʵ�������ǣ� ��
A. ������ˮϴ����ʽ�ζ��ܺ�װ���������еζ�
B. ������ˮϴ����ƿ������NaOH��Һ��ϴ������װ��һ�������NaOH��Һ���еζ�
C. �ü�ʽ�ζ���ȡ10.00 mL NaOH��Һ����������ˮϴ������ƿ�У��ټ�����������ˮ���еζ�
D. ������Һ��ȡ10.00 mL��NaOH��Һ��������ƿ����Һ�ܼ���Һ�崵ȥ
3. ʵ�����ñ�������Һ�ⶨijNaOH��Һ��Ũ�ȣ��ü�����ָʾ�������в�������ʹ�ⶨ���ƫ�͵��ǣ� ��
A. ��ʽ�ζ�����װҺǰδ�ñ�������Һ��ϴ2�Ρ�3�Σ�
B. ��ʼʵ��ʱ����ʽ�ζ��ܼ��첿�������ݣ��ڵζ������У�������ʧ��
C. �ζ������У���ƿ����Һ��ɫ�仯�ɻ�ɫ���ɫ���������ֱ�Ϊ��ɫ����ʱ�����µζ���Һ����ʾ�Ŀ̶ȣ�
D. �ﵽ�ζ��յ�ʱ�����Ӷ����� E. ʢNaOH��Һ����ƿ�ζ�ǰ��NaOH��Һ��ϴ��
֪ʶ���� �к͵ζ������ݴ���
1. �����ȫ�к�ʱ�� ��w.w.w.k.s.5.u.c.o.m
A. ���������ʵ���һ�����
B. �������ṩ��H+�ͼ������ṩ��OH-�����ʵ������
C. ������������� D. ��Һ������
2. �к͵ζ��У���Ũ��ΪC mol·L��1��ij��Ԫ����Һ�к�Ħ������ΪM g·mol��1��һԪ��W g�������ֶ�Ԫ����Һ������ǣ� ��
A. 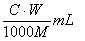 B.
B. 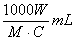 C.
C. 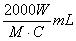 D.
D. 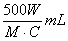
3. �к���ͬ�������ͬpH��Ba(OH)2��NaOH��NH3·H2O����ϡ��Һ��������ͬŨ�ȵ����������ֱ�ΪV1��V2��V3�������ߵĴ�С��ϵΪ�� ��
A. V3>V2>V1 B. V3>V2=V1 C. V3=V2>V1 D. V1=V2>V3��
4. ������Һһ���Ǽ��Ե���( )
A. ��Һ��c(OH��)��c(H��) B. �μӼ��Ⱥ���Һ�Ժ�ɫ
C. ��Һ�к���OH�� D. �μӼ��Ⱥ���Һ�Ի�ɫ
