实验4:配制100mL1.00 mol/L的NaCl溶液
班级: 姓名:
【实验目的】
1、练习配制一定物质的量浓度的溶液;
2、加深对物质的量浓度概念的理解;
3、练习容量瓶的使用方法
【实验仪器药品】
托盘天平、小烧杯、药匙、100ml容量瓶、胶头滴管、玻璃棒、量筒
【实验药品】
NaCl固体、蒸馏水
【实验步骤】
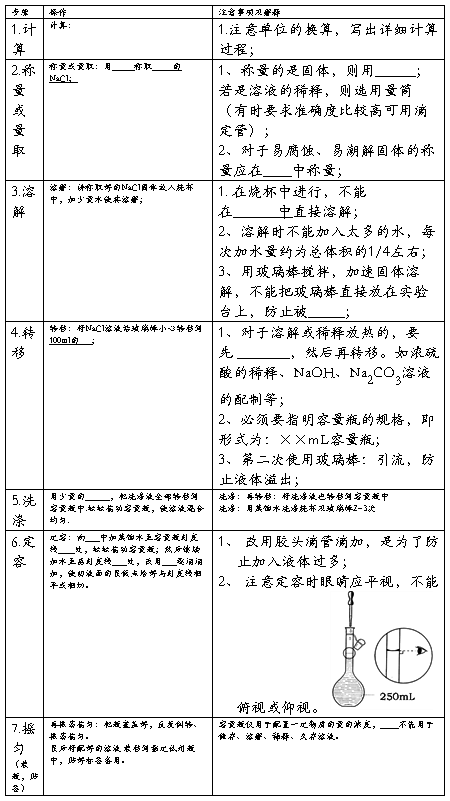
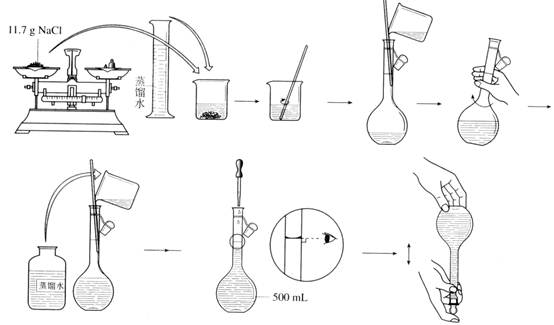
【交流与思考】
1、 容量瓶使用时应注意的事项:
2、 为什么要用蒸馏水来配置溶液而不能用自来水配置呢?
3、 为什么要洗涤玻璃棒和烧杯?如何洗涤?
4、 能否将溶解的NaCl溶液立即注入容量瓶中?为什么?
5、 为什么要将配好的溶液,从容量瓶里倒入试剂瓶?
6、 定容时不慎滴加液体超过刻度线,则该怎么做?
7、 下列实验操作会使所配制的溶液浓度偏高,偏低,还是不变?为什么?
①把溶液向容量瓶中转移,有少量溶液溅出;( ) 原因: ;
②未洗涤烧杯和玻璃棒;( ) 原因: ;
③定容时加水超过了刻线;( )原因: ;
④定容时仰视观察液面;( )原因: ;
⑤定容时俯视观察液面;( )原因: ;
⑥将溶液转移到容量瓶之前,容量瓶中有少量蒸馏水;( )原因: ;
⑦将配得的溶液从容量瓶转移到干燥、洁净的试剂瓶中时,有少量溅出;( )原因: ;
⑧定容时,俯视观察容量瓶刻度线;( )原因: ;
第二篇:一定溶质质量分数的氯化钠溶液的配制实验报告单
化学实验报告

