(六) 旋光法测定蔗糖转化反应的速率常数
一、目的要求
1、 测定蔗糖转化反应的速率常数和半衰期。
2、 了解该反应的反应物浓度与旋光度之间的关系。
3、 了解旋光仪的基本原理,掌握旋光仪的正确使用方法。
二、仪器与试剂
WZZ-2B自动旋光仪,样品管,秒表,恒温槽,量筒,锥形瓶,蔗糖水溶液,盐酸水溶液
三、实验原理
蔗糖在水中水解成葡萄糖与果糖的反应为
C12H22O11(蔗糖)+ H2O 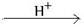 C6H12O6 (葡萄糖)+ C6H12O6(果糖)
C6H12O6 (葡萄糖)+ C6H12O6(果糖)
为使水解反应加速,反应常常以H+为催化剂。由于在较稀的蔗糖溶液中,水是大量的,反应达终点时,虽然有部分水分子参加了反应,但与溶质(蔗糖)浓度相比可以认为它的浓度没有改变。因此,在一定的酸度下,反应速度只与蔗糖的浓度有关,所以该反应可视为一级反应(动力学中称之为准一级反应)。该反应的速度方程为:-dC/dt = kC
其中C为蔗糖溶液的浓度,k为蔗糖在该条件下的水解反应速度常数
该反应的半衰期与k的关系为:t1/2 = ln2/k
蔗糖、葡萄糖、果糖都是旋光性的物质,即都能使透过它们的偏振光的振动面旋转一定的角度,称为旋光度,以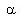 表示。其中蔗糖、葡萄糖能使偏振光的振动面按顺时针方向旋转,为右旋光性物质,旋光度为正值。而果糖能使偏振光的振动面按逆时针方向旋转,为左旋光性物质,旋光度为负值。
表示。其中蔗糖、葡萄糖能使偏振光的振动面按顺时针方向旋转,为右旋光性物质,旋光度为正值。而果糖能使偏振光的振动面按逆时针方向旋转,为左旋光性物质,旋光度为负值。
反应进程中,溶液的旋光度变化情况如下:
当反应开始时,t=0,溶液只有蔗糖的右旋,旋光度为正值,随着反应的进行,蔗糖溶液减少,葡萄糖和果糖浓度增大,由于果糖的左旋能力强于葡萄糖的右旋。整体来说,溶液的旋光度随着时间而减少。当反应进行完全时,蔗糖溶液为零,溶液中只有葡萄糖和果糖,这时,溶液的旋光度为负值。可见,反应过程中物质浓度的变化可以用旋光度来代替表示。
ln(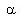 t-
t- ) = - k t +ln(
) = - k t +ln(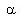 0-
0- )
)
从上式可见,以ln(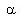 t-
t- )对 t作图,可得一直线,由直线斜率可求得速度常数k。
)对 t作图,可得一直线,由直线斜率可求得速度常数k。
四、实验步骤
1、从烘箱中取出锥形瓶。恒温槽调至55℃。
2、开启旋光仪,按下“光源”和“测量”。预热10分钟后,洗净样品管,然后在样品管中装人蒸馏水,测量蒸馏水的旋光度,之后清零。
3、量取蔗糖和盐酸溶液各30毫升至干净干燥的锥形瓶,盐酸倒入蔗糖中,摇匀,然后迅速用此溶液洗涮样品管3次,再装满样品管,放入旋光仪中,开始记时。将锥形瓶放入恒温槽中加热,待30分钟后取出,冷却至室温。
4、记时至2分钟时,按动“复测”,记录。如此,每隔2分钟测量一次,直至30分钟(注意:数值为正值时使用“+复测”,数值为负值时使用“-复测”)。
5、倒去样品管中的溶液,用加热过的溶液洗涮样品管3次,再装满样品管,测其旋光值,共测5次,求平均值。
五、实验数据记录

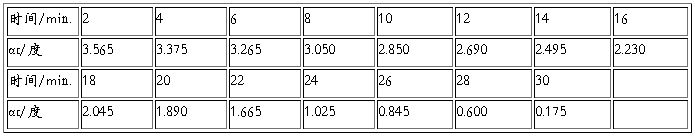
α∞= -0.570 、-0.590 、-0.590 、-0.605 、-0.610 。
α∞的平均值为 :-0.593
六、数据处理
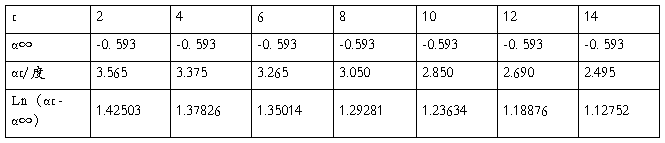
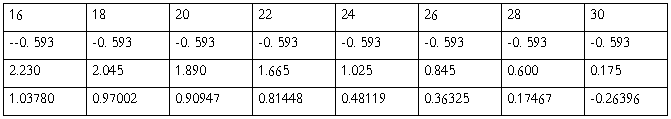
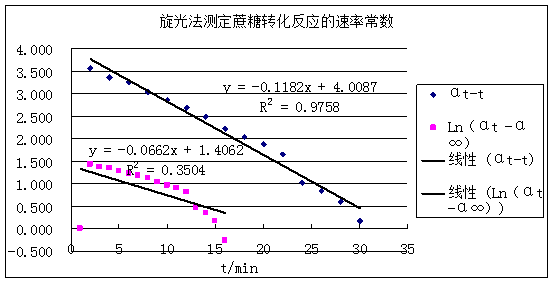
由Ln(αt -α∞)~t直线y = -0.0662x + 1.4062 可求得:
蔗糖的转化反应速率K=0.0662
半衰期:t =
= 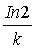 =
=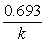 =10.47min
=10.47min
七、思考题
1.实验中,为什么用蒸馏水来校正旋光仪的零点? 在蔗糖转化反应过程中,所测的旋光度αt是否需要零点校正?为什么?
答:蒸馏水无旋光性,消除旋光仪的系统误差;实验中,所测的旋光度α t可以不校正零点,因αt-α∞ ,已将系统的零点误差消除掉。
2.蔗糖溶液为什么可粗略配制?
答:初始浓度对于数据影响不大。速率常数K与温度和催化剂的浓度有关,实验 测定反应速率常数k,以ln(αt-α∞)对t作图,由所得直线的斜率求出反应速 率常数k,与初始浓度无关
3.蔗糖的转化速度和哪些因素有关?
答:温度,催化剂得浓度、种类等。
4.溶液的旋光度与哪些因素有关?
答:溶液的旋光度与溶液中所含旋光物质的种类、浓度、溶剂的性质、液层厚度、 光源波长及温度等因素有关。
5. 反应开始时,为什么将盐酸溶液倒入蔗糖溶液中,而不是相反?
答:因为盐酸是作为催化剂。若把蔗糖倒入盐酸当中,会导致反应液中盐酸的浓度过大,使得蔗糖在还没检测的时候就反应完全,使实验存在很大误差。若那盐酸倒入蔗糖溶液中,可以避免这种事情发生,最大地降低了误差的出现。
八、 实验结果与讨论:
本实验测得蔗糖的转化反应速率K=0.0662 ,半衰期为10.47min,测得的旋光度变化趋势是从大到小,最终出现负值。证明果糖的旋光度为负值,并在数值上大于葡萄糖的旋光度值。而最终的旋光度几乎不变,这说明反应几乎已经达到极限。
通过该实验,了解该反应的反应物浓度与旋光度之间的关系,同时明白旋光仪的基本原理,掌握旋光仪的正确使用方法。
第二篇:旋光法测定蔗糖转化反应的速率常数
实验六:旋光法测定蔗糖转化反应的速率常数
一、实验目的:
1、了解反应的反应物浓度与旋光度之间的关系;
2、了解旋光仪的基本原理,掌握旋光仪的正确使用方法;
3、测定蔗糖转化反应的平均活化能;
二、实验原理:
蔗糖在水中水解成葡萄糖的反应为:
C12H22O11+H20→ C6H12O6+C6H12O6
蔗糖 葡萄糖 果糖
为使水解反应加速,反应常以H3O+ 为催化剂,故在酸性介质中进行水解反应中。在水大量存在的条件下,反应达终点时,虽有部分水分子参加反应,但与溶质浓度相比认为它的浓度没有改变,故此反应可视为一级反应,其动力学方程式为:lnC=-kt+lnC0
式中:C0为反应开始时蔗糖的浓度;C为t时间时的蔗糖的浓度。
当C=0.5C0时,t可用t1/2表示,即为反应的半衰期。
t1/2=ln2/k
上式说明一级反应的半衰期只决定于反应速率常数k,而与起始无关,这是一级 反应的一个特点。
蔗糖及其水解产物均为旋光物质,当反应进行时,如测定体系的旋光度的改变就可以量度反应的进程。而溶液的旋光度与溶液中所含旋光物质的种类、浓度、液层厚度、光源波长及反应温度等因素有关。为了比较各种物质的旋光能力,引入比旋光度[α]这一概念,并表示为:
[α]20D=α*100/(L*CA)
式中:20为实验时温度20℃;D为所用钠灯光源D线,波长589nm,α为旋光度;L为液层厚度(dm);C为浓度(g*100mL-1 ),当其他条件不变时,即:
A=K’C
(K’在一定条件下是一常数)。
且当温度及测定条件一定时,其旋光度与反应物浓度有下列关系:
反应时间为0时: α0=β反C0 (1)
反应时间为t时: αt=β反C+β生(C0-C) (2)
反应时间为 ∞ 时: α∞=β生C0 (3)
联立以上三式: [(1)-(3)]/[(2)-(3)] 代入式(4)中,得:
ln(αt-α∞)=-kt+ln(α0-α∞)
由上式可以看出,以ln(αt-α∞) 对t 作图可得一直线,由直线斜率即可求得反应速度常数k ,由截距可得到α0值。
三、实验步骤:
1、仪器装置
2、旋光仪的零点校正
根据蒸馏水为非旋光物质,可以用蒸馏水来校正旋光仪的零点。打开光源,调节目镜聚焦,使视野清晰,再旋转检偏镜至能观察到三分视野暗度相等为止。记下检偏镜的旋光度α,重复测量数次,取其平均值。此平均值即为零点,用来校正仪器系统误差。
3、反应过程的旋光度的测定
在锥形瓶中称取20g蔗糖,加入100ml蒸馏水,使蔗糖完全溶解,用移液管移取蔗糖溶液25ml,注入预先清洁干燥的50ml试管内并加盖;用另一支移液管移取25ml4.00mol·dm-3的HCL溶液,置于另一支50ml试管内加盖。
4、α∞的测定
将余下反应液置于50-60℃的水浴内温热40min,使其加速反应至完全,然后取出,冷至试验温度下测定旋光度,在10-15min内,读取5-7个数据,如在测量误差范围内,取其平均值,即为α∞值。
四、数据处理
数据记录:

1、将反应过程所测得的旋光度αt和对应时间t列表,作出αt-t曲线图。
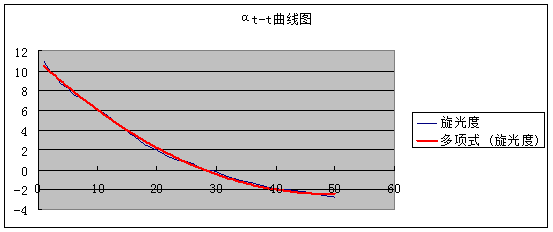 2、在αt-t曲线上,等间隔取8个(αt-t)数组,并通过计算,以㏑(αt-α∞)对t作图,由直线斜率求反应速率常数k并计算反应半衰期t1/2。
2、在αt-t曲线上,等间隔取8个(αt-t)数组,并通过计算,以㏑(αt-α∞)对t作图,由直线斜率求反应速率常数k并计算反应半衰期t1/2。
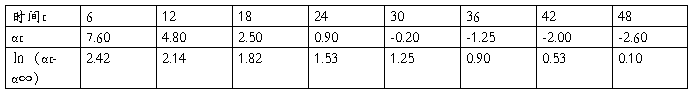

所以k=0.054, t1/2=ln2/k=13min
五、注意事项:
⑴ 装样品时,旋光管管盖旋至不漏液体即可,不要用力过猛,以免压碎玻璃片。
⑵ 在测定α∞时,通过加热使反应速度加快转化完全。加热温度不要超过60℃。
⑶ 由于酸对仪器有腐蚀,操作时应特别注意,避免酸液滴漏到仪器上。实验结束后必须将旋光管洗净。
⑷ 旋光仪中的钠光灯不宜长时间开启,测量间隔较长时应熄灭,以免损坏。
六、问题分析
1.实验中,我们用蒸馏水来校正旋光仪的零点,在蔗糖转化反应过程中,所测的旋光度αt是否需要零点校正?
答:蔗糖溶液以蒸馏水作溶剂,故用纯蒸馏水作零点校正。蔗糖转化反应过程中,无须再作零点校正,因都以蒸馏水作校正,只需校正一次。
2.配置蔗糖溶液时称量不够准确,对测量结果是否有影响?
答:有,当蔗糖称量过大时,使蔗糖浓度变大,蔗糖水解速率测量结果会偏大;反之则偏小。
3.在混合蔗糖溶液和盐酸溶液时,我们将盐酸加到蔗糖溶液中, 可否将蔗糖溶液加到盐酸溶液中去?为什么?
答:如将蔗糖溶液加到HCl溶液中,由于,HCl溶液浓度过大, 会加快蔗糖水解,影响测量结果。
4、本实验要想减少误差,应注意什么?
答:(1)正确操作仪器;
(2)准确配制蔗糖溶液浓度,HCL浓度也需精准。
