有 机 化 学 实 验 报 告

实 验 名 称: 无水乙醇的制备
学 院: 化学工程学院
专 业: 化学工程
班 级: 10-6班
姓 名: 学 号
指 导 教 师: 邵琼芳 陈 斌
日 期: 2011.11.13
一、 实验目的
1. 了解氧化钙法制备无水乙醇的原理和方法;
2. 熟练掌握回流、蒸馏装置的安装和使用方法。
二、 实验原理
普通工业酒精是含乙醇95.6%和4.4%水的恒沸混合物,其沸点为78.15℃,用蒸馏的方法不能奖乙醇中的水进一步除去。要制得无水乙醇,在实验室中可加入生石灰后回流,使水分与生石灰结合后再进行蒸馏,得到无水乙醇。
 CaO + H2O Ca (OH)2
CaO + H2O Ca (OH)2
简单蒸馏原理:利用混合液中各组分在热能驱动下,具有不同的挥发能力,使得各组分在气液两相中的组成之比发生改变,即易挥发组分(轻组分)在气相中增浓,难挥发组分(重组分)在液相中得到浓缩。
三、 主要试剂及物理性质
试剂:95%乙醇、CaO、NaOH、CaCl2、沸石。
仪器:100ml圆底烧瓶、直行冷凝管、球形冷凝管、干燥管、锥形瓶、接收器、表面皿、电炉、温度计、烧锅等。
四、 试剂用量规格

五、 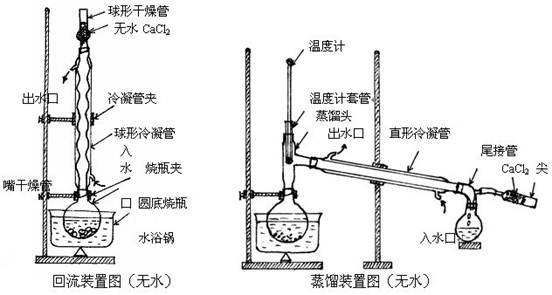 实验装置
实验装置
六、 实验步骤及现象
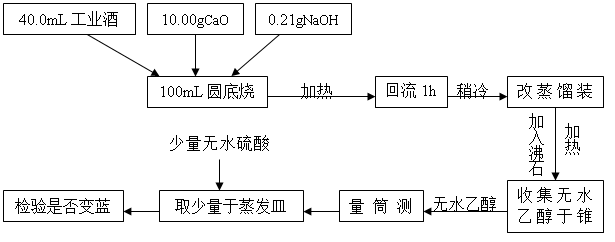
七、 数据记录和处理
实验回流时间9:10~10:10。
实验前数据记录表

实验数据记录

八、 实验讨论
造成损失的原因大致有以下几点:
1、回流时有部分乙醇逸出;
2、所用的实验仪器没有完全干燥;
3、蒸馏时间过短,导致无水乙醇没有收集完全。
九、 注意事项
1、仪器应事先干燥;
2、接引管支口上接干燥管,防止空气中的水分影响实验;
3、使用颗粒状的氧化钙,若使用粉末的氧化钙则暴沸严重;
4、实验后需要及时清理仪器。
第二篇:无水乙醇工艺制作开题报告
第一章 课题的背景与意义
1.1无水乙醇的特点及开发的目的
乙醇为无色透明状,易燃易挥发的液体。有酒的气味和刺激性辛辣味。溶于水、甲醇、 和氯仿。能溶解许多有机化合物和若干无机化合物。具有吸湿性。能与水形成共沸混合物。蒸汽与空气形成爆炸性混合物,爆炸极限4.3%-19.0%(体积)。无水乙醇相对密度0.7893(20/4℃),熔点-117.3℃,沸点 78.32℃,折射率1.3614,闪点(闭杯)14℃。
乙醇是重要的有机溶剂,广泛用于医药、涂料、卫生用品、化妆品、油脂等各个方面。 乙醇是重要的基本化工原料,用于制造乙醛、乙二烯、乙胺、乙酸乙酯、乙酸、氯乙烷等等,并衍生出医药、染料、涂料、香料、合成橡胶、洗涤剂、农药等产品的许多中间体,其制品多达300种以上。 75%的乙醇水溶液具有强杀菌能力,是常用的消毒剂。现在一些国家主要在研究乙醇燃料,如果能广泛应用,那将为我们解决能源危机带来很大的转机。燃料乙醇拥有相比汽油绝对的优势:
乙醇是燃油氧化处理的增氧剂,使汽油增加内氧,燃烧充分,达到节能和环保目的。乙醇具有极好的抗暴性能,调合辛烷值一般都在120以上,它可有效提高汽油的抗暴指数(辛烷值)。还有,在新标准汽油中,乙醇还可以经济有效地降低芳烃、稀烃含量、降低炼油厂的改造费用。更重要的是乙醇是太阳能的一种表现形成,在整个自然界这个大系统中,乙醇的整个生产和消费过程可形成无污染和非常清洁的闭路循环过程。永恒再生,永不枯竭。
正是因为乙醇有如此多的用处,而且理化性质很好,所以制造乙醇一直是人们研究的话题。20 世纪30年代以前,发酵法是乙醇的唯一工业生产方法。随着石油化工的迅速发展,合成法乙醇的产量越来越大。但合成法乙醇中夹杂的异构高碳醇,对人的高级神 经中枢的麻痹作用,不适宜用作饮料、食品、医药及香料等。因此,我们迫切需要制造无水乙醇的新工艺。
自从二十世纪七十年代发生能源危机以来,人们开始关注对可再生资源的利用,采用农作物原料发酵生产无水酒精替代或部分替代汽油被重新提上了日程。
1.2无水乙醇的现状
1.2.1 我国乙醇现状
我国对汽油醇的研究起步较晚,改革开放以来,我国粮食大幅度增产,由早期的勉强满足自给变为市场相对过剩 。20世纪90年代后期,我国对燃料乙醇进行试生产。
20##年我国已经将“大力发展汽油醇”产业列入“十五”计划当中,同时国务院已批准在东北、中原等省粮食基地建设几个十万吨以上的无水酒精生产基地[1]。这些都表明,我国政府巳开始大力地推动燃料酒精研究计划的进行。20##年,国家投资建立了4个大型燃料乙醇生产企业。并于20##年推广使用燃料乙醇。
20##年9月,发改委颁布了《可再生能源中长期发展规划》,燃料乙醇作为再生能源成为了政府重点推广的新型能源。
另外,《国家可再生能源中长期发展规划》中提出:到 20##年,生物燃料乙醇年利用量要达到1ⅹ107吨。
这些都表明,我国政府已开始犬力地推动燃料酒精研究计划的进行。
相比之下,一些发达国家的无水乙醇生产技术比较成熟,20世纪初,乙醇开始作为车用燃料应用,后因石油的大规模、低成本开采而中断。随着一些先进农业国劳动生产率的大幅度提高,以及70年代中期以来的石油危机,燃料乙醇在一些国家重新获得发展。美国、巴西于70年代中期率先推行燃料乙醇计划,加拿大、法国、西班牙、瑞典等国随之效仿,形成了一定的规模生产和应用市场。目前,一些具有农业资源优势的国家,如英国、荷兰、德国、奥地利、泰国、南非等国政府也已制定规划,积极发展燃料乙醇并推广应用车用乙醇汽油。
巴西政府发展燃料乙醇计划始于1975年,当时巴西80%的石油依赖进口,油价暴涨使巴西政府失去了40亿美元的外汇收入。1977年,在圣保罗推行20%乙醇的乙醇燃料,1980年将比例提高到26%,并在全国推广。巴西是目前世界上唯一不供应纯汽油的国家,汽油发动机车辆均使用乙醇汽油。主要车用燃料有三种:纯乙醇(乙醇含量大于93%)、乙醇汽油(乙醇含量20%~26%)和柴油。目前巴西乙醇产量的97%用于燃料,有370万辆以纯乙醇为燃料的汽车。
1.2.2巴西乙醇现状
20##年,巴西的乙醇产量达1139万吨,乙醇消费量超过952万吨,出口量180万吨。同年,车用燃料构成中,柴油占55.7%,按照乙醇占25%的比例调和的乙醇汽油占35.3%,纯乙醇直接作为汽车燃料的占6.6%。
1.2.3美国乙醇现状
20世纪30年代,美国就开展了燃料乙醇的研究及应用工作,70年代的世界石油危机和1990年美国国会通过空气清净法(修正案)是美国燃料乙醇发展的两个关键时期。1979年,联邦政府出台“乙醇发展计划”,减免联邦消费税,推广使用含10%乙醇的混合燃料(E10),乙醇产量从1979年的3万吨迅速增加到1990年的295万吨。1990年,美国国会通过空气清净法修正案,要求39个臭氧超标地区从1995年开始使用新配方汽油。目前,美国使用新配方汽油量约占全美汽油消耗量3.5亿吨的1/3。其中,大约有8%的新配方汽油使用乙醇作为增氧剂,乙醇添加量为5.7%。
据美国可再生燃料协会统计,当前美国共有81套乙醇生产装置,产能超过1044万吨/年,此外还有14套乙醇生产装置正在建设中。20##年产量645万吨、20##年产量863万吨,20##年达到1044万吨,已和巴西相差无几。
第二章无水乙醇的主要制备方法
由于乙醇与水存在着共沸点,采用普通精馏法无法得到浓度达到99%以上的无水酒精。一般说来,将发酵液中的酒精制成无水酒精要占据整个无水酒精生产过程中能耗的50%一80%.而其中大郭分能耗都发生在85%以上。采用苯恒沸精馏法时,每生产80kg无水乙醇,消耗175kg蒸汽和370kg水[2],每生产一吨无水乙醇,附加值约2000元[3],大大失去与汽油的竞争能力。因此,随着燃料酒精计划的实施,如何高效节能地制备燃料酒精已成为一个迫切需要的课题。目前制备无水酒精的方法主要有生石灰脱水法、萃取蒸馏法、真空蒸馏法、离子交换树脂法、恒沸精馏法、盐溶精馏法、无水硫酸钙法、作物吸附法、分子筛法以及膜分离法等。其中,作物吸附法、分子筛法和膜分离法作为新型的方法,具有良好的发展前景,已经在实践中得到了应用。
本次的工艺设计就是针对无水乙醇的一些制作方法,选择了分子筛法,研究其优点,缺点及可行性。
2.1分子筛法生产无水乙醇的原理[4]:
分于筛吸附法实现分离的原理主要是位阻效应。因为水分子的分子直径只有28nm,而酒精的分子直径为44nm,因此,水分子可以进入分子筛内部,而酒精分子则被阻挡在外,从而实现对水、甲醇等小分子与酒精的选择性吸附分离。但对于不同的分子筛,尽管其均为3A分子筛,但是在同样的操作条件下,其分离效果有所不同。Carmo等[4]通过对分子筛吸附过程动力学和热力学进行研究,从中筛选出了效果最佳的分子筛。通过对固定吸附床穿透曲线的研究,Teo等[5]发现在颗粒大小和气速不同的情况下,颗粒内扩散传质阻力是整个吸附过程中的主要传质阻力。但在低的气速和高浓度的情况下,外膜阻力也对传质具有一定的影响。穿透曲线可以很好地用weber和Chakravorti而模型[6]模拟,这为进一步对装置进行放大和经济评价提供了理论依据。
吸附过程是一个放热过程,由于分子筛所吸附的水静电作用力非常强,因此其放热更为明显,这使得吸附温度明显上升。在进行气相吸附时,为了打破酒精一水共沸体系,吸附温度有可能会上升到120℃,这对吸附过程的等温线以及产品的质量产生了很大的影响[7,8]。因此,研究吸附过程中吸附床层的温度变化曲线就具有很大的意义。Salcm研究了吸附床层中温度变化曲线与穿透曲线的关系以及它对产品脱水效果的影响,发现温度变化曲线会以稍快于或等于传质曲线的速率穿越床层。对于给定的流速,初始流出物中水的含量以及温度曲线的最高点与进料中水的浓度直接成正比。对于给定的进料浓度,可通过降低进料速率的方法来降低流出物中水的含量及最高温度。此外.Garg研究了如何通过控制温度曲线来控制酒精一水共沸溶液的脱水。
2.2分子筛法生产无水乙醇的优势
分子筛吸附法也是近20年来发展起来的方法,它在工业上已经有大规模应用。分子筛法与其他方法相比主要具有以下特点:
(1)能耗较低。在没有考虑与其他过程集成从而进行能量综合利用的前提下,能耗少于560KJ/L。
(2)操作简便。
(3)可以全过程采用自动化控制,劳动强度小。
(4)整个过程中没有使用任何有毒化学物质。
(5)产品质量高。
分子筛法自动化程度高,劳动强度小,同时产品质量好,但再生时能耗较大,因而导致整体成本略有上升,适合于大规模的工业化生产,通过规模经营减少其对总成本的影响。
第三章研究内容
3.1工艺流程图

3.2工艺流程说明
无水酒精的制造与一般酒精制造方法不同,它不能用普通的精馏方法精馏出
来,因为酒精—水混合物在酒精成分达95%(v/v) 时达到它们的共沸点78.15
℃,此时汽、液两相中的酒精含量相等,都是95%(v/v),所以采用普通的精馏方
法无法生产出超过95%(v/v)的酒精,因此为了提高酒精浓度,去除多余的水分,
则需要采用特殊的脱水方法才能完成。
本工艺采用的是吸附法脱水,常用的吸附剂有石灰、活性炭、离子交换树脂、
分子筛、硅胶等。目前国际上公认分子筛脱水法节能效果好,以分子筛脱水法生
产无水酒精最常用。分子筛是一类具有骨架结构的硅铝酸盐晶体。晶体内的阳离
子和水分子在骨架中有很大的移动自由度,可进行阳离子交换和可逆地脱水。
第四章进度安排

参考文献:
[1] 黄宇彤,杜连样,赵继湘。世界燃料酒精生产形势,酿酒.2001,(s):24.
[2] 无锡轻工业学院,等。酒精工艺学[M]。第一版,北京:叶国财政经济出版社,1961,511.
[3] 张久恺,刘大中.山东轻工业学院学报[M].1998,(3):1
[4] Carmo,M. J.,Gubulin,J .C. Ethanol—water adsorption on commercial
3A zeolites:kinetic and thermodynamic data Brazilian Jounmal of Chemical Engineering,Vol.14.1997:217
[5] Wah Koom Teo;Ruthven,Douglas M. Adsorption of Water from Aqueous Ethanol Using 3A Molleculor Sieves.Ind Eng Chern Process Des Dev.Vol.25,1986,17.
[6] Weber,T.W.,Chakravorti,R.K.Pore and Solid Diffusion Models for
Fixed—bed Adsorbers. AlchE J.,Vol. 20,No.2.1974:228.
[7] B.D Crittenden,B. Sowerby. Advances in separation process.IChemE
Symp. Ser.Vol .118,1990:55.
[8] B.Sowerby.Dryang 0f 0rganic Vapour by Adsorption.PhD Thcsis University of Bath,1988.
