有 机 化 学 实 验 报 告

实 验 名 称: 无水乙醇的制备
学 院: 化学工程学院
专 业: 化学工程与工艺
班 级: 化工11-2班
姓 名:赵应松 学 号11402010242
指 导 教 师: 方烨汶 张莉
日 期: 20##年10月18日
一、实验目的
1、了解氧化钙法制备无水乙醇的原理和方法。
2、学会制备教学用的无水乙醇,并掌握蒸馏技术
3学会检测无水乙醇的方法。
4初步掌握实验中易燃依然有机物的一般灭火知识。
二、实验原理
普通工业酒精是含乙醇95.6%和4.4%水的恒沸混合物,其沸点为78.15oC,用蒸馏的方法不能将乙醇中的水进一步除去。要制得无水乙醇,在实验室中可加入生石灰后回流,使水分与生石灰结合后再进行蒸馏,得到无水乙醇。
CaO + H2O → Ca(OH)2
三、试剂用量及规格
40ml 95%乙醇、10g生石灰、0.1gNaOH、CaCl。
四、仪器装置
![RJ0P7D)]UAD_1$OQRAA3~0C](https://upload2.fanwen118.com/wk001/3409915/3409915_img_003.jpg)
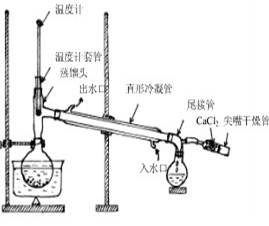
回流装置 .蒸馏装置
五、实验步骤及现象

六、实验结果

七、注意事项
1.仪器要先干燥,接引管支口接干燥管,防止水蒸气进入。
2必须在烧瓶中加入沸石,以防止回流和蒸馏过程中发生爆沸。
3蒸馏开始时,应缓慢加热,使瓶内的物流缓慢升温。当温度计的温度达到乙醇的沸点时,在收集流出液.
4当烧瓶中的物料变为糊状物时,表示蒸馏已接近尾声。此时,停止加热,利用余温将剩余的液体蒸出。
八·实验讨论
1
(1)在蒸馏烧瓶中放少量碎瓷片,防止液体暴沸。
(2)温度计水银球的位置应与支管口下缘位于同一水平线上。
(3)蒸馏烧瓶中所盛放液体不能超过其容积的2/3,也不能少于1/3。
(4)冷凝管中冷却水从下口进,上口出。(5)加热温度不能超过混合物中沸点最高物质的沸点
第二篇:无水乙醇的制备实验报告
有 机 化 学 实 验 报 告

实 验 名 称 无水乙醇的制备
学 院: 化学工程学院
专 业: 化学工程与工艺
班 级: 化工10-5班
姓 名:王雪霞 学 号 10402010508
指 导 教 师: 沈梁钧 方烨汶
日 期: 2011年11月6日
一、 实验目的
1. 学会氧化钙法制备无水乙醇的原理和方法。
2. 掌握回流和蒸馏的基本操作。
二、 实验原理
普通的工业酒精是含乙醇95.6%和4.4%水的恒沸混合物,其沸点为78.16℃,用蒸馏或分馏的方法不能将水进一步除去。
可利用氧化钙与工业酒精中的水反应生成不挥发,一般加热不分解的熟石灰(氢氧化钙),以得到无水乙醇。
CaO+H2O→Ca(OH)2
为了使反应充分进行,让其加热回流一段时间。制得的无水乙醇(纯度可达99.5%)再用蒸馏法收集。
三、 主要试剂及物理性质
95%乙醇:乙醇是无色、透明、有香味、易挥发的液体,熔点-117.3℃,沸点78.16℃。
生石灰:白色或带灰色块状或颗粒。熔点2572℃。沸点2850℃。折光率1.838。
溶于水成氢氧化钙并产生大量热,溶于酸类、甘油和蔗糖溶液,几乎不溶于乙醇。
相对密度3.32~3.35。
氢氧化钠:熔点318.4℃,沸点1390℃。纯的无水氢氧化钠为白色半透明,结晶状固体。氢氧化钠极易溶于水,溶解度随温度的升高而增大,溶解时能放出大量的热。
氯化钙:白色晶体或块状物。熔点782℃,沸点1600℃,密度2.15克/厘米3( 25℃)。
四、 试剂用量规格
95%乙醇40ml,生石灰10g,无水硫酸铜适量,氯化钙适量,氢氧化钠少许。
五、 仪器装置
回流装置 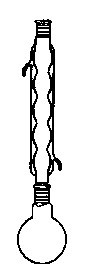 蒸馏装置
蒸馏装置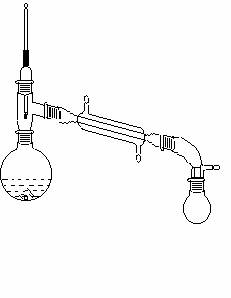
六、 实验步骤及现象
1. 回流加热除水
在100ml的圆底烧瓶中,首先加入10g粉末状的氧化钙和几片氢氧化钠,再加入40ml95%乙醇。回流一小时。
记录:9点33分,溶液开始加热。9点39分,溶液开始沸腾。
2. 蒸馏
回流完毕后,改为蒸馏装置,以圆底烧瓶做接受器,接引管支口上接盛有无水氯化钙
的干燥管。所得的乙醇密封储存,并用无水硫酸铜检验。
记录:开始沸腾的温度为39℃,出馏分时的温度为76℃。10点46分,第一滴液滴出
现。11点32分,最后一滴液滴出现。
3. 检验
记录:用无水硫酸铜检验所得液体,溶液微微变蓝。
七、 实验结果
所得溶液的体积为33ml,产率a%=(33/40)×100%=82.5%
八、 实验讨论
在更换装置时,没有塞上空心塞,使空气进入或是在连接蒸馏装置时没有在磨口处紧密连接,导致空气进入,最后使液体检验时溶液微微变蓝。
更换装置时,动作不及时或没有塞上空心塞使酒精部分挥发,加热时装置间没有紧密连接,蒸馏结束判断失误等原因导致产率偏低。
