求实中学高二第一次月考
生物试卷
一、选择题(每题2分,共48分)
1、下列关于同源染色体概念的叙述中,正确的是
A.由一条染色体复制而形成的两条染色体
B.来自父方(或母方)的全部染色体
C.形状、大小必须都相同的两条染色体
D.在减数分裂过程中彼此联会的两条染色体
2、在减数第一次分裂中,发生了
A.同源染色体分离,非同源染色体自由组合
B.同源染色体分离,同时着丝点也随着分裂
C.着丝点的分裂引起了同源染色体的分离
D.着丝点的分裂引起非同源染色体自由组合
3、在高等动物的细胞分裂中,既有同源染色体,又有姐妹染色单体的时期是
A.有丝分裂的前期 B.有丝分裂的后期
C.减数第二次分裂中期 D.减数第二次分裂后期
4、下图为某雌性动物体内的一个细胞示意图,该细胞的名称是
A.卵原细胞
B.初级卵母细胞
C.次级卵母细胞
D.卵细胞
5、下列关于联会和四分体的说法正确的是
A.联会的染色体经过复制形成四分体 B.四分体是联会的同源染色体
C.联会时期的染色体是不含染色单体的 D.一个四分体含有四个染色体
6、下列是具有二同源染色体的动物卵细胞图,正常情况下不能出现的是
7、某生物的体细胞内含有三对同源染色体(AA′、BB′、CC′),经减数分裂产生的ABC型配子占配子总数的( )
A.1/2 B.1/

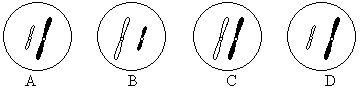
4
1
C.l/8 D.1/16
8、在正常情况下,刚形成的次级精母细胞与体细胞相比
A. 染色体数减半,DNA含量不变 B. 染色体数减半,DNA含量也减半
C.染色体数不变,DNA含量不变 D. 染色体数不变,DNA含量减半
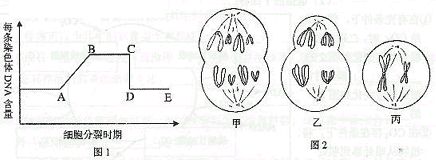
9、下图表示某生物体内有关细胞分裂图解与图像。根据图示下列叙述不正确是
A.甲图细胞位于图1的DE段
B.图1中CD段形成的原因是由于细胞分裂成两个子细胞
C.由乙图可判断该生物是雌性动物
D.丙图与图1的BC段相吻合
10、800个卵原细胞和400个精原细胞成熟后,理论上最多能形成的受精卵数是 A.400个 B.800 个
C.1600 个 D.3200个
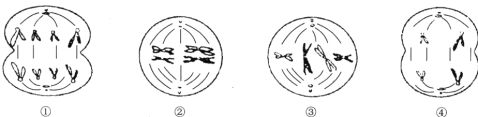
11、下图是某种动物不同细胞分裂的图像,下列与此相关的叙述中,不正确的是
A.只有④所示细胞不具有同源染色体
B.动物的睾丸中有可能同时发现上述4种细胞
C.图②所示细胞具有同源染色体
D.①②③细胞中均含有8条染色单体
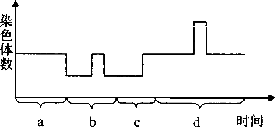
12、下图表示在不同生命活动过程中,细胞内染色体的变化曲线,下列叙述正确的是
2
A.a过程没有姐妹染色单体 B.b过程细胞数目不变
C.c过程发生细胞融合 D.d过程没有同源染色体
13、下列有关孟德尔遗传规律的说法错误的是
A.叶绿体基因控制的性状遗传不遵循孟德尔遗传规律
B.受精时,雌雄配子的结合是随机的,这是得出孟德尔遗传规律的条件之一
C.孟德尔发现分离定律与自由组合定律的过程运用了假说—演绎法
D.基因型为AaBb的个体自交,其后代一定有4种表现型和9种基因型
14、果蝇的灰身和黑身是常染色体上的一对等位基因控制的相对性状。用杂合的灰身雌 雄果蝇杂交,去除后代中的黑身果蝇,让灰身果蝇自由交配,理论上其子代果蝇基 因型比例为
A.4∶4∶1 B.3∶2∶1
C.1∶2∶1 D.8∶1
15、已知水稻高秆(T)对矮秆(t)为显性,抗病(R)对感病(r)为显性,两对基因独立遗传。
现将一株表现型为高秆、抗病植株的花粉授给另一株表现型相同的植株,F1高秆∶ 矮秆=3∶1,抗病∶感病=3∶1。再将F1中高秆抗病类型分别与矮秆感病类型进行 杂交,则产生的F2表现型之比理论上为
A.9∶3∶3∶1 B.1∶1∶1∶1
C.4∶2∶2∶1 D.3∶1∶3∶1
16、下列叙述中,正确的是
A.两个纯合子的杂交后代必是纯合子
C.纯合子自交后代都是纯合子 B.两个杂合子的杂交后代必是杂合子 D.杂合子自交后代都是杂合子
17、豌豆黄色(Y)对绿色(y)呈显性,圆粒(R)对皱粒(r)呈显性,这两对基因自由组合。甲豌豆(YyRr)与乙豌豆杂交,其后代中四种表现型的比例是3∶3∶1∶1。乙豌豆的基因型是
A.yyRr
C.yyRR B.YyRR D.YyRr
18、将基因型为AaBbCc和AABbCc的向日葵杂交,按基因自由组合定律,后代中基因型为AABBCC的个体比例应为()
A.1/8
C.1/32 B.1/16 D.1/64
19、大豆的白花和紫花是一对相对性状。下列四组杂交实验中,能判断出显性、隐性关系的是()
①紫花×紫花→紫花
②紫花×紫花→301紫花+101白花
3
③紫花×白花→紫花
④紫花×白花→98紫花+102白花
A.①和②
C.①和③ B.②和③ D.③和④
20、基因型为HH的绵羊有角,基因型为hh的绵羊无角,基因型为Hh的绵羊,母羊无角,公羊有角。现有一头有角母羊生了一头无角小羊,这头小羊的性别和基因型分别为
A.雄性,hh
C.雄性,Hh B.雌性,Hh D.雌性,hh
21、孟德尔的两对相对性状的遗传杂交实验中,具有1∶1∶1∶1比例的是
①F1产生配子类型的比例 ②F2表现型的比例
③F1测交后代类型的比例 ④F1表现型的比例⑤F2基因型的比例
A.②④
C.④⑤ B.①③ D.②⑤
22、西葫芦是一种雌雄异花同株的植物,其皮色性状中的黄皮基因(M)对绿皮基因(m)为显性,但有白皮显性基因(W)存在时,基因M和m都会受到抑制。已知这两对等位基因独立遗传,下列叙述正确的是
A.西葫芦皮色能稳定遗传的植株的基因型共有5种
B.基因型为mmW_西葫芦由于没有M基因,所以表现为白色
C.基因型为Mmww与基因型为mmWw的植株测交,后代有3种表现型
D.基因型为MmWw的西葫芦个体自交,后代表现型比例为9︰3︰4
23、孟德尔利用豌豆作为实验材料进行植物杂交实验,成功地发现了生物的遗传规律。下列各项中不能作为豌豆作为遗传实验材料的优点是
A. 豌豆是严格的闭花自花授粉植物 B. 豌豆在自然状态下一般是纯种
C. 豌豆具有许多明显的相对性状 D. 杂种豌豆自交后代容易发生性状分离 24、某植物细胞的基因型为Aa,该细胞在分裂过程中携带A和携带a的一对同源染色体存在以下两种情况:
① 减数第一次分裂正常,减数第二次分裂不正常
②减数第一次分裂不正常,减数第二次分裂正常
若上述两种情况中不正常分裂时染色体都移向一极,下列有关配子说法中正确的是
A.两种情况下配子的基因型都为Aa
B.两种情况下配子的基因型都为AA或aa
C.第①种情况下,配子的基因型可为AA或aa,第②种情况下,配子基因型可为Aa
D.第①种情况下,配子的基因型可为Aa,第②种情况下,配子基因型可为AA或aa
4
二、非选择题(每空2分,共52分)
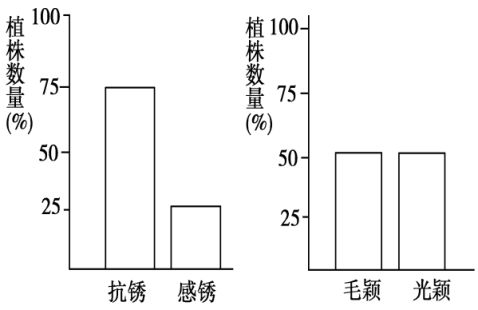
25、小麦的毛颖和光颖是一对相对性状(显、隐性由P、P基因控制),抗锈和感锈是另一对相对性状(由R、r控制),控制这两对相对性状的基因位于两对同源染色体上。以纯种毛颖感锈(甲)和纯种光颖抗锈(乙)为亲本进行杂交,F1均为毛颖抗锈(丙)。再用F1与丁进行杂交, F2有四种表现型,对每对相对性状的植株数目作出的统计结果如下图:
(1)亲本甲、乙的基因型分别是: ; 丁的基因型是 。 (2)F2中,基因型为PPRR个体所占的比例是 ,光颖抗锈植株所占的比例是 。 (3)F2中,表现型不同于双亲(甲和乙)的个体占全部F2代的 。 (4)写出F2中抗锈类型的基因型及比例 。
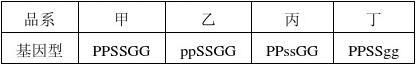
26、玉米果皮黄色(PP)对白色(pp)为显性,非甜味胚乳(SS)对甜味胚乳(ss)为显性,黄色胚乳(GG)对白色胚乳(gg)为显性,三对基因分别位于不同的同源染色体上。现有甲、乙、丙、丁(1)若要利用果皮黄色与白色这一对相对性状来验证基因分离定律,可作为亲本的组合有_____________________(填写品系类型)。
(2)甲和丁________(能/不能)作为亲本进行验证自由组合定律的实验,原因是 _____________________________________________________________________。 (3)丙和丁杂交获得F1,再自花受粉,后代中出现黄色果皮、甜味、白色胚乳的概率是________,出现白色果皮、非甜味、白色胚乳的概率是________。
27、下图为某家族某种遗传病的遗传系谱,请据图回答(相关的遗传基因用A、a表示)
5
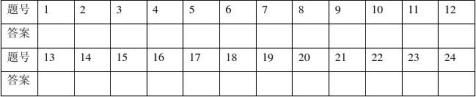
(1)该病是由_________ 性基因控制的。
(2)Ⅰ3和Ⅰ4都是正常,但他们有一儿子为患者,此现象在遗传学上称为_____________________________________。
(3)Ⅱ3是杂合体子的概率是__________。
(4)Ⅱ2与Ⅱ3婚配,生一患病女孩的概率是__________,如果已经生了一个患病女儿,再生一个患病孩子的概率是__________。
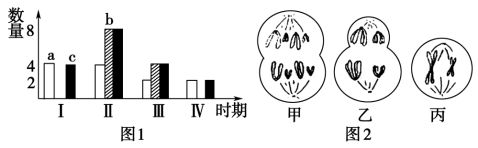
28、下图中图1和图2分别表示某动物(2n=4)体内细胞不同时期细胞内染色体、染色单体和DNA含量的关系及细胞分裂图象,请分析回答:
(1)图1中a~c柱表示染色单体的是________,图1中所对应的细胞中存在同源染色体的是________。
(2)图1中Ⅱ的数量关系对应于图2中________,由Ⅱ变为Ⅲ ,相当于图2中________→________的过程。
(3)图2中乙细胞产生的子细胞名称为__________________________________。
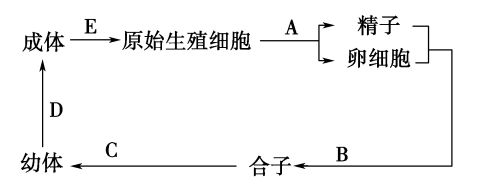
29、下图为某生物生活示意图。请据图回答:
\
(1)下列过程的细胞分裂方式分别是:A___________;C___________;E___________。
(2)B过程称为___________;A、B过程的意义是___________________________ ____________________________________________________________________。
6
求实中学高二第一次月考
生物试卷答案
25、(1)PPrr,ppRR ppRr (2)1/8 3/8 (3)1/2
(4)RR:Rr=1:2。
26、(1)乙与甲、乙与丙、乙与丁 (答到一组即给分) (2)不能 甲与丁之间只具有一对相对性状
(3)1/16 0 27、(1)隐 (2)性状分离 (3)2/3 (4)1/18 1/4
28、(1)b Ⅰ、Ⅱ
(2)乙 乙→丙(此算一空) (3)次级卵母细胞、极体
29、减数分裂 有丝分裂 有丝分裂
(2)受精作用 对于维持每种生物前后代染色体数目的恒定,对于生物的遗传和变异,都是十分重要的
7
第二篇:高二上学期第一次月考
大成中学高二第一学期第一次月考化学试题
可能用到的原子量:H:1 C:12 O:16 S:32 Cl:35.5 Cu:64 Mn:55 Zn:65
一、选择题:(每小题只有一个正确选项,每小题2分,共32分)
1.下列过程中△H<0的是( )
A. 氯酸钾分解制氧气 B. 实验室用氯化铵和氢氧化钙制氨气
C.煅烧石灰石制生石灰 D.盐酸与NaOH溶液反应
2.下列说法或表示方法正确的是 ( )
A.若将等量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 B.由―C(石墨)→C(金刚石) ΔH=+1.9KJ/mol‖可知,金刚石比石墨稳定 C.在稀溶液中:H(aq)+OH(aq)=H2O(l) △H=-57.3KJ·mol+--1
若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热量大于57.3KJ
D.在101KPa时,2gH2完全燃烧生成液态水,放出285.8KJ热量,氢气燃烧的热化学方程
式表示为:2H2(g)+O2(g)=2H20(l)ΔH=+285.8KJ/mol
3.已知:①2C(s)+O2(g)===2CO(g) ΔH=-221.0 kJ·mol1; -
②2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ·mol1。 -
则制备水煤气的反应C(s)+H2O(g)===CO(g)+H2(g)的ΔH为 ( )
A.+262.6 kJ·mol
C.-352.3 kJ·mol-1 B.-131.3 kJ·mol-1 -1 D.+131.3 kJ·mol1 -
-1 4.已知:H2O(g)===H2O(l) ΔH=Q1 kJ·mol C2H5OH(g)===C2H5OH(l) ΔH=Q2 kJ·mol1 C2H5OH(g)-
-+3O2(g)===2CO2(g)+3H2O(g) ΔH=Q3 kJ·mol1 若使46 g酒精液体完全燃烧,最后恢复到室温,
则放出的热量为 ( )
A.(Q1+Q2+Q3) kJ B.0.5(Q1+Q2+Q3) kJ
C . (0.5Q1-1.5Q2+0.5Q3) kJ D.(3Q1-Q2+Q3) kJ
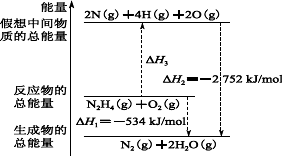
5. 肼(H2NNH2)是一种高能燃料,有关化学反应的能量变化如
图所示。已知断裂1 mol化学键所需的能量(kJ):N≡N为
942、O=O为500,N—N为154,则断裂1 mol N—H键所需
的能量(kJ)是
A.194 B.391 C.516 D.658
6.我国首创的海洋电池以铝板为负极,铂网为正极,海水为
电解质溶液,空气中的氧气与铝反应产生电流。电池总反应为4Al+3O2+6H2O===4Al(OH)3,下列说法不正确的是 ( )
A.正极反应式为O2+2H2O+4e== 4OH
B.电池工作时,电流由铝电极沿导线流向铂电极
--
C.以网状的铂为正极,可增大与氧气的接触面积
D.该电池通常只需更换铝板就可继续使用
7. 研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源。该电池以金属锂和钢板为电极材料,以LiOH为电解质,使用时加入水即可放电。关于该电池的下列说法不正确的是( )
A.水既是氧化剂又是溶剂 B.放电时正极上有氢气生成
C.放电时OH向正极移动 D.总反应为:2Li+2H2O===2LiOH+H2↑
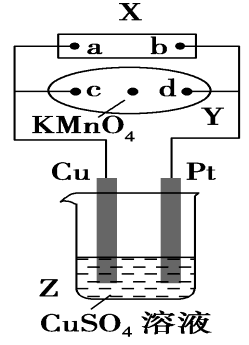
8. 图中X为电源,Y为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一
滴KMnO4溶液,通电后Y中央的紫红色斑向d端扩散。下列判断正确的
是 ( ) -
A.Z中溶液的pH不断增大
B.Cu电极质量减小,Pt电极质量增大
C.滤纸上c点附近会变红色
D.溶液中的SO42向Cu电极定向移动 -
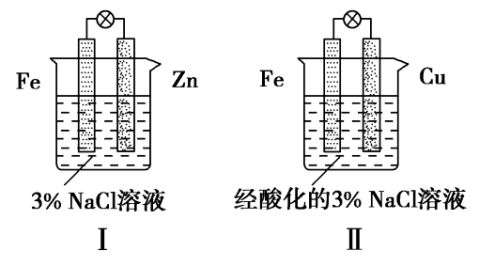
9. K3[Fe(CN)6] 铁氰化钾,别名赤血盐,深红色或红色单
斜晶系柱状结晶或粉未,有剧毒。遇亚铁盐生成蓝色沉
淀。结合下图判断,下列叙述正确的是
A.Ⅰ和Ⅱ中负极反应均是Fe-2e===Fe2 -+
B.Ⅰ和Ⅱ中正极均被保护
C.Ⅰ和Ⅱ中正极反应均是O2+2H2O+4e===4OH --
D.Ⅰ和Ⅱ中分别加入少量K3[Fe(CN)6]溶液,均有蓝色沉淀
10.下列关于铜电极的叙述正确的是( )
A.在电解池中,铜做阳极时,溶液中的阴离子在铜极上失电子
B.用电解法精炼铜时粗铜做阴极
C.在镀件上电镀铜时,可用金属铜做阳极
D.电解稀硫酸制O2、H2时,铜做阳极
11.电解CuCl2溶液时,如果阴极上有1.6g铜析出,则阳极上产生气体的体积(标准状况)约为
A.0.28L B.0.56L C.0.14L D.11.2L
12.用惰性电极电解CuCl2和NaCl的混合溶液,阴极和阳极上分别析出的物质是( )
A.H2和Cl2 B. Cu和Cl2 C. H2和O2 D. Cu和O2
13.用惰性电极电解下列溶液,一段时间后,再加入一定质量的另一种物质(中括号内),溶液能与原来溶液完全一样的是( )
A. CuCl2[CuO] B.NaOH[Na2O]
C.NaCl[HCl] D. CuSO4[Cu(OH)2]
14.金属镍有广泛的用途。粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是(已知:氧化性Fe2+<Ni2+<Cu2+)( )
A. 阳极发生还原反应,其电极反应式:Ni2++2e? =Ni
B. 电解过程中,阳极质量的减少与阴极质量的增加相等
C. 电解后,溶液中存在的金属阳离子只有Fe2+
D. 电解后,电解槽底部的阳极泥中只有Cu和Pt
15. 下列关于金属腐蚀的说法正确的是 ( )
A.金属在潮湿的空气中腐蚀的实质是:M+nH2O===M(OH)n+n/2H2↑
B.金属的化学腐蚀的实质是:M-ne===Mn,电子直接转移给还原剂
C.金属的化学腐蚀必须在酸性条件下进行 -+
D.在潮湿的中性环境中金属的电化学腐蚀主要是吸氧腐蚀
16.用惰性电极电解下列溶液,电解一段时间后,阴极质量增加,电解质溶液的pH下降的是( )
A. CuCl2 B. AgNO3 C.BaCl2 D.H2SO4
二、填空题:(每小题只有一个正确选项,每小题3分,共48分)
17.(8分,每空2分)用―>‖、―<‖或―=‖填空:
(1)相同条件下,2mol氢原子所具有的能量 1mol氢分子所具有的能量。
(2)已知常温时红磷比白磷稳定,比较下列反应中ΔH的大小:ΔH1H2 。
①P4(白磷,s)+5O2(g)===2P2O5(s) ΔH1 ②4P(红磷,s)+5O2(g)===2P2O5(s) ΔH2
(3)已知:稀溶液中,H(aq)+OH(aq)===H2O(l) ΔH=-57.3 kJ/mol,则浓硫酸与稀NaOH溶液反应生成1 mol水,放出的热量 57.3 kJ。
(4)已知一定条件下合成氨反应:N2(g)+3H2(g)? 2NH3(g) ΔH=-92.0 kJ·mol1,相同条件下将-+-
1 mol N2和3 mol H2放在一密闭容器中充分反应,测得反应放出的热量(假定热量无损失) 。
18.(15分)已知下列热化学方程式:
1-①H2(g)+2(g)=H2O(l) ΔH=-285.8 kJ·mol1 21-②H2(g)+2(g)=H2O(g) ΔH=-241.8 kJ·mol1 21-③C(s)+O2(g)=CO(g) ΔH=-110.5 kJ·mol1 2
④C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol1, -
回答下列问题:
(1)上述反应中属于放热反应的是____________。
(2)H2的燃烧热为____________;C的燃烧热为____________。
(3)燃烧10 g H2生成液态水,放出的热量为____________。
(4)写出CO燃烧的热化学方程式__________________________________。
19.(12分) Zn—MnO2干电池应用广泛,其电解质溶液是ZnCl2—NH4Cl混合溶液。
(1)若ZnCl2—NH4Cl混合溶液中含有杂质Cu2,会加速某电极的腐蚀,其主要原因是 +
Cu2+,最好选用下列试剂中的 (填代号)。
a.NaOH b.Zn c.Fe d.NH3·H2O
(2)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液。阴极的电极反应式是 。若电解电路中通过2mol电子,MnO2的理论产量为 。
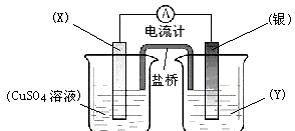
20.(18分)依据氧化还原反应:2Ag(aq) + Cu(s) == Cu(aq) + 2Ag(s)设计的原电池如+2+
图所示。请回答下列问题:
(1)电极X的材料是 ;
电解质溶液Y是 ;
(2)银电极为电池的 极,
发生的电极反应为 ;
X电极上发生的电极反应为;
(3)外电路中的电子的移动方向是 。
三、实验题(本题包括1小题,共15分)
21.(15分)盐酸或硫酸和氢氧化钠溶液的中和反应没有明显的
现象。某学习兴趣小组的同学为了证明氢氧化钠溶液与盐酸或
硫酸发生了反应,从中和反应的热效应出发,设计了下面几种
实验方案。请回答有关问题。
(1)方案一:如图组装好实验装置,图中小试管用细线吊
着,细线的上端拴在细铁丝上。开始时使右端U形管两端红墨水相平。实验开始,向下插细铁丝,使小试管内盐酸和广口瓶内氢氧化钠溶液混合,此时观察到的现象是____________,原因是______________。
(2)方案二:该小组借助反应溶液温度的变化来判断反应的发生。如果氢氧化钠溶液与盐酸混合前后有温度的变化,则证明发生了化学反应。该小组同学将不同浓度的氢氧化钠溶液和盐酸各10 mL
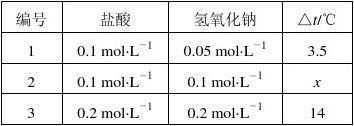
则x=____________。
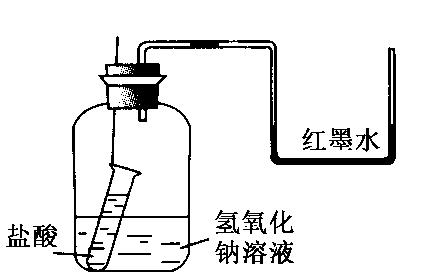
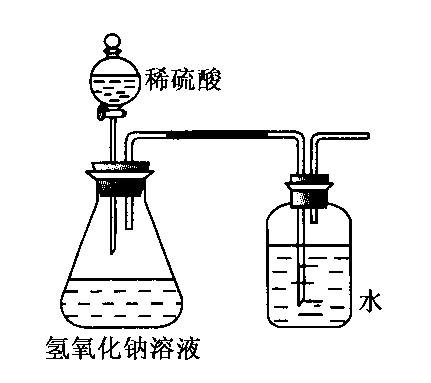
(3)方案三:该小组还设计了如图所示装置来证明氢氧化钠溶液确实与稀硫酸发生了反应。他们认为若洗气瓶中导管口有气泡冒出,则说明该反应放出热量,从而证
明发生了反应。
①实验时,打开分液漏斗活塞,发现导管流出液体不畅,原因可
能是__________________________________。
②从原理上讲,该实验设计的不合理之处为_______________。
班级 姓名 电脑号 大成中学高二第一学期第一次月考化学答题卡 18.(15分) (1) (2) (3) (4) 19. (16分)(1) (2) 20.(共18分) (1) (2) (3) 21.(15分)(1) (2) (3)① ②
大成中学高二第一学期第一次月考化学参考答案
一、选择题
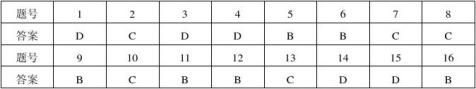
二、填空题
17.(8分,每空2分) (1)> (2)< (3)> (4)<
18. (1)①②③④
(2)285.8 kJ/mol 393.5 kJ/mol (3)1429 kJ
1
(4)CO(g)+O2(g)=CO2(g) ΔH=-283 kJ/mol
2
19. (12分)(1)Zn与Cu2+反应生成Cu,Zn与Cu构成原电池,加快反应速率 b
(2)2H++2e-=H2↑ 87g
20.(共18分)
(1) Cu 硝酸银溶液
(2) 正极 Ag+ + e – = Ag Cu - 2e – =Cu (3) X电极流向Ag电极
21. (1)U形管内液面左边下降、右边升高 盐酸和氢氧化钠发生中和反应放出热量,使瓶内气体温度升高,压强增大
(2)7
(3)①没打开分液漏斗上部塞子
②稀硫酸具有一定的体积,冒出气泡的原因可能是加入稀硫酸的体积引起的
