醇 酚
一、认识醇和酚
羟基与 相连的化合物叫做醇;羟基与 直接相连形成的化合物叫做酚。
二、醇的性质和应用
1.醇的分类
(1)根据醇分子中羟基的多少,可以将醇分为
饱和一元醇的分子通式:
(2)根据醇分子中羟基所连碳原子上氢原子数目的不同,可以分为
2.醇的命名(系统命名法)
一元醇的命名:选择含有羟基的最长碳链作为主链,把支链看作取代基,从离羟基最近的一端开始编号,按照主链所含的碳原子数目称为“某醇”,羟基在1位的醇,可省去羟基的位次。
多元醇的命名:要选取含有尽可能多的带羟基的碳链作为主链,羟基的数目写在醇字的前面。用二、三、四等数字表明
3.醇的物理性质
(1)状态:C1-C4是低级一元醇,是无色流动液体,比水轻。C5-C11为油状液体,C12以上高级一元醇是无色的蜡状固体。甲醇、乙醇、丙醇都带有酒味,丁醇开始到十一醇有不愉快的气味,二元醇和多元醇都具有甜味,故乙二醇有时称为甘醇(Glycol)。
甲醇有毒,饮用10毫升就能使眼睛失明,再多用就有使人死亡的危险,故需注意。
(2)沸点:醇的沸点比含同数碳原子的烷烃、卤代烷 。且随着碳原子数的增多而 。
(3)溶解度:低级的醇能溶于水,分子量增加溶解度就降低。含有三个以下碳原子的一元醇,可以和水混溶。
4.乙醇的结构
分子式:C2H6O
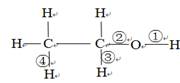 结构式:
结构式:
结构简式:CH3CH2OH
5.乙醇的性质
(1)取代反应
A.与金属钠反应
化学方程式:
化学键断裂位置:
对比实验:乙醇和Na反应现象:
水和钠反应现象:
乙醚和钠反应:无明显现象
结论:①
②
B.与HX反应
化学方程式:
断键位置:
实验(教材P68页)
现象:
实验注意:烧杯中加入自来水的作用:
C.乙醇的分子间脱水
化学方程式:
化学键断裂位置:
〖思考〗甲醇和乙醇的混合物与浓硫酸共热生成醚的种类分别为

 D.酯化反应
D.酯化反应
 化学方程式:
化学方程式:
断键位置:
(2)消去反应
化学方程式:
断键位置:
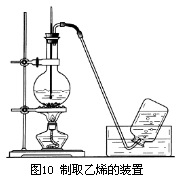
实验装置:(如图)
注:乙醇的消去反应和卤代烃的消去反应类似,都属于β-消去,即羟基的β碳原子上必须有H原子才能发生该反应
(3)氧化反应
 A.燃烧
A.燃烧
CH3CH2OH + 3O2
CxHyOz + O2
[思考]某饱和一元醇与氧气的混合气体,经点燃后恰好完全燃烧,反应后混合气体的密度比反应前减小了1/5,求此醇的化学式(气体体积在105℃时测定)
B.催化氧化
化学方程式:
断键位置:
说明:醇的催化氧化是羟基上的H与α-H脱去
[思考]下列饱和一元醇能否发生催化氧化,若能发生,写出产物的结构简式


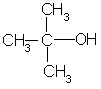
A B C
结论:伯醇催化氧化变成
仲醇催化氧化变成
叔醇
C.与强氧化剂反应
乙醇能使酸性KMnO4溶液褪色
三、其它常见的醇
(1)甲醇
结构简式:
物理性质:甲醇俗称木精,能与水任意比互溶,有毒,饮用10毫升就能使眼睛失明,再多用就有使人死亡的危险,故需注意。
化学性质:请写出甲醇和金属Na反应以及催化氧化的化学方程式
(2)乙二醇
物理性质:乙二醇是一种 的液体,主要用来生产聚酯纤维。乙二醇的水溶液凝固点很低,可作汽车发动机的 。
化学性质:写出乙二醇与金属钠反应的化学方程式
(3)丙三醇(甘油)
丙三醇俗称 ,是无色粘稠,有甜味的液体,吸湿性强,有护肤作用,是重要的化工原料。
结构简式:
化学性质:
A.与金属钠反应:
B.与硝酸反应制备硝化甘油
一、酚的结构与物理性质
①苯酚俗称 分子式为 结构简式 官能团名称
酚类的结构特点
②苯酚的物理性质
(1)常温下,纯净的苯酚是一种 色晶体,从试剂瓶中取出的苯酚往往会因部分氧化而略带 色,熔点为:40.9℃
(2)溶解性:常温下苯酚在水中的溶解度 ,会与水形成浊液;当温度高于65℃时,苯酚能与水 。苯酚易溶于酒精、苯等有机溶剂
(3)毒性:苯酚有毒。苯酚的浓溶液对皮肤有强烈的腐蚀作用,如不慎将苯酚沾到皮肤上,应立即用 清洗,再用水冲洗。
二、酚的化学性质
(1)弱酸性:由于苯环对羟基的影响,使苯酚中的羟基能发生微弱电离,所以苯酚能够与NaOH溶液反应:
A.与NaOH溶液的反应
所以向苯酚的浊液中加入NaOH溶液后,溶液变 。
苯酚的酸性极弱,它的酸性比碳酸还要 ,以致于苯酚 使紫色石蕊试剂变红。
B.苯酚的制备(强酸制弱酸)
注意:产物是苯酚和碳酸氢钠,这是由于酸性:H2CO3 > 苯酚 > HCO3-
(2)苯酚的溴化反应
苯酚与溴水在常温下反应,立刻生成白色沉淀2,4,6-三溴苯酚
该反应可以用来
(3)显色反应:酚类化合物与Fe3+ 显 色,该反应可以用来检验酚类化合物。
三、废水中酚类化合物的处理
(1)酚类化合物一般都有毒,其中以甲酚(C7H8O)的污染最严重,含酚废水可以用
吸附或苯等有机溶剂 的方法处理。
(2)苯酚和有机溶剂的分离
苯酚和苯的分离:
四、基团间的相互影响
(1)酚羟基对苯环的影响
酚羟基的存在,有利于苯环上的取代反应,例如溴代反应。
苯的溴代:
苯酚的溴代:
从反应条件和产物上来看,苯的溴代需要在催化剂作用下,使苯和与液溴较慢反应,而且产物只是一取代物;而苯酚溴代无需催化剂,在常温下就能与溴水迅速反应生成三溴苯酚。足以证明酚羟基对苯环的活化作用,尤其是能使酚羟基邻、对位的氢原子更活泼,更易被取代,因此酚羟基是一种邻、对位定位基
邻、对位定位基:-NH2、-OH、-CH3(烷烃基)、-X
其中只有卤素原子是钝化苯环的,其它邻对位定位基都是活化苯环的基团。
间位定位基:-NO2、-COOH、-CHO、间位定位基都是钝化苯环的基团
(2) 苯环对羟基的影响

通过上面的对比,可以看出苯环的存在同样对羟基也有影响,它能使羟基上的氢更容易电离,从而显示出一定的弱酸性。
五、苯酚的用途
苯酚是重要的 原料,其制取得到的酚醛树脂俗称 ;苯酚具有
 ,因此药皂中掺入少量的苯酚,葡萄中含有的酚可用于制造 茶叶中的酚用于制造 另外一些农药中也含有酚类物质。
,因此药皂中掺入少量的苯酚,葡萄中含有的酚可用于制造 茶叶中的酚用于制造 另外一些农药中也含有酚类物质。
醛学案
一、乙醛
1.组成与结构
乙醛的分子式 结构简式 官能团 。
2.物理性质
乙醛是 色、具有 气味的液体,密度小于水,沸点为20.8℃。乙醛易挥发,能与水、乙醇、氯仿等互溶。
3.化学性质
(1)加成反应(醛基中的 能够发生加成反应)
还原反应:在有机化学反应中,常把有机物分子中得 或失 的反应。
(2)氧化反应:
①可燃性:
②催化氧化(在醛基中的碳氢之间插入 )
氧化反应:在有机化学反应中,通常把有机物分子中得 或失 的反应。
③被弱氧化剂氧化
银镜反应原理: 。
与新制氢氧化铜的反应原理: 。
二、醛类
1.概念:分子里由烃基与 基相连构成的化合物。
2.饱和一元醛的通式
3.醛类的化学通性:
(1)催化加氢:RCHO十H2  (还原反应)
(还原反应)
也属于加成反应(主要表现在与氢气的催化加成上,亦称为还原反应)
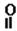 (催化剂常用金属镍)
(催化剂常用金属镍)
【思考】 若已知含羰基(—C—)类的有机物也能发生类似的加成反应,
试写出:① 丙酮与氢气:
② 2—甲基丁醛与氢气:
(2)氧化反应
①催化氧化:RCHO+O2 
②银镜反应:RCHO+  + + +
+ + +
③新制氢氧化铜悬浊液的反应:RCHO+  + +
+ +
4.甲醛
(1)结构特点:甲醛的分子式 ,结构简式 ,结构式 。
(2)物理性质:甲醛又叫蚁醛是一种无色具有强烈刺激性气味的 体,易溶于水。含35%~40%的甲醛水溶液叫 。甲醛 毒,装饰材料释放出的气体中含有甲醛,要注意安全及环境保护。
5.醇、醛、羧酸的相互关系。
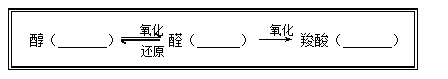
羧酸 酯
一、乙酸
1.结构:分子式:___;结构式:_____; 结构简式:_____。官能团是_____。
2.物理性质:
乙酸俗称 ,它是一种无色 气味的 体,易挥发,熔、沸点较 ,其熔点为16.6℃时,因此当温度低于16.6℃时,乙酸就凝成像冰一样的晶体,故无水乙酸又称 。它易溶于水和乙醚等溶剂。
⒊化学性质:
⑴酸性:电离方程式:
 写出有关反应的离子方程式:
写出有关反应的离子方程式:
A:与大理石反应:
 B:与小苏打溶液反应:
B:与小苏打溶液反应:
 C: 设计一个简单的一次性完成的实验装置,验证乙酸、碳酸和苯酚溶液的酸性强弱。
C: 设计一个简单的一次性完成的实验装置,验证乙酸、碳酸和苯酚溶液的酸性强弱。
⑵酯化反应:CH3COOH+C2H5OH CH3COO C2H5+H2O
CH3COO C2H5+H2O
①试剂加入顺序:
②加热目的:
③饱和Na2CO3的作用:
④现象:
⑤注意事项:
A、化学原理:浓硫酸起催化脱水作用。
B、装置:液-液反应装置。用烧瓶或试管。试管倾斜成45°(使试管受热面积大)。弯导管起冷凝回流作用。导气管不能伸入饱和Na2CO3溶液中(防止Na2CO3溶液倒流入反应装置中)。
C、饱和Na2CO3溶液的作用。①.乙酸乙酯在饱和Na2CO3溶液中的溶解度较小,减小溶解,利于分层。②挥发出的乙酸与Na2CO3反应,除掉乙酸;挥发出的乙醇被Na2CO3溶液吸收。避免乙酸特殊气味干扰乙酸乙酯的气味。
二、羧酸
⑴定义:由烃基或H与羧基相连的一类化合物,官能团为 —COOH
⑵分类:
 C原子数目:低级,高级脂肪酸
C原子数目:低级,高级脂肪酸
 脂肪酸
脂肪酸
 烃基种类 烃基的饱和情况:饱和,不饱和
烃基种类 烃基的饱和情况:饱和,不饱和
 芳香酸
芳香酸
 一元羧酸
一元羧酸
羧基数目
多元羧酸
w.w.w.k.s.5.u.c.o.m
⑶饱和一元羧酸:CnH2nO2
①酸CnH2nO2的同分异构体的数目:看R-COOH中-R的异构体数目
②与C数相同的饱和一元酯异构
⑷物性:①熔沸点:随n↑而升高
②溶解性:随n↑而减小(低级脂肪酸易溶,高级脂肪酸不溶)
(5)甲酸:俗称蚁酸,结构式 结构简式 ,所以甲酸即具有酸的性质又具有醛的性质。甲酸被氧化成碳酸。在碱性条件下,甲酸可发生银镜反应,可跟新制氢氧化铜作用析出氧化亚铜红色沉淀,可是酸性高锰酸钾和溴水退色。
三、酯
⒈定义:酸( 、 )与醇发生酯化反应生成的一类有机化合物。
举例:CH3COOC2H5、C2H5ONO2、硝化甘油、油脂(脂肪、油)、涤纶树脂、有机玻璃
苹果、菠萝、香蕉中的香味物质
⒉组成、结构、通式
有机酸酯的结构通式: 官能团:
饱和一元酯:CnH2nO2 (n≥2)
3.命名:某酸某酯 写出下列物质的结构简式:
乙二酸二乙酯、乙二酸乙二酯、二乙酸乙二酯、乙二酸乙二酯
w.w.w.k.s.5.u.c.o.m
4.物性:⑴低级酯具有芳香气味,可作香料;
⑵一般是比水 , 溶于水的中性油状液体,可作有机溶剂。
5.化性:水解反应
① 水解条件:
水解方程式:
③与酯化反应的关系:互为可逆反应
RCOOH+HO—R’ RCOOR’+ H2O
RCOOR’+ H2O
思考:分析酯化反应正向和逆向进行的措施。
 w.w.w.k.s.5.u.c.o.mw.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.mw.w.w.k.s.5.u.c.o.m
6.特殊的酯——甲酸酯:HCOOR
①水解;②氧化反应:能被银氨溶液、新制Cu(OH)2碱性浊液氧化成HOCOOR(碳酸酯)(酯中只有甲酸酯才能发生银镜反应)
有机合成
1、有机合成遵循的原则
(1)起始原料要价廉、易得、简单,通常采用四个碳以下的单官能团化合物和单取代苯。
(2)尽量选择步骤最少的合成路线。
(3)“绿色、环保”。
(4)操作简单、条件温和、能耗低,易于实现。
(5)不能臆造不存在的反应事实。
2、有机合成的解题方法
首先要看目标产物属于哪一类、带有何种官能团。
然后结合所学过的知识或题给信息,寻找官能团的引入、转换、保护或消去的方法。
3、解答有机合成题的关键在于:(1)选择合理简单的合成路线。
(2)熟练各类物质的组成、结构、性质、相互衍生关系以及官能团的引进和消去等知识。
二、有机物的种类、官能团之间的转换
1、官能团的引入
(1)引入羟基(—OH):烯烃与水加成,卤代烃水解,酯的水解,醛、酮与H2加成还原等。
(2)引入卤原子(—X):烃的取代,不饱和烃与X2、HX的加成,醇或酚与HX的取代等。
(3)引入C=C:卤代烃消去 醇消去 炔烃不完全加成。
(4)引入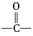 :醇的催化氧化
:醇的催化氧化
2、官能团的消除
(1)通过加成消除不饱和键。
(2)通过加成(加H)或氧化(加O)消除醛基。
(3)通过消去或氧化或酯化等消去羟基。
3、官能团的衍变
(1)利用衍生关系引入官能团,如醇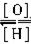 醛
醛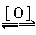 羧酸
羧酸
(2)通过化学反应增加官能团
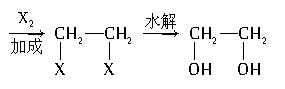
CH2=CH2
如C2H5OH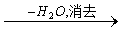 CH2==CH2
CH2==CH2
(3)通过某种手段,改变官能团位置
如:CH3CH2CH2OH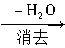 CH3CH==CH2
CH3CH==CH2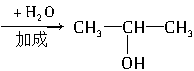
4、各类官能团之间的互换和变化,一般来说有以下几种情况
(1)相互取代关系:如卤代烃与醇的关系,R—X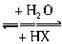 R—OH (—X与—OH之间的取代)。
R—OH (—X与—OH之间的取代)。
(2)氧化还原关系:如醇与醛、酸之间的转化,—CH2—OH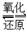 —CHO
—CHO —COOH
—COOH
(3)消去加成关系:如①R—OH与浓硫酸共热170 ℃消去反应生成C=C和水,而C=C在催化剂、加热、加压条件下与水发生加成反应生成R—OH。
②:R—X在NaOH的醇溶液中消去成C=C、和HX,而C=C在催化加热下与HX加成为R—X
(4)结合重组关系:如醇与羧酸的酯化与酯的水解RCOOH+R′—OH R—COOR′+H2O。
R—COOR′+H2O。
5、碳骨架的增减
①增长:有机合成题中碳链的增长,一般会以信息形式给出。
②变短:如烃的裂化、裂解,某些烃的氧化。
三、有机合成题的解题方法
(1)顺合成法:其思维程序是:原料→中间产物→产品。
▲(2)逆合成法:此法是采用逆向思维方法,从产品的组成、结构、性质入手,找出合成所需要的直接或间接的中间产物,逐步推向已知原料,其思维程序是:

(3)综合比较法:此法是采用综合思维的方法,将正向或逆向推导出的几种合成途径进行比较,从而得到最佳的合成路线。
四、相关链接
1.有机反应类型及相应有机物种类
(1)取代反应:烷烃(卤代),苯及其同系物(卤代、硝化、磺化),醇(卤代),苯酚(溴代)。
(2)加成反应:烯烃(X2、H2、HX、H2O),炔烃(X2、H2、HX),苯(H2),醛(H2),油脂(C=C氢化)。
(3)消去反应:卤代烃脱HX,醇分子内脱H2O。
(4)酯化反应:醇和羧酸,纤维素和酸,甘油和酸,醇和无机含氧酸。
(5)水解反应:卤代烃,酯、油脂,二糖和多糖,蛋白质。
(6)氧化反应:烯、炔、烷基苯、醇、醛等。
(7)还原反应:醛、葡萄糖与H2加成。
(8)加聚反应:乙烯、异戊二烯、氯乙烯等。
(9)缩聚反应:苯酚和甲醛等。
2.重要的有机反应规律
(1)双键的加成和加聚:双键之一断裂,加上其他原子或原子团或断开键相互连成链。
(2)醇的消去反应:消去和羟基所在C相邻的C上的H,若相邻的C上无H则不能发生消去。
(3)醇的催化氧化反应:和羟基相连的C上若有H则可被氧化为醛或酮,若无H则不能被氧化。
(4)有机物成环反应:a.二元醇脱水,b.羟酸的分子内或分子间酯化,c.氨基酸脱水,d.二元羧酸脱水,e.以上化合物之间的脱水或酯化。
五、拓展迁移
1、碳链的增长或缩短
(1)增长:有机物与HCN加成;单体通过加聚或缩聚等。
如CH3CH2Br CH3CH2CN
CH3CH2CN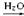 CH3CH2COOH。
CH3CH2COOH。
(2)减少:烃的裂化或裂解,脱羧反应(如制CH4),苯的同系物的氧化,烯烃的氧化等。
2、原子经济性
最大限度地利用原料分子的每一个原子,使反应达到零排放。原子经济性可以用原子利用率来衡量。原子的利用率越高,原子经济性越强。
原子利用率= ×100%
×100%
