物理化学实验报告
(20##------20##学年第二学期)
班 级
学 号
姓 名
年 月 日
燃烧热的测定
一、目的与要求
1.用氧弹热量计测定奈的燃烧热,了解并掌握热量计的构造、原理和使用方法;
2.明确燃烧热的定义,了解恒压燃烧热与恒容燃烧热的差别及相互关系;
3.学会用雷诺图解法校正温度改变值。
二、实验原理(绘制装置图)
在恒容条件下测得的燃烧热称为恒容燃烧热(Qv), 其值等于这个过程的内能变化(ΔU)
Qv = – MCVΔT/m
在恒压条件下测得的燃烧热称为恒压燃烧热(Qp),其值等于这个过程的热焓变化(ΔH)
Qp = Q + ΔnRT 在略去体系与环境的热交换的前提下,体系的热平衡关系为
Qv = –M[(WC水+ C体系)ΔT–QaLa]/m (1)
令 k = WC水+ C体系,则
则Qv = – M( kΔT – QaLa)/M (2)
其中:M为燃烧物质的摩尔质量;m为燃烧物质的质量;Qv 为物质的定容燃烧热; ΔT为燃烧反应前后体系的真实差;W为水的质量;C水为水的比热容;C体系为量热计的水氧弹,水桶,贝克曼温度计,搅拌器的热容;Qa为点火丝;La为点火丝长度。
在已知苯甲酸燃烧热值的情况下,我们通过实验可测出k的大小,用同样的方法我们就可以测出萘的燃烧热值Qv 。
三、实验步骤
1.样品处理:分别称取苯甲酸0.6g, 萘0.4g。压片后精确称量,并置于坩埚中。
2.氧弹内安装:置氧弹盖于氧弹支架上,取已知质量的点火丝固定在两电极间,并是点火丝与坩埚中样品接触,盖上氧弹盖,一定要上紧弹盖。
3.氧弹充气:将充氧器阀口接在氧弹顶进气阀上,按下充气手柄(一定要按紧,使充氧器阀口紧紧扣住进气阀)。
4.总装:首先开启控制器电源,向桶内注入2.7kg水,再放置氧弹于其中,之后盖好量热计盖并插入热电阻温度计。
5.测量工作
(1)开启搅拌器,搅拌3分钟,使体系达温度平衡,按[恢复]键,使计数时间归零。
(2)前期测量:每半分读取温度一次,共10次之后快速同时按[点火]及[复位]键。
(3)主期测量:接上测量,每半分读取温度一次,直至温度开始下降。
(4)末期测量:按下[复位]键,接上测量,每半分读取温度一次,共10次。
(5)清理工作:取出氧弹,用放气阀压于氧弹顶上,下压放气;打开氧弹取出未燃烧的燃烧丝量取其长度;清洗整理仪器。
四、数据记录及处理
1.原始数据黏贴处
2. 雷诺曲线(用坐标纸绘制)
3.数据处理与误差分析
二组分固-液相图的绘制
一、实验目的及要求
1.用热分析法测绘Sn-Bi二元合金相图;
2.掌握热分析法的测量技术。
二、实验原理(绘制装置图)
用来表示多相体系的温度、压力与体系中各组分的状态、组成之间关系的平面图形称为相图。二组分固-液相图是描述体系温度与二组分组成之间关系的图形。由于固液相变体系属凝聚体系,一般视为不受压力影响,因此在绘制相图时不考虑压力因素。
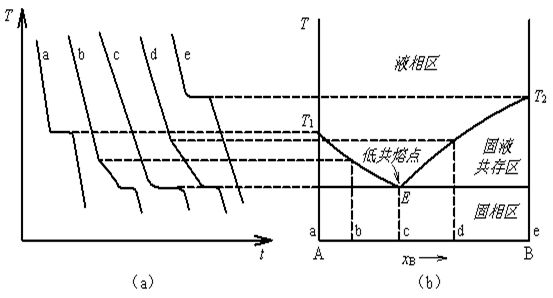
若二组分体系的两个组分在固相完全不溶,在液相可完全互溶,一般具有简单低共熔点,其相图具有比较简单的形式。根据相律,对于具有简单低共熔点的二组分体系,其相图可分为三个区域,即液相区、固液共存区和固相区。绘制相图时,根据不同组成样品的相变温度(即凝固点)绘制出这三个区域的交界线—液相线,即图1(b)中的T1E和T2E,并找出低共熔点E所处的温度和液相组成。
步冷曲线法又称热分析法,是绘制相图的基本方法之一。它是将某种组成的样品加热至全部熔融,再均速冷却,测定冷却过程中样品的温度 – 时间关系,即步冷曲线。根据步冷曲线上的温度转折点获得该组成的相变点温度。
步冷曲线有三种形式,分别如图1(a)中的a、b和c三条曲线。a曲线是纯物质A的步冷曲线。在冷却过程中,当体系温度到达A物质凝固点时,开始析出固体,所释放的熔化热抵消了体系的散热,使步冷曲线上出现一个平台,平台的温度即为A物质的凝固点。纯B步冷曲线e的形状与此相似。
三、实验步骤
1.将装有样品的坩埚放在电炉加热,待样品全部溶化后,将温度计插入样品中继续加热至高于所测温度20℃;
2.从电路上将坩埚取下,待温度下降至所测温度上线开始计时,且每隔0.5min测读一次温度,直至所测温度下线;
3.根据所测数据绘制步冷曲线和金属相图。
4.温度测定范围:
100%锡和100%铋:350~200℃, 70%锡:300℃~120℃, 42%锡:200℃~120℃
四、数据记录及处理
1.原始数据黏贴
2.利用所得数据绘制步冷曲线和Bi─Sn二组分体系的相图,并注出相图中各区域的相平衡,从相图上找出Bi─Sn系统的低共熔温度和低共熔点混合物的组成。(用坐标纸绘制)
液体饱和蒸气压的测定
【目的要求】
1.明确纯液体饱和蒸汽压的定义和气液平衡的概念,理解纯液体饱和蒸汽压与温度的关系。
2.用静态法测定不同温度下环己烷的饱和蒸汽压。
3.学会用图解法求被测液体在实验温度范围内的平均摩尔汽化热与正常沸点。
【实验原理】
液体的饱和蒸气压与温度的关系用克劳修斯-克拉贝龙方程式表示:
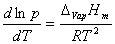
式中P为纯液体在温度T时的饱和蒸汽压,T为热力学温度,ΔHm为液体的摩尔汽化热,R为气体常数。如果温度变化范围不大,ΔHm可视为常数,当做平均摩尔汽化热,将上式积分得:
 ㏒P=-
㏒P=-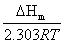 +A
+A
式中A为积分常数,故上式可知,在一定范围内,测定不同温度下的饱和蒸汽压,以㏒P
对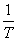 作图,可得一直线,而由直线的斜率可以求出是温度范围的液体平均摩尔汽化热
作图,可得一直线,而由直线的斜率可以求出是温度范围的液体平均摩尔汽化热
ΔHm。
【仪器试剂】
蒸汽压测定装置 1套 电加热器 1只
真空泵 1台 温度计(0.1℃及1℃) 各1只
沸庭式气压计 1支 烧杯(3000ml) 1个
磁力搅拌器 1台 环己烷(A.R.)
【实验步骤】
1.装样 将等压计洗净烘干,然后烘烤A管,把内部空气赶出,迅速将液体从C管的管口灌入,冷却A管,液体即被吸入,反复几次,使液体灌至A管高度的三分之一处,而B,C管各装有二分之一为宜,最后接在装置上。
2.检查气密性
关闭通大气活塞,开动真空泵,慢慢打开通真空泵活塞抽气,使体系内压力减小500mmHg左右,关闭活塞同真空泵活塞及真空泵,注意观察U型压力计读书在数分钟内有无变化,若有变化说明漏气,经仔细检查各接口直到不漏气为止。
3.在沸庭式气压计上读取外界大气压值。
4.排空气
打开通大气活塞使系统与大气相通,接通冷却水,打开搅拌机,并对水浴进行加热,随着温度的上升,C管中有气泡溢出,说明A、B管中空气被排出。继续加热直至85℃,保持温度数分钟,以赶净A、B之间的空气。
5测定大气压下的沸点
等压计中空气赶后,停止加热,片刻之后,温度开始下降,C管中气泡逐渐减少并消失,C管液面下降而B管液面上升,这事要密切注意两液面,一旦达到同一水平面,立刻记下此时的温度,重新加热到85℃,等压计液体重又沸腾,停止加热,在进行测定,重复测定2次,取平均值。
6.测定不同温度下纯液体蒸汽压
在最后一次测定大气压的沸点完毕后,迅速关闭通大气活塞,开动真空泵,缓慢打开通真空泵活塞对系统进行减压,同时观察等压计,是C管液面高于B管液面5cm左右,然后关闭通真空泵活塞及真空泵。此时液体重又沸腾,有气泡逸出,等待片刻,气泡消失,当两管液面相平时,迅速记下温度,然后从U形压力计上读取左右水银柱的高度值,然后立即开动真空泵再次减压,读数要快要准,不间断连续进行测定,共测定15组数据,停止实验,打开通大气活塞,关闭仪器,
【数据处理】
1.原始数据粘贴处
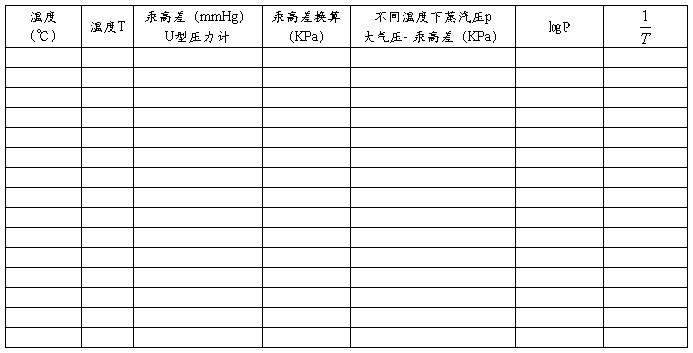
2.数据处理表
大气压值: KPa 大气压下的沸点: ℃
3.由以上数据以㏒P对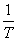 作图,并求直线斜率,由斜率计算被测液在实验温度区间内的平均摩尔汽化热,并与文献值比较。
作图,并求直线斜率,由斜率计算被测液在实验温度区间内的平均摩尔汽化热,并与文献值比较。
4由P—T曲线求待测液体的正常沸点。
文献值:ΔHm=32.76KJ.mol-1 T沸=80.74℃
电导法测定乙酸乙酯皂化反应速率常数
【目的要求】
1.了解测定化学反应速率常熟的一中物理方法—电导法,了解反应活化能的测定方法。
2.了解二级反应的特点,学会用图解法求二级反应的速率常数。
3.掌握DDS-11A型数字电导率仪和控温仪的使用方法。
【实验原理】
对于二级反应:A+B→产物
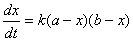 (a-1)
(a-1)
式中a、b分别为反应开始时A、B的温度,x为反应进行到t时产物的浓度,k就是要测定的反应速率常数。
如果A、B两物质起始浓度相同均为a反应速率表示式为:
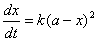 (a-2)
(a-2)
上式积分得: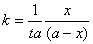 (a-3)
(a-3)
以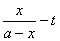 作图所得直线,证明是二级反应,并可以从直线的斜率求出k。
作图所得直线,证明是二级反应,并可以从直线的斜率求出k。
所以在反应进行中,只要能够测出反应物或产物的浓度,即可求得该反应的速率常数。
如果知道不同温度下的速率常数k(T1)和k(T2),按Arrhenius公式计算出该反应的活化能E
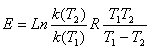 (a-4)
(a-4)
乙酸乙酯皂化反应是二级反应,其反应式为:
CH3COOC2H5+Na++OH-→CH3COO-+Na++C2H5OH
如果乙酸乙酯皂化在稀溶液中反应,应存在如下关系式:
k0=A1a (a-5)
k∞= A2a (a-6)
kt= A1(a-x)+A2x (a-7)
A1 、A2是与温度、电解质性质、溶剂等因素有关的比例常数,k0, k∞分别为反应开始和终了时溶液的总电导率。kt为时间t是溶液的总功率,由(a-5)、(a-6)、(a-7)三式可得
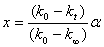 代入(10-3)得
代入(10-3)得 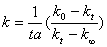 (a-8)
(a-8)
重新排列整理得: 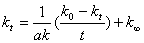
因此,以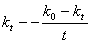 作图为一直线即为二级反应,其斜率等于
作图为一直线即为二级反应,其斜率等于 (a为浓度)
(a为浓度)
【仪器试剂】
玻璃恒温槽水浴 1套 电导率仪 1台
电导电极 1支 皂化管 1支
秒表 1块, 移液管(10ml) 2支
0.02 mol?L-1NaOH溶液 0.02mol?L-1CH3COOC2H5溶液
0.01 mol?L-1CH3COONa溶液.
【实验步骤】
1、调节恒温槽温度至25℃。
2、将20ml配好的0.01 mol?L-1的NaOH溶液置于锥形瓶中在恒温槽中恒温10分钟,然后测其电导,取三次测量的平均值,此值即为G0值。
3、将20ml 0.01 mol?L-1CH3COONa溶液置于锥形瓶中在恒温槽中恒温10分钟,后测其电导,取三次测量的平均值,此值即为G∞值。
4、用移液管分别取10ml 0.02 mol?L-1NaOH溶液和10ml 0.02mol?L-1CH3COOC2H5溶液,缓慢注入皂化管的两边(不要混合!),恒温10分钟后,推动针筒使两种溶液混合均匀,当一种溶液推过去一半时开始计时,每2分钟测一次Gt值,反应45分钟后停止。
5、调节恒温槽温度至35℃,重复上述2、3、4步骤。
【数据处理】
1.原始数据粘贴处
2.数据处理表
K0= us/cm
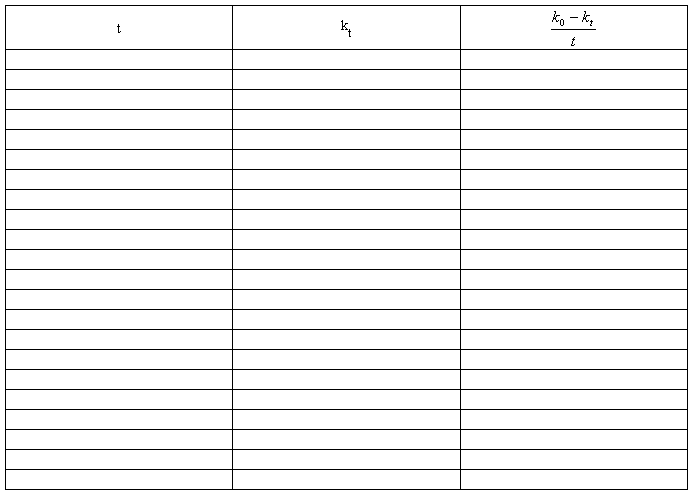
3图像粘贴处
4由直线斜率计算反应速率常数
粘度法测定高聚物相对分子量
【目的要求】
1.测定多糖聚合物-右旋糖酐的平均相对分子质量。
2.掌握用乌贝路德粘度计测定粘度的原理和方法。
【实验原理】
高聚物在稀溶液中的粘度,主要反映了液体在流动时存在着内摩擦,其中溶剂分子之间的内摩擦表现出来的粘度叫纯溶剂粘度,记作η0,;此外还有高聚物分子相互之间的内摩擦,以及高分子与溶剂分子之间的内摩擦。三者之和表现为溶液的粘度η,在同一温度下,一般来说,η>η0,相对于溶剂,其溶液粘度增加的分数,称为增比粘度,记作ηsp,
即ηsp= (a-3)
(a-3)
而溶液粘度与纯溶剂粘度的比值称为相对粘度,记作ηr,即
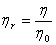 (a-4)
(a-4)
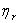 也是整个溶液的粘度行为,ηsp则意味着已扣除了溶剂分子之间的内摩擦效应,两者关系为
也是整个溶液的粘度行为,ηsp则意味着已扣除了溶剂分子之间的内摩擦效应,两者关系为 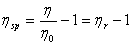 (a-5)
(a-5)
对于高分子溶液,增比粘度ηsp往往随溶液的浓度c的增加而增加,为了便于比较,将单位浓度下所显示出的增比粘度,即ηsp/c称为比浓粘度;㏑ηr/c称为比浓粘度。
为了进一步消除高聚物分子之间的内摩擦效应,必须将溶液浓度无限稀释,使得每个高聚物分子彼此相隔极远,其相互干扰可忽略不计,这时溶液所呈现的粘度行为基本上反映了高分子与溶剂分子之间的内摩擦。这一粘度的极限值记为:
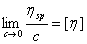 (a-6)
(a-6)
[η]被称为特性粘度,其值与浓度无关,实验证明,当聚合物、溶剂和温度确定以后,[η]数值只与高聚物平均相对分子质量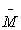 有关,它们之间的半经验关系可用Mark Houwink方程式表示:
有关,它们之间的半经验关系可用Mark Houwink方程式表示:
[η]=K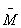 a (a-7)
a (a-7)
式中K为比例常数,a是与分子形状有关的经验常数,它们都与温度、聚合物、溶剂性质有关,在一定的相对分子质量范围内与相对分子质量无关。
通过测定溶液和溶剂的流出时间t和t0,就可算出ηr:
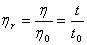 (a-10)
(a-10)
【仪器试剂】
恒温水浴 1套 乌氏粘度计 1支
秒表 1块 10ml移液管 2支
【实验步骤】
1、调节恒温槽温度至25℃。
2、配制3%右旋糖酐溶液。
3、将粘度计洗净烘干,并按教材要求安装粘度计。
4、分别测定5种不同浓度溶液的流出时间各三次,取平均值。
5、测定溶剂(重蒸馏水)的流出时间t0三次(每次相差不超过0.2秒),取平均值。
【实验注意事项】
1、安装粘度计要垂直,应远离加热器和搅拌器,注意防止灰尘、纤维、油污等堵塞毛细管。
2、粘度计安装前必须用洗液和重蒸馏水洗净烘干。
3、测定时恒温槽搅拌器停止搅拌以防震动。
4、每次改变浓度后一定要混合均匀,抽吸溶液时注意控制抽吸速度,不要在毛细管内形成气泡。
5、实验结束后要彻底洗净粘度计,放置烘箱烘干。
【数据处理】
1.原始数据粘贴处
2.数据处理表
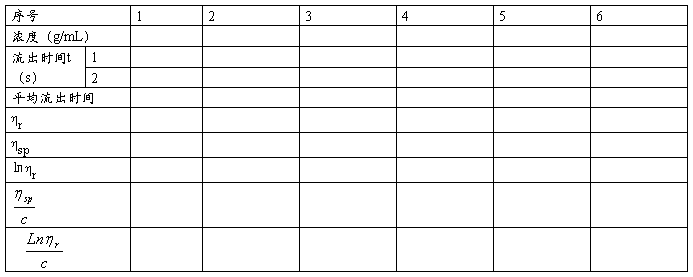
3图像粘贴处
以
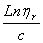 ~c及
~c及 ~c在同一坐标纸上作图。并外推c→0求得截距即得[η]。
~c在同一坐标纸上作图。并外推c→0求得截距即得[η]。
4计算聚乙烯醇的粘均相对分子量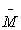 。25℃时,右旋糖酐水溶液的参数K=9.22×10-2cm3/g-1,a=o.5
。25℃时,右旋糖酐水溶液的参数K=9.22×10-2cm3/g-1,a=o.5
第二篇:长安大学C语言-数组实验报告

学生实验报告
实验课名称: C语言
实验项目名称:
专业名称:
班级:
学号:
学生姓名:
教师姓名:
2011 年 03 月 31 日
实验日期:2011 年 03 月 31 日 实验室名称: WM 2303



