分析化学(第六版)总结
第二章 误差和分析数据处理
第一节 误差
定量分析中的误差就其来源和性质的不同,可分为系统误差、偶然误差和过失误差。
一、系统误差
定义:由于某种确定的原因引起的误差,也称可测误差
特点:①重现性,②单向性,③可测性(大小成比例或基本恒定)
分类:
1. 方法误差: 由于不适当的实验设计或所选方法不恰当所引起。
2. 仪器误差: 由于仪器未经校准或有缺陷所引起。
3. 试剂误差: 试剂变质失效或杂质超标等不合格 所引起
4. 操作误差: 分析者的习惯性操作与正确操作有一定差异所引起。
操作误差与操作过失引起的误差是不同的。
二、偶然误差
定义:由一些不确定的偶然原因所引起的误差,也叫随机误差. 偶然误差的出现服从统计规律,呈正态分布。
特点:
①随机性(单次)
②大小相等的正负误差出现的机会相等。
③小误差出现的机会多,大误差出现的机会少。
三、过失误差
1、过失误差:由于操作人员粗心大意、过度疲劳、精神不集中等引起的。其表现是出现离群值或异常值。
2、过失误差的判断——离群值的舍弃
a) 在重复多次测试时,常会发现某一数据与平均值的偏差大于其他所有数据,这在统计学上称为离群值或异常值。
b) 离群值的取舍问题,实质上就是在不知情的情况下,区别两种性质不同的偶然误差和过失误差。
离群值的检验方法:
(1)Q 检验法:该方法计算简单,但有时欠准确。
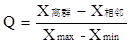 设有n个数据,其递增的顺序为x1,x2,…,xn-1,xn,其中x1或xn可能为离群值。
设有n个数据,其递增的顺序为x1,x2,…,xn-1,xn,其中x1或xn可能为离群值。
当测量数据不多(n=3~10)时,其Q的定义为
具体检验步骤是:
1) 将各数据按递增顺序排列;2)计算最大值与最小值之差;3)计算离群值与相邻值之差;
4) 计算Q值;5)根据测定次数和要求的置信度,查表得到Q表值;6)若Q >Q表,则舍去可疑值,否则应保留。
该方法计算简单,但有时欠准确。
(2)G检验法:该方法计算较复杂,但比较准确。
具体检验步骤是:
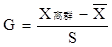
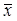 1)计算包括离群值在内的测定平均值
1)计算包括离群值在内的测定平均值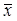 ;2)计算离群值与平均值 之差的绝对值
;2)计算离群值与平均值 之差的绝对值
3)计算包括离群值在内的标准偏差S4)计算G值。
5)若G > Gα,n ,则舍去可疑值,否则应保留
第二节 测量值的准确度和精密度
一、准确度与误差
1.准确度:指测量结果与真值的接近程度,反映了测量的正确性,越接近准确度越高。系统误差影响分析结果的准确度 。
2.误差:准确度的高低可用误差来表示。误差有绝对误差和相对
 误差之分。
误差之分。
 (1)绝对误差:测量值x与真实值μ之差
(1)绝对误差:测量值x与真实值μ之差
(2)相对误差:绝对误差占真实值的百分比
3.真值与标准参考物质
任何测量都存在误差,绝对真值是不可能得到的,我们常用的真值是
1) 理论真值:如三角形的内角和为180°等。
2) 约定真值:由国际权威机构国际计量大会定义的单位、数值,如 时间、长度、原子 量、物质的量等,是全球通用的
3) 相对真值:由某一行业或领域内的权威机构严格按标准方法获得的测量值,如卫生部药品检定所派发的标准参考物质,应用范围有一定的局限性。
4) 标准参考物质:具有相对真值的物质,也称为标准品,标样,对照品。应有很好的均匀性和稳定性,其含量测量的准确度至少要高于实际测量的3倍。
二、精密度与偏差
1.精密度:平行测量值之间的相互接近程度,反映了测量的重现性,越接近精密度越高。偶然误差影响分析结果的精密度,
2.偏差精密度的高低可用偏差来表示。
 偏差的表示方法有
偏差的表示方法有
(1)绝对偏差 :单次测量值与平均值之差:
 (2)平均偏差:绝对偏差绝对值的平均值
(2)平均偏差:绝对偏差绝对值的平均值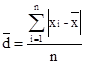
(3)相对平均偏差:平均偏差占平均值的百分比:

 (4)标准偏差
(4)标准偏差
(5)相对标准偏差(RSD, 又称变异系数CV )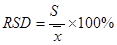
 (必考相关大题)例:用邻二氮菲显色法测定水中铁的含量,结果为10.48, 10.37, 10.47, 10.43, 10.40 mg/L; 计算单次分析结果的平均偏差,相对平均偏差,标准偏差、相对标准偏差和置信区间(95%和99%)。(相关题目,此题做不成)
(必考相关大题)例:用邻二氮菲显色法测定水中铁的含量,结果为10.48, 10.37, 10.47, 10.43, 10.40 mg/L; 计算单次分析结果的平均偏差,相对平均偏差,标准偏差、相对标准偏差和置信区间(95%和99%)。(相关题目,此题做不成)
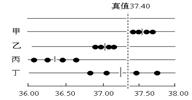 三、准确度与精密度的关系
三、准确度与精密度的关系
1. 准确度高,一定要精密度好
2. 精密度好,不一定准确度高。只有在消除了系统误差的前提下,精密度好,准确度才会高
四、误差的传递:误差的传递分为系统误差的传递和偶然误差的传递。
1.系统误差的传递
①和、差的绝对误差等于各测量值绝对误差的和、差
R = x + y -z δR=δx+δy-δz
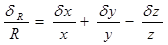 ②积、商的相对误差等于各测量值相对误差的和、差
②积、商的相对误差等于各测量值相对误差的和、差
R = x y / z
2.偶然误差的传递
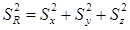 ①和、差结果的标准偏差的平方,等于各测量值的标准偏差的平方和。
①和、差结果的标准偏差的平方,等于各测量值的标准偏差的平方和。
R = x + y -z
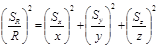 ②积、商结果的相对标准偏差的平方,等于各测量值的相对标准偏差的平方和。
②积、商结果的相对标准偏差的平方,等于各测量值的相对标准偏差的平方和。
R = x y / z
3.测量值的极值误差
在分析化学中,若需要估计一下整个过程可能出现的最大误差时,可用极值误差来表示。它假设在最不利的情况下各种误差都是最大的,而且是相互累积的,计算出结果的误差当然也是最大的,故称极值误差。
五、提高分析结果准确度的方法
1、系统误差的判断与评估
(1)对照试验:选用组成与试样相近的标准试样,在相同条件下进行测定,测定结果与标准值对照,判断有无系统误差,又可用此差值对测定结果进行校正。
(2)回收试验:其结果用于系统误差的评估,不能用于结果的校正。
2、消除系统误差的方法
(一)选择恰当的分析方法,消除方法误差:不同方法,其灵敏度、准确度、精密度和选择性是不相同的,应根据待测组分的含量、性质、试样的组成及对准确度的要求来选择,还要考虑现有条件和分析成本。
(二)校准仪器,消除仪器误差:对砝码、移液管、酸度计等进行校准,消除仪器引起的系统误差
(三)采用不同方法, 减小测量的相对误差
(四)空白实验,消除试剂误差:在不加试样的情况下,按试样分析步骤和条件进行分析实验,所得结果为空白值,从试样测定结果中扣除即可以消除试剂、蒸馏水和容器引入的杂质。
(五)遵守操作规章,消除操作误差
3、减小偶然误差的方法:增加平行测定次数,用平均值报告结果,一般测3~5次。
第三节 有效数字及其运算法则
一、有效数字
1.定义:为实际能测到的数字。有效数字的位数和分析过程所用的测量仪器的准确度有关。
有效数字=准确数字+ 最后一位欠准的数(±1)
如滴定管读数23.57ml,4位有效数字。称量质量为6.1498g,5位有效数字
2. “0”的作用:作为有效数字使用或作为定位的标志。
例:滴定管读数为20.30毫升, 有效数字位数是四位。表示为0.02030升,前两个0是 起定位作用的,不是有效数字,此数据仍是四位有效数字。
3. 规定
(1)改变单位并不改变有效数字的位数。20.30ml 0.02030L
(2)在整数末尾加0作定位时,要用科学计数法表示。
例:3600 → 3.6×10 3 两位 → 3.60×10 3三位
(3)在分析化学计算中遇到倍数、分数关系时,视为无限多位有效数字。
(4)pH、pC、logK等对数值的有效数字位数由小数部分数字的位数决定。
[H+]= 6.3×10 -12 [mol/L] → pH = 11.20 两位
(5)首位为8或9的数字,有效数字可多计一位。例92.5可以认为是4位有效数;
二、有效数字的修约规则
1. 基本规则:四舍六入五成双:当尾数≤4时则舍,尾数≥6时则入;尾数等于5而后面的数都为0时,5前面为偶数则舍,5前面为奇数则入;尾数等于5而后面还有不为0的任何数字,无论5前面是奇或是偶都入。
例:将下列数字修约为4位有效数字。
0.526647--------0.5266 10.23500--------10.24 250.65000-------250.6
18.085002--------18.09 3517.46--------3517
2. 一次修约到位,不能分次修约
错误修约:4.1349 → 4.135 → 4.14 正确修约:4.1349 → 4.13
 3. 在修约相对误差、相对平均偏差、相对标准偏差等表示准确度和精密度的数字时,一般取1~2位有效数字,只要尾数不为零,都可先多保留一位有效数字,从而提高可信度
3. 在修约相对误差、相对平均偏差、相对标准偏差等表示准确度和精密度的数字时,一般取1~2位有效数字,只要尾数不为零,都可先多保留一位有效数字,从而提高可信度
三、有效数字的运算法则
(一)加减法:以小数点后位数最少的数为准(即以绝对误差最大的数为准)
例: 50.1 + 1.45 + 0.5812 = 52.1
δ ±0.1 ±0.01 ±0.0001
(二)乘除法:以有效数字位数最少的数为准(即以相对误差最大的数为准)
δ ±0.0001 ±0.01 ±0.00001
例: 0.0121 × 25.64 × 1.05782 = 0.328
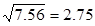
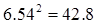 RE ±0.8% ±0.4% ±0.009%
RE ±0.8% ±0.4% ±0.009%
(三)乘方、开方:结果的有效数字位数不变
(四)对数换算:结果的有效数字位数不变
[H+]= 6.3×10 - 12 [mol/L] → pH = 11.20 两位
四、在分析化学中的应用
1.数据记录:如在万分之一分析天平上称得某物体重0.2500g,只能记录为0.2500g,不能记成0.250g或0.25g。又如从滴定管上读取溶液的体积为24mL时,应该记为24.00mL,不能记为24mL或24.0 mL。
2.仪器选用:若要称取约3.0g的样品时,就不需要用万分之一的分析天平,用十分之一的天平即可。
3.结果表示:如分析煤中含硫量时,称样量为3.5g。两次测定结果:
甲为0.042%和0.041%;乙为0.04201%和0.04199%。显然甲正确,而乙不正确。
第四节 分析数据的统计处理
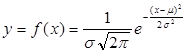 一、偶然误差的正态分布
一、偶然误差的正态分布
偶然误差符合正态分布, 正态分布的概率密度函数式:
正态分布的两个重要参数:
(1)μ为无限次测量的总体均值,表示无限个数据的集中趋势(无系统误差时即为真值)
(2)σ是总体标准偏差,表示数据的离散程度
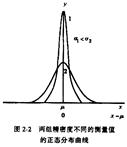 特点:
特点:
1. x =μ时,y 最大
2. 曲线以x =μ的直线为对称
3. 当x →﹣∞或﹢∞时,曲线以x 轴为渐近线
4. σ↑,y↓, 数据分散,曲线平坦;σ↓,y↑, 数据集中,曲线尖锐
5. 测量值都落在-∞~+∞,总概率为1

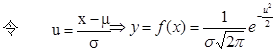 为了计算和使用方便,作变量代换
为了计算和使用方便,作变量代换
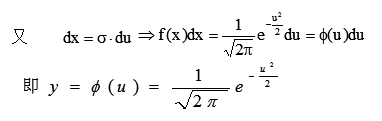
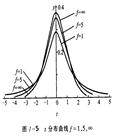 以u为变量的概率密度函数表示的正态分布曲线称为标准正态分布曲线(u分布),此曲线的形状与σ大小无关
以u为变量的概率密度函数表示的正态分布曲线称为标准正态分布曲线(u分布),此曲线的形状与σ大小无关
二、t分布曲线
在t分布曲线中,纵坐标仍为概率密度,横坐标是统计
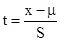
 量t而不是u。t定义为 或
量t而不是u。t定义为 或
t分布曲线随自由度f=n-1变化,当n→∞时,t分布曲线即是正态分布。
三、平均值的精密度和置信区间
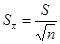 (一)平均值的精密度
(一)平均值的精密度
 平均值的标准偏差
平均值的标准偏差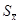 与样本的标准偏差(即单次测量值的标准偏差)S的关系:
与样本的标准偏差(即单次测量值的标准偏差)S的关系:
(二)平均值的置信区间
我们以x为中心,在一定置信度下,估计μ值所在的范围(x±tS),称为单次测量值的置信区间: μ=X±ts
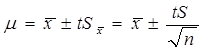
 我们以
我们以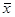 为中心,在一定置信度下,估计μ值所在的范围
为中心,在一定置信度下,估计μ值所在的范围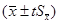 称为平均值的置信区间:
称为平均值的置信区间:
注意:
1. 置信度越大且置信区间越小时,数据就越可靠
2. 置信度一定时,减小偏差、增加测量次数以减小置信区间
3. 在标准偏差和测量次数一定时,置信度越大,置信区间就越大
四、显著性检验
在分析工作中常碰到两种情况:1用两种不同的方法对样品进行分析,分析结果是否存在显著性差异; 2不同的人或不同单位,用相同的方法对试样进行分析,分析结果是否存在显著性差异。这要用统计的方法加以检验。
(一) F检验:比较两组数据的方差(S2),确定它们的精密度是否存在显著性差异,用于判断两组数据间存在的偶然误差是否显著不同。(用来做什么?考点)
 检验步骤:
检验步骤:
计算两组数据方差的比值F,
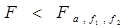
 查单侧临界临界值
查单侧临界临界值 比较判断:
比较判断:
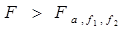 两组数据的精密度不存在显著性差别,S1与S2相当。
两组数据的精密度不存在显著性差别,S1与S2相当。
两组数据的精密度存在着显著性差别,S2明显优于S1。
(二)t 检验:将平均值与标准值或两个平均值之间进行比较,以确定它们的准确度是否存在显著性差异,用来判断分析方法或操作过程中是否存在较大的系统误差。(用来做什么?考点)
1. 平均值与标准值(真值)比较
检验步骤:
a)  计算统计量t,
计算统计量t,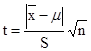 b)查双侧临界临界值
b)查双侧临界临界值
比较判断:
1) 当t ≥ 时,说明平均值与标准值存在显著性差异,分析方法或操作中有较大的系统误差存在,准确度不高;
时,说明平均值与标准值存在显著性差异,分析方法或操作中有较大的系统误差存在,准确度不高;
2) 当t < 时,说明平均值与标准值不存在显著性差异,分析方法或操作中无明显的系统误差存在,准确度高。
时,说明平均值与标准值不存在显著性差异,分析方法或操作中无明显的系统误差存在,准确度高。
2. 平均值与平均值比较:两个平均值是指试样由不同的分析人员测定,或同一分析人员用不同的方法、不同的仪器测定。
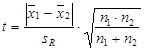 检验步骤:
检验步骤:
计算统计量t,
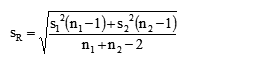
式中SR称为合并标准偏差:
查双侧临界临界值 (总自由度 f =n1+n2-2)
(总自由度 f =n1+n2-2)
比较判断:
当t ≥ 时,说明两个平均值之间存在显著性差异,两个平均值中至少有一个存在较大的系统误差;
时,说明两个平均值之间存在显著性差异,两个平均值中至少有一个存在较大的系统误差;
当t <  时,说明两个平均值之间不存在显著性差异,两个平均值本身可能没有系统误差存在,也可能有方向相同、大小相当的系统误差存在。
时,说明两个平均值之间不存在显著性差异,两个平均值本身可能没有系统误差存在,也可能有方向相同、大小相当的系统误差存在。
注意:要检查两组数据的平均值是否存在显著性差异,必须先进行 F 检验,确定两组数据的精密度无显著性差异。如果有,则不能进行 t 检验。
。
第四章 滴定分析法概论
(考)定义:将一种已知准确浓度的试剂溶液滴加到待测物质的溶液中,直到所滴加的试剂与待测物质按化学计量关系定量反应为止,然后根据试液的浓度和体积,通过定量关系计算待测物质含量的方法(容量分析)
基本概念:
Ø 滴定:将滴定剂通过滴管滴入待测溶液中的过程
Ø 标准溶液:已知准确浓度的试剂溶液
Ø 滴定剂:用于滴定的标准溶液
Ø 化学计量点:滴定剂(标准溶液)与待测物质按化学计量关系恰好完全反应的那一点,简称计量点。(理论值)
Ø 指示剂:能在计量点附近发生颜色变化的试剂
Ø 滴定终点:滴定分析中指示剂发生颜色改变的那一点(实测值)
Ø 终点误差(滴定误差):滴定终点与化学计量点不一致造成的误差
分类:滴定分析法可分为酸碱滴定,沉淀滴定, 氧化-还原滴定,配位滴定。大多数滴定都是在水溶液中进行的,若在水以外的溶剂中进行,称为非水滴定法。
特点:仪器简单,操作简便、快速,应用广泛,用于常量分析,准确度高,相对误差为±0.2%
第一节 滴定反应条件和滴定方式
一、滴定反应条件
1.有确定的化学计量关系2.反应定量完成3.反应速度要快4.有适当的方法确定滴定终点
二、滴定方式
1. 直接滴定法:用标准溶液直接滴定被测物质溶液。
2. 剩余滴定法(返滴定法):先准确加入过量的标准溶液,与被测物完全反应后,再用另外一个标准溶液滴定剩余的标准溶液。如碳酸钙的测定
CaCO3 +2 HCl = CO2 + H2O + CaCl2 NaOH + HCl = NaCl + H2O
3. 置换滴定法:先用适当试剂与待测物质反应,定量置换出另一种物质 ,再用标准溶液去滴定该物质的方法。
4. 间接滴定法:将被测物通过一定的化学反应转化为另一种物质,再用滴定剂滴定。
第二节 基准物质与标准溶液
一、基准物质:能用于直接配制或标定标准溶液的物质
基准物质具备的条件:1.组成与化学式相符;2.具有较大的摩尔质量;3.纯度高;4.性质稳定
常用的基准物质有Na2CO3、KHC8H4O4、Na2B4O7·10H2O, CaCO3、K2Cr2O7、H2C2O4·2H2O、NaCl、Zn 等
二、标准溶液的配制与标定
浓度准确已知的试剂溶液
1、直接法:准确称取一定量的基准物质,溶解,转移到容量瓶中,稀释至刻度。根据基准物质的质量和容量瓶的体积算出标准溶液的准确浓度。
2、间接法(标定法):先配制成一种近似于所需浓度的溶液,再利用基准物质或另一标准溶液来确定该溶液的准确浓度。
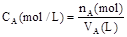 三、标准溶液浓度的表示方法
三、标准溶液浓度的表示方法
(一)物质的量浓度:单位体积溶液所含溶质的物质的量
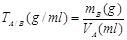 (计算题)(二)滴定度:TA/B指每毫升滴定剂溶液相当于待测物的质量(g/ml) (A指滴定剂,B指待测物)
(计算题)(二)滴定度:TA/B指每毫升滴定剂溶液相当于待测物的质量(g/ml) (A指滴定剂,B指待测物)
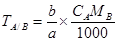
 滴定剂的量浓度与滴定度的换算
滴定剂的量浓度与滴定度的换算
aA + bB = cC + dD
滴定剂 被测物
第三节 滴定分析中的计算
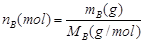 一、基本计算公式
一、基本计算公式
1. 物质的量
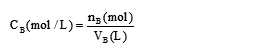
2. 物质的量浓度
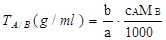

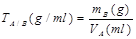 3. 滴定度
3. 滴定度
<=> 或
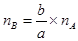
 4.化学反应计量关系
4.化学反应计量关系
aA + bB = cC + dD

5.质量分数

6. 质量浓度
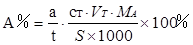 7. 被测物质含量的计算 被测组分的含量是指被测组分(mA)占样品质量(S)的百分比
7. 被测物质含量的计算 被测组分的含量是指被测组分(mA)占样品质量(S)的百分比
(1)直接滴定法
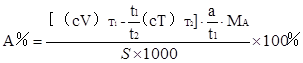 (2)返滴定法
(2)返滴定法
第五章 酸碱滴定法
第一节 水溶液中的酸碱平衡
一、酸碱质子理论:酸是能给出质子的物质,碱是能接受质子的物质。
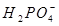 既可以是酸,又可以是碱,这类物质称为两性物质。
既可以是酸,又可以是碱,这类物质称为两性物质。
实质上是发生在两对共轭酸碱对之间的质子转移反应,由两个酸碱半反应组成。
二、酸碱溶液中各型体的分布
(一)分布系数:溶液中某型体的平衡浓度在溶质总浓度所占的比例,以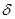 i表示
i表示
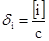
 式中:i为某种型体
式中:i为某种型体
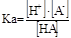
 (二)弱酸(弱碱)各型体的分布系
(二)弱酸(弱碱)各型体的分布系
一元弱酸

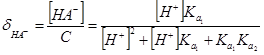
 二元弱酸
二元弱酸
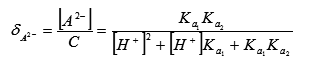
(二)酸度对弱酸(碱)各型体分布的影响
弱酸(弱碱)各型体的分布系数与溶液的酸度和酸碱的离解常数有关,而与分析浓度无关。
(三)水溶液中酸碱平衡的处理方法
 1、质量平衡(物料平衡):在一个化学平衡体系中,某一组分的分析浓度等于该组分各种存在型体的平衡浓度之和,称为质量平衡
1、质量平衡(物料平衡):在一个化学平衡体系中,某一组分的分析浓度等于该组分各种存在型体的平衡浓度之和,称为质量平衡
C mol/L Na2CO3溶液的质量平衡式
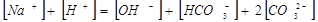 2、电荷平衡:在一个化学平衡体系中,正离子电荷的总和与负离子电荷的总和相等,称为电荷平衡
2、电荷平衡:在一个化学平衡体系中,正离子电荷的总和与负离子电荷的总和相等,称为电荷平衡
C mol/L Na2CO3 水溶液的电荷平衡式:
3、质子平衡:酸碱反应达平衡时,酸失去的质子数等于碱得到的质子数,称为质子平衡
质子参考水准:能参与质子交换的组分的初始形态以及溶剂水。
例:写出Na(NH4)HPO4水溶液的质子条件式
 得质子产物 参考水准 失质子产物
得质子产物 参考水准 失质子产物


 NH
4
+ —→ NH
3
NH
4
+ —→ NH
3



 HPO
4
2- —→ PO
4
3-
HPO
4
2- —→ PO
4
3-
 H3O+(H+) ←— H2O —→ OH-
H3O+(H+) ←— H2O —→ OH-
-三、酸碱溶液中pH的计算
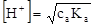 (1)当Ca
(1)当Ca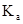 ≥20
≥20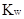 ,同时Ca/
,同时Ca/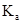 ≥500时,最简式:
≥500时,最简式:
(2)弱酸HA(浓度为Ca mol/L)与共轭碱A-(浓度为Cb mol/L)的PH计算
 当Ca≥20[H+], Cb≥20[H+]时
当Ca≥20[H+], Cb≥20[H+]时

缓冲溶液▲
第二节 基本原理
一、酸碱指示剂
(一)变色范围
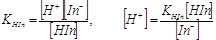
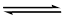 HIn H+ + In-
HIn H+ + In-
 酸式 碱式
酸式 碱式
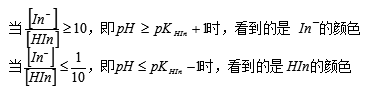
故指示剂的理论变色范围是: pH=pKHIn±1
由于人眼对深色比浅色灵敏,实际变色范围与理论推算的的变色范围并不完全相同。
pKa 理论范围 实际范围 酸色 碱色
甲基橙 3.4 2.4~4.4 3.1~4.4 红 黄
甲基红 5.1 4.1~6.1 4.4~6.2 红 黄
酚酞 9.1 8.1~10.1 8.0~10.0 无 红
百里酚酞 10.0 9.0~11.0 9.4~10.6 无 蓝
注:一般而言,人们观察指示剂颜色的变化约有0.2~0.5pH单位的误差,称之为观测终点的不确定性,用△pH来表示,一般按△pH=±0.2来考虑,作为使用指示剂目测终点的分辨极限值。
(三)影响指示剂变色范围的因素
1. 指示剂的用量
Ø 对于双色指示剂用量多少对色调变化有影响,用量太多或太少都使色调变化不鲜明。
Ø 对于单色指示剂用量多少对色调变化影响不大,但影响变色范围和终点。
Ø 指示剂本身都是弱酸或弱碱,也会参与酸碱反应。
2. 温度:温度变时指示剂常数和水的离子积都会变,则指示剂的变色范围也随之发生改变。
3. 中性电解:溶液中中性电解质的存在增加了溶液的离子强度,使指示剂的表观离解常数改变,将影响指示剂的变色范围。某些盐类具有吸收不同波长光波的性质,也会改变指示剂颜色的深度和色调。
4.滴定程序:为了达到更好的观测效果,在选择指示剂时还要注意它在终点时的变色情况。例如:酚酞由酸式无色变为碱式红色,易于辨别,适宜在以强碱作滴定剂时使用。同理,用强酸滴定强碱时,采用甲基橙就较酚酞适宜。
(四)混合指示剂:混合指示剂是把两种或两种以上试剂混合,利用它们颜色的互补性,使终点颜色变化更鲜明,变色范围更窄。
混合指示剂通常有两种配制方法:
1.指示剂+惰性染料:对于这种混合指示剂,变色范围和终点基本不变,但色调变化更明。
2. 指示剂+指示剂:对于这种混合指示剂,变色范围、终点以及色调均发生了改变。混合 后的指示剂,色调变化更鲜明,变色范围更窄。
注:混合指示剂在配制时,应严格按比例混合。
二、滴定曲线
Ø 在滴定过程中,我们把计量点附近溶液某种参数(如PH)的急剧变化称为滴定突跃
Ø 滴定百分率为99.9%至100.1%即滴定相对误差为±0.1%时,溶液某种参数(如PH)的变化范围称为滴定突跃范围。
Ø 滴定突跃范围是选择指示剂的重要依据。酸碱指示剂的选择原则:指示剂的变色范围要全部或至少有一部分落在滴定突跃范围内。
三、滴定突跃与指示剂选择
一、(1)影响滴定突跃范围的因素:
Ø 对于强酸强碱,溶液浓度越大,突跃范围越大,可供选择的指示剂愈多;浓度越小,突跃范围越小,可供选择的指示剂就越少。当突跃范围小于0.4PH时(C=10-4mol/L)就没有合适的指示剂了。
Ø 对于弱酸弱碱的滴定,浓度越大、离解常数越大,则突跃范围就越大,反之则越小。当突跃范围减小至约0.4PH时(CK=10-8),指示剂就不合适了。
(2)指示剂的选择
Ø 强酸强碱的滴定,计量点时溶液呈中性,突跃范围横跨酸性区和碱性区,突跃范围较大,酸性范围内和碱性范围内变色的指示剂都可以考虑选用。
Ø 强碱滴定弱酸,计量点时溶液呈弱碱性,突跃范围较小,位于碱性区,碱性范围内变色的指示剂可以考虑选用。
Ø 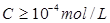 强酸滴定弱碱,计量点时溶液呈弱酸性,突跃范围较小,位于酸性区,酸性范围内变色的指示剂可以考虑选用。
强酸滴定弱碱,计量点时溶液呈弱酸性,突跃范围较小,位于酸性区,酸性范围内变色的指示剂可以考虑选用。
¨  强酸强碱准确滴定的条件:
强酸强碱准确滴定的条件:
¨ 一元弱酸弱碱准确滴定的条件:
(二)一元弱酸弱碱的滴定
1. 滴定曲线
现以NaOH滴定一元弱酸HAc为例:设HAc为浓度 Ca=0.1000mol/L,体积Va =20.00ml;NaOH的浓度 Cb=0.1000mol/L,滴定时加入的体积为Vb ml,
 滴定反应:HAc+OH-=H2O+Ac-
滴定反应:HAc+OH-=H2O+Ac-
滴定反应常数:
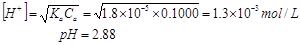 ① 滴定开始前
① 滴定开始前

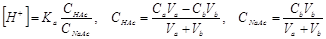 ② 滴定开始至化学计量点前
② 滴定开始至化学计量点前
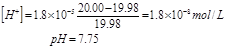 当Vb=19.98 ml 即相对误差为-0.1%时,
当Vb=19.98 ml 即相对误差为-0.1%时,
 ③ 化学计量点
③ 化学计量点
④ 化学计量点后
由于过量NaOH的存在,抑制了Ac 的水解,溶液的pH值仅由过量的NaOH的量和溶液体积来决定,其计算方法与强碱滴定强酸相同。
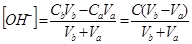

当Vb=20.02 ml 即相对误差为+0.1%时,
(三)多元酸碱的滴定
1. 多元酸的滴定
多元酸准确(分步)滴定的条件:
① 当CaKai <10-8时,第 i 级离解的H+不能准确滴定,没有滴定突跃
② 当CaKai ≥10-8时,若Kai/Kai+1 ≥104,则第 i 级离解的H+可以准确滴定,有滴定突跃; 若Ka/Kai+1 <104,则第 i 级离解的H+不能准确滴定,没有滴定突跃
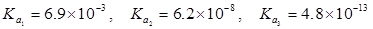 例:用1mol/LNaOH滴定20.00ml 1mol/LH3PO4
例:用1mol/LNaOH滴定20.00ml 1mol/LH3PO4

1mol/L 的H3PO4 可以用NaOH准确分步进行滴定,有两个滴定突跃。
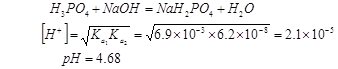 对于H3PO4的滴定,第一计量点:
对于H3PO4的滴定,第一计量点:
 可选甲基橙、甲基红指示剂,也可选甲基橙与溴甲酚绿的混合指示剂
可选甲基橙、甲基红指示剂,也可选甲基橙与溴甲酚绿的混合指示剂
第二计量点:
可选酚酞、百里酚酞指示剂,也可选酚酞与百里酚酞的混合指示剂。
2. 多元碱的滴定:多元碱准确(分步)滴定的条件与多元酸相同。
第三节 滴定终点误差
 (必考)定义:由于指示剂的变色不恰好在化学计量点而使滴定终点和化学计量点不相符合所致的相对误差,也称滴定误差(TE);常用百分数表示。
(必考)定义:由于指示剂的变色不恰好在化学计量点而使滴定终点和化学计量点不相符合所致的相对误差,也称滴定误差(TE);常用百分数表示。
一、强酸强碱滴定的终点误差:
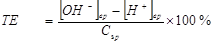 式中:[OH-]、[H+]分别为滴定前的原始浓度;
式中:[OH-]、[H+]分别为滴定前的原始浓度;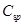 、
、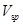 为化学计量点时被测物的实际浓度和体积;
为化学计量点时被测物的实际浓度和体积;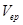 为滴定终点时溶液的体积,因
为滴定终点时溶液的体积,因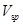 ≈
≈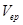 ,带入上式,得
,带入上式,得
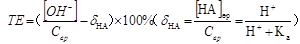 二、弱酸(碱)的滴定终点误差
二、弱酸(碱)的滴定终点误差
强碱滴定一元弱酸

强酸滴定一元弱碱
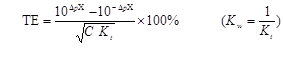 滴定误差也可用PH按林邦误差公式直接计算
滴定误差也可用PH按林邦误差公式直接计算
式中:pX为滴定过程中发生变化的参数,如pH或pM;△pX为终点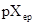 与计量点
与计量点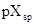 之差;△pX=
之差;△pX=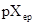 —
—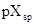 ;Kt为滴定反应平衡常数即滴定常数,c与计量点时滴定产物的总浓度
;Kt为滴定反应平衡常数即滴定常数,c与计量点时滴定产物的总浓度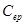 有关。
有关。
三、应用示例
- 乙酰水杨酸的测定
乙酰水杨酸(阿司匹林)是常用的解热镇痛药,属芳酸酯类结构,可用标准碱溶液直接滴定,以酚酞为指剂,其滴定反应为:
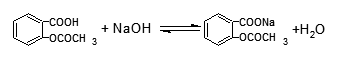
2.药用氢氧化钠的测定 (计算题)
药用氢氧化钠易吸收空气中的CO2 ,形成NaOH和Na2CO3 的混合物。该混合碱的测定有两种方法。
(1)氯化钡法
称取一定量样品ms g,溶解并稀释至一定体积为Va ml。吸取等体积的两份试液,各为Vbml。一份以甲基橙为指示剂,用HCl标准溶液滴定至终点,消耗体积为V1 ml
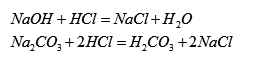
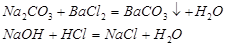 另一份先加入过量的BaCl2 ,再以酚酞为指示剂,用HCl标液滴定至终点,消耗体积为V2 ml,显然,V1 > V2
另一份先加入过量的BaCl2 ,再以酚酞为指示剂,用HCl标液滴定至终点,消耗体积为V2 ml,显然,V1 > V2

(2)双指示剂法
 称取一份试样,溶解,先以酚酞为指示剂,用HCl标液滴定至终点,消耗体积为V1 ml,
称取一份试样,溶解,先以酚酞为指示剂,用HCl标液滴定至终点,消耗体积为V1 ml,
再加入甲基橙指示剂,继续用HCl标液滴定至终点,消耗体积为V2 ml,

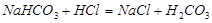 显然,V2 < V1
显然,V2 < V1
双指示剂法操作简便,但在使用酚酞时误差较大,氯化钡法准确度较高。
(考点)用双指示剂法判断混合碱试样的组成:
有一碱溶液可能是NaOH,NaHCO3,Na2CO3或以上几种物质混合物,用HCL标准溶液滴定,以酚酞为指示剂滴定到终点时消耗HCL V1 mL;继续以甲基橙为指示剂滴定到终点时消耗HCL V2 mL,由以下V1和V2的关系判断该碱溶液的组成。
(1)V1 > 0, V2 = 0 NaOH
(2)V2 > 0, V1 = 0 NaHCO3
(3)V1 = V2 Na2CO3
(4)V1 > V2 > 0 NaOH + Na2CO3
(5)V2 > V1 > 0 Na2CO3 + NaHCO3
4、氮的测定
 (1)
蒸馏法
(1)
蒸馏法


 a. NH4+ + OH - NH3↑+ H2O
a. NH4+ + OH - NH3↑+ H2O
NH3 + HCL(定过量) NH4CL
 HCL(过量)+ NaOH NaCL + H2O
HCL(过量)+ NaOH NaCL + H2O
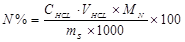
 b. NH4+ + OH - NH3↑+ H2O
b. NH4+ + OH - NH3↑+ H2O
 NH3 + H3BO3 NH4+ + H2BO3-
NH3 + H3BO3 NH4+ + H2BO3-
 H2BO3- + HCL CL- + H3BO3
H2BO3- + HCL CL- + H3BO3
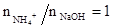 (2) 甲醛法:甲醛与铵盐生成六次甲基四胺离子,同时放出定量的酸,再以酚酞为指示剂,用NaOH标准溶液滴定
(2) 甲醛法:甲醛与铵盐生成六次甲基四胺离子,同时放出定量的酸,再以酚酞为指示剂,用NaOH标准溶液滴定
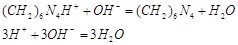
 4NH4+ + 6HCHO (CH2)6N4H+ + 3H+ + 6H2O
4NH4+ + 6HCHO (CH2)6N4H+ + 3H+ + 6H2O
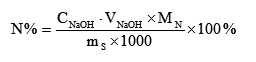
第八章 氧化还原滴法
Ø 氧化还原滴定:以氧化还原反应为基础的滴定方法。
Ø 氧化还原反应的特点:
1) 氧化还原反应机制比较复杂,反应分多步完成,常伴有多种副反应,
2) 有些反应K值很大,但速度很慢。
Ø 按选用的滴定剂的不同可分为:碘量法、高锰酸钾法、重铬酸钾法、亚硝酸钠法、溴量法、铈量法 等
第 一 节 氧化还原反应
一、电极电位与Nernst方程式
电极电位是电极与溶液接触处存在的双电层产生的。物质的氧化还原性质可以用相关氧化还原电对电极电位来衡量。
电对电极电位的大小可通过Nernst方程式计算。
对一个氧化还原半反应(也称为电极反应)
Ox + ne = Red
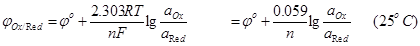 所构成的氧化还原电对用Ox/Red表示。该电对具有一定的电位称为电极电位,电极电位可以用Nernst方程表示。
所构成的氧化还原电对用Ox/Red表示。该电对具有一定的电位称为电极电位,电极电位可以用Nernst方程表示。
式中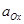 、
、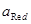 分别是游离Ox、Red的活度。式中φ0为标准电极电位,它是温度为25℃时,相关离子的活度均为1mol/L,气压为1.013×10 5Pa时,测出的相对于标准氢电极的电极电位(规定标准氢电极电位为零)。R为气体常数:8.314J/(K·mol);T为绝对温度K;F为法拉第常数(96487c/mol);n为氧化还原半反应转移的电子数目
分别是游离Ox、Red的活度。式中φ0为标准电极电位,它是温度为25℃时,相关离子的活度均为1mol/L,气压为1.013×10 5Pa时,测出的相对于标准氢电极的电极电位(规定标准氢电极电位为零)。R为气体常数:8.314J/(K·mol);T为绝对温度K;F为法拉第常数(96487c/mol);n为氧化还原半反应转移的电子数目
二、条件电极电位及其影响因素
 (一)条件电极电位
(一)条件电极电位
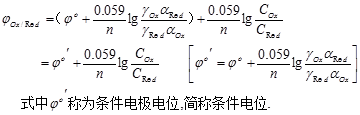 代入Nernst方程,得
代入Nernst方程,得
条件电位是在特定条件下,氧化态和还原态的总浓度Cox和CRed都为1mol/L时的实际电位。
(二)影响条件电位的因素
1.盐效应:溶液中盐类电解质对条件电位的影响。
2.酸效应:溶液酸度对条件电位的影响
① 氧化形或还原形是弱酸或弱碱,发生离解,其影响可由副反应系数计算。
② 半反应中有H 或OH 参加,因而条件电位的算式中应包括H 或OH 的浓度。
3.生成配合物:向溶液中加入一种配位剂,与氧化态或还原态反应。若氧化态生成稳定的配合物,则条件电位降低;若还原态生成稳定的配合物,则条件电位升高。
4.生成沉淀:加入可与氧化态或还原态生成沉淀的沉淀剂,因改变氧化态或还原态的浓度而改变电位。氧化态生成沉淀时,条件电位降低;还原态生成沉淀时,条件电位升高。
 计算KI浓度为1mol/L时,Cu2+/Cu+电对的条件电位,在此条件下,Cu2+能否氧化I- ?
计算KI浓度为1mol/L时,Cu2+/Cu+电对的条件电位,在此条件下,Cu2+能否氧化I- ?
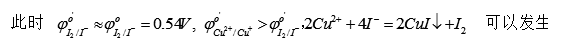
 注:
注:
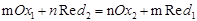 三、氧化还原反应进行的程度
三、氧化还原反应进行的程度
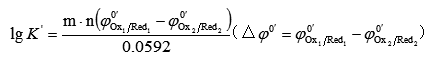
式中m、n是最小公倍数
(二)判断反应能否定量进行
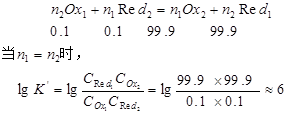 要使反应定量进行,反应的完全程度应达到99.9%以上。
要使反应定量进行,反应的完全程度应达到99.9%以上。
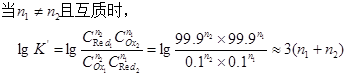 即 lgK/ ≥ 6时,反应能定量进行。
即 lgK/ ≥ 6时,反应能定量进行。
即 lgK/ ≥ 3(n1 + n2 )时,反应能定量进行。
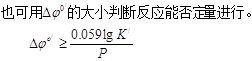 对不同类型的氧化还原反应,能定量进行所要求的lgK/是不相同的。
对不同类型的氧化还原反应,能定量进行所要求的lgK/是不相同的。
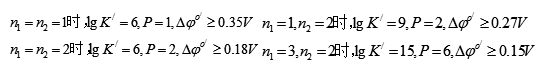
注:一般而言,不论什么类型的氧化还原反应,只要△φo’ ≥0.35V,都能定量进行,可以满足滴定分析的要求。若△φo’<0.35 V,则应考虑反应类型。例如,△φo’=0.30V,若n1 =1,n2 =2,则可以定量进行。
四、氧化还原反应速率及其影响因素
影响反应速度的因素很多,除了反应物本身的性质外,还与反应物的浓度、温度、催化剂等因素有关。
1.氧化剂、还原剂本身的性质:不同的氧化剂和还原剂,反应速率可以相差很大,这与它们的电子层结构以及反应机理有关。
2.反应物浓度
3.反应温度:升温可增加碰撞,使活化分子增多,加快反应。每增高100C,速度增加2~3倍
4.催化剂:加入催化剂可以改变反应的历程,因而改变反应速度。分析化学中主要利用正催化剂使反应加速,如Ce4+ 氧化AsO2- 的反应速度很慢,加入少量KI可使反应迅速进行;再如MnO4-氧化C2O42- 反应速度很慢,但反应生成的Mn2+ 对反应有催化作用,这种生成物本身起催化作用的反应叫自动催化反应。
 5.诱导反应MnO4-氧化Cl-的反应进行得很慢,但当溶液中存在Fe2+时,由于MnO4-与Fe2+反应的进行,诱发MnO4-与Cl-反应加快进行。这种由一个反应的发生促进另一个反应进行的现象,称为诱导反应。例:
5.诱导反应MnO4-氧化Cl-的反应进行得很慢,但当溶液中存在Fe2+时,由于MnO4-与Fe2+反应的进行,诱发MnO4-与Cl-反应加快进行。这种由一个反应的发生促进另一个反应进行的现象,称为诱导反应。例:
其中MnO4-称为作用体;Fe2+称为诱导体;Cl-称为受诱体。
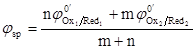
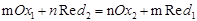 五、化学计量点点位
五、化学计量点点位
第二节 基本原理
一、滴定曲线
氧化还原滴定的突跃范围大小与反应电对条件电位差有关,条件电位差△φo/越大,滴定突跃范围越大。对称电对参与的氧化还原反应,浓度改变对突跃范围影响不大。
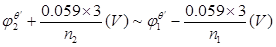 在一般氧化还原滴定中
在一般氧化还原滴定中
突跃范围是
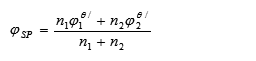
计量点是
当两个半电池反应转移电子数相等时,化学计量点电位恰好位于滴定突跃的中央;当半电池反应转移电子数不等时,化学计量点电位偏向转移电子数多的电对一方。
二、指示剂
指示氧化还原滴定终点的常用指示剂有以下四种:
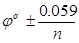 (一)氧化还原指示剂:指示剂本身是一种弱氧化剂或还原剂,它的氧化形或还原形具有明显不同的颜色。如二苯胺磺酸钠
(一)氧化还原指示剂:指示剂本身是一种弱氧化剂或还原剂,它的氧化形或还原形具有明显不同的颜色。如二苯胺磺酸钠
氧化还原指示剂变色的电位范围是

这一点称为氧化还原指示剂的变色点。
(考点)选择氧化还原指示剂时,应使指示剂的条件电位落在滴定突跃范围内,并尽可能靠近化学计量点,以减小终点误差
(二)自身指示剂:有些标准溶液本身有很深的颜色,滴定时无需另外加入指示剂,只要标准溶液稍微过量一点,即可显示终点的到达。如高锰酸钾
(三)特殊指示剂:有些指示剂本身不具有氧化还原性,但能与氧化剂或还原剂作用产生特殊的颜色,利用这种特殊颜色的出现或消失指示滴定终点,称为特殊指示剂。如淀粉
第三节 碘量法
一、基本原理
碘量法(iodimetry)是以碘作为氧化剂,或以碘化物作为还原剂,进行氧化还原滴定的方法。
 (一)直接碘量法:以I2 标液为滴定剂的碘量法凡电极电位低于I2/I- 电对的,其还原形可用I2 标准溶液直接滴定。
(一)直接碘量法:以I2 标液为滴定剂的碘量法凡电极电位低于I2/I- 电对的,其还原形可用I2 标准溶液直接滴定。
(考点)直接碘量法只能在酸性、中性或弱碱性溶液中进行.
(一) 间接碘量法:以Na2S2O3标液为滴定剂的碘量法,包括剩余滴定和置换滴定。
Ø 凡标准电极电位高于I2/I- 电对的,其氧化形可将加入的I-氧化成I2 ,再用Na2S2O3 标准溶液滴定置换出来的I2 ,这种滴定方法,叫做置换碘量法
注:反应要求在中性或弱酸性溶液中进行.
Ø 还有些还原性物质与I2的反应速度慢,可先加入过量的I2标准溶液,待反应完全后,用Na2S2O3 标准溶液滴定剩余的I2,这种滴定方法,叫做剩余碘量法。
二、误差来源及措施
防止碘挥发的方法:
1)过量加入KI;2)在室温下进行;3)使用碘量瓶;4)快滴慢摇
防止碘离子氧化的方法:
1)溶液酸度不宜过高;2)密塞避光放置 ;3)除去催化性杂质(NO2-,Cu2+)
4)I2完全析出后立即滴定;5)滴定速度稍快
三、指示剂
碘量法中应用最多的是淀粉指示剂。
注意:
a) 滴定时应注意淀粉指示剂的加入时刻。直接碘量法,可于滴定前加入,滴定至浅蓝色出现即为终点。间接碘量法则须在临近终点时加入,滴定蓝色消失即为终点。如果过早加入,溶液中有大量碘存在,碘被淀粉表面牢固吸附,不易与Na2S2O3 立即作用,致使终点拖后。
b) 淀粉指示剂应取可溶性直链淀粉新鲜配制,放置过久会腐败变质。支链淀粉只能松动地吸附I2 ,形成一种红紫色产物,不能用作碘量法的终点指示剂。
四、标准溶液的配制与标定
(一)碘标准溶液
注:1)为了避免KI的氧化,配制好的碘标准溶液,须盛于棕色瓶中,密塞存放。
2) 碘标准溶液的准确浓度,可采用已知浓度的硫代硫酸钠溶液标定;也可用基准物As2O3进行标定。
(二)硫代硫酸钠标准溶液
硫代硫酸钠标准溶液不稳定,原因是:
a.水中溶解的CO2易使NaS2O3分解 S2O32- + CO2 + H2O → HSO3- + HCO3-+ S↓
b.空气氧化: 2S2O32-+ O2 →SO42- + S↓
c.水中微生物作用: S2O32- →Na2SO3 + S↓
在配制Na2S2O3 标准溶液,应注意以下问题:
1.采用新煮沸放冷的蒸馏水 这样既可驱除水中残留的CO2 和O2 ,又能杀死微生物。
2.加入少量Na2CO3 作为稳定剂 使溶液呈弱碱性,抑制细菌生长。
3. 贮于棕色瓶中,暗处保存,待浓度稳定后(7~10天),再进行标定。
四、应用与示例
1.维生素C含量的测定-直接碘量法
注意:在滴定时加入适量稀HAc,使溶液保持弱酸性,避免空气氧化。
2.中药胆矾中CuSO4·5H2O的测定—间接碘量法
注意:1.CuI强烈吸附I2造成终点提前,滴定时应用力振摇或在近终点时加KSCN, 将CuI沉淀转化为CuSCN沉淀,释放I2
2.碘离子既是沉淀剂,又是还原剂、配位剂
第四节 高锰酸钾法
一、基本原理
反应需在强酸中进行,且通常为H2SO4才能全部生成Mn2+
二、指示剂
Ø KMnO4作自身指示剂,以出现粉红色且30秒不褪为终点。
Ø 若标准溶液的浓度较低(0.002mol/L以下),可选用二苯胺磺酸钠等氧化还原指示剂指示终点。
二、标准溶液的配制与标定
高锰酸钾在制备和贮存过程中,常混入少量二氧化锰杂质,蒸馏水中常含有少量有机杂质,能还原KMnO4 使其水溶液浓度在配制初期有较大变化, 因此不能用直接法配制标准溶液。间接法配制时,常将溶液煮沸以加速与其杂质的反应,并将配成的溶液盛在棕色玻璃瓶中在冷暗处放置7~10天,待浓度稳定后,过滤除去MnO2等杂质,方可进行标定。
标定KMnO4 溶液常用的基准物有:As2O3 、Na2C2O4 、H2C2O4 ·2H O等。
标定时应注意:
1. 温度:一般控制在75~85oC
2. 酸度:用H2SO4调节酸度,滴定刚开始的酸度一般应控制在约1mol/L。
3. 滴定速度:刚开始滴定的速度不宜太快
4. 催化剂:在滴定前可加几滴MnSO4溶液。
5. 指示剂:一般情况下,高锰酸钾自身可作为指示剂
三、应用与示例(考得可能性不大)
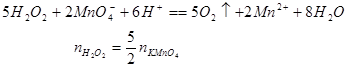 取双氧水10.00ml于100ml容量瓶中,加水稀释至刻度。取25.00ml硫酸酸化,用0.3100mol/L的KMnO4标准溶液滴定,用去31.50ml。问双氧水中H2O2的含量是多少(g/L)
取双氧水10.00ml于100ml容量瓶中,加水稀释至刻度。取25.00ml硫酸酸化,用0.3100mol/L的KMnO4标准溶液滴定,用去31.50ml。问双氧水中H2O2的含量是多少(g/L)

第五节 其他氧化还原滴定法(了解)
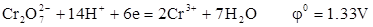 一、重铬酸钾法
一、重铬酸钾法
以二苯胺磺酸钠为指示剂
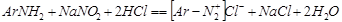 二、亚硝酸钠法(不考,了解)
二、亚硝酸钠法(不考,了解)
 重氮化滴定法
重氮化滴定法
亚硝基化滴定法
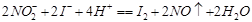 (亚硝酸钠标准溶液常用间接法配制)
(亚硝酸钠标准溶液常用间接法配制)
常用KI-淀粉外指示剂
三、溴酸钾法及溴量法
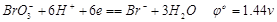 1)酸钾法是以KBrO3标液为滴定剂的氧化还原滴定法。溴酸钾是强氧化剂,在酸性溶液中
1)酸钾法是以KBrO3标液为滴定剂的氧化还原滴定法。溴酸钾是强氧化剂,在酸性溶液中
用溴酸钾标液直接滴定的还原性物质有As(Ⅲ)、Sb3+、Fe2+、Sn2+、H2O2等。
2)将过量的KBr加到一定量的KBrO3标准溶液中,配成KBr-KBrO3标准溶液,即所谓溴液。以溴液为标准溶液的氧化还原滴定法称为溴量法。
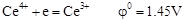 四、铈量法
四、铈量法
(考点)优点:
1.易于提纯,可以直接配制标准溶液。2.溶液稳定,放置较长时间或加热煮沸也不易分解
3.反应简单,副反应少。 4.多选用邻二氮菲-Fe(Ⅱ)为指示剂
注:凡KMnO4法能测定的物质几乎都能用铈量法测定。但铈盐价贵,实际应用不太多。

