高一化学教学工作总结
第一学期的教学工作已经结束,想想本学期的化学教学工作,有得有失, 为了更好地完成今后的教学工作,我就本学期的教学工作总结如下 这学期,我担任了高一年级四个班级的化学教学工作,所以教学任务重,但经过一学期的努力,也取得了较好的教学成绩,得到了所担任班级学生的好评和尊
教师不仅要让学生掌握知识,更重要的是要学生会学习的方法。这就需要教师更新观念,改变教法,把学生看作学习的主体,逐步培养和提高学生的自学能力,思考问题、解决问题的能力,使他们能终身受益。下面,浅谈自己的几点做法。
1、注重课前预习
课前预习是教学中的一个重要的环节,从教学实践来看,学生在课前做不做预习,学习的效果和课堂的气氛都不一样。为了做好这一工作,我经常会在本节课结束时给学生留一些问题,在第二堂课我会及时提问,还会让一些同学站起来给大家讲一讲,通过这些措施督促学生在课后做好预习工作,一提高他们的自学能力。
2、注重课堂教学
课堂是教学活动的主阵地,也是学生获取知识和能力的主要渠道。作为新时代的教师也应与时俱进,改变以往的“满堂灌”,老师知识一味的讲,学生只是坐着听,记笔记,灌输式的的教学方式。我一直都很注重学生在课堂中的角色,老师应该是教学活动的组织者,而课堂教学活动的主体应该是学生,要想办法让每一位学生都动起来,让每一位学生都参与到课堂中来,注重知识的传授过程,而不是只注重结论。为了达到很好的教学效果,我也做了很多的工作:
(1)让学生积极的发言。认真、耐心的听学生讲,然后针对学生讲的做点评,有时候点评也让其他同学进行,最后给予鼓励,肯定。
(2)课堂尽量给同学们充足的时间,让他们来解决一些问题。让同学上黑板做题,讲题。
(3)充分利用化学学科的特点,组织好化学实验。通过实验来启发学生的思维,引导学生积极的思考。我也曾经让学生自己到黑板上来做课
堂演示实验,结果学生很积极,教学效果很好,我觉的这种方法应该继续运用下去。
(4)尽量的设置一些有意义的问题。我一般是会设置好几组问题,问题的设置遵循有简单到难,由浅到深的原则,而且,我也很注重提问题的方式,语气等,尽量做到每个人都积极的思考。
(5)通过几年来的教学,我发现好多学生已经具备了一种很有趣的能力,他们会听老师的语气来回答问题,比如说“是不是!”他们就会回答“是!”,“对不对??”他们就会回答“错!”等,所以我也经常的在语气上误导他们,为的就是让每一位同学都积极的思考,而不是经常的滥竽充数。
(6)我也经常给他们灌输一种思想,一定要独立的思考,老师讲的不一定对,也许那一天我讲的就是错的,所对老师讲的知识要大胆的质疑,有问题就问,要勇敢的坚持自己的看法观点,不要一味的符合别人,以来别人。
通过以上的一些措施,我的目标也基本上达到了,现在好多学生已经具备了一定的独立获取知识的能力,我觉的这是对学生来说最大的收获。
3、注重课后作业和课后复习
课后作业是检验学生知识是否掌握的很重要的方法,从课后作业上可以反映出很多的问题,所以,每次的作业我都会精心的及时的批改,而且会做好作业批改记录,在第二堂课上及时的给学生做说明,让学生重新做一遍,以达到掌握知识的目的、
我也经常给学生讲课后一定要及时的复习,每天都要花一定的时间复习当天的知识,每门课只要花5-10分钟每天就可以了,只要天天坚持下来,复习的效果绝对是很好的。
通过种种的措施,完成了一学期的化学教学工作,对化学的教学工作,我还是比较满意的。在今后的教育教学工作中,我还将会用更大的热情投入到教学工作中,争取以后的工作干的更好。
第二篇:高一化学必修一化学方程式及离子方程式小结[1]
必修一化学方程式及离子方程式小结
1、硫酸根离子的检验:
BaCl2 + Na2SO4 = BaSO4↓+ 2NaCl SO42- + Ba2+ == BaSO4↓
2、碳酸根离子的检验:
CaCl2 + Na2CO3 = CaCO3↓ + 2NaCl CO32- + Ca2+== CaCO3↓
3、碳酸钠与盐酸反应:
Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑ CO32- + 2H+== CO2↑+ H2O
4、木炭还原氧化铜: 2CuO + C  2Cu + CO2↑
2Cu + CO2↑
5、钠与非金属单质反应:
4Na+O2=2Na2O
2Na+O2 Na2O2
Na2O2
Cl2 +2Na 2NaCl
2NaCl
6、钠与水反应:2Na+2H2O=2NaOH+H2↑ 2Na + 2H2O == 2Na+ + 2OH- + H2↑
7、氧化钠的主要化学性质:2Na2O+O2 2Na2O2
2Na2O2
Na2O+H2O=2NaOH Na2O+SO3=Na2SO4
Na2O+CO2=Na2CO3 Na2O+2HCl=2NaCl+H2O
8、过氧化钠的主要反应:
2Na2O2+2H2O=4NaOH+O2↑;2Na2O2+2CO2=2Na2CO3+O2
Na2O2+H2SO4(冷、稀)=Na2SO4+H2O2
9、氯气的主要化学性质:
Cl2 +H2 2HCl (或光照)
2HCl (或光照)
3Cl2 +2P 2PCl3
2PCl3
Cl2 +PCl3 PCl5
PCl5
3Cl2 +2Fe 2FeCl3
2FeCl3
Cl2 +2Na 2NaCl
2NaCl
Cl2+Cu CuCl2
CuCl2
Cl2 +2FeCl2=2FeCl3 Cl2 + 2Fe2+== 2Fe3+ + 2Cl-
Cl2+ 2NaBr = Br2+ 2NaCl Cl2+ 2Br-= Br2+ 2Cl-
Cl2 + 2KI =2KCl + I2 Cl2 + 2I- == 2Cl- + I2
Cl2+H2O=HCl +HClO Cl2 + H2O == Cl- + H+ + HClO
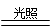 2HClO 2HCl + O2↑
2HClO 2HCl + O2↑
Cl2+SO2 +2H2O=H2SO4 +2HCl Cl2 + SO2 + 2H2O == 2Cl- + SO42- + 4H+
Cl2+2NaOH=NaCl+NaClO+H2O Cl2 + 2OH- == Cl- + ClO- + H2O
2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O 2Ca(OH)2 +2Cl2=2Ca2++2ClO-+2Cl -+2H2O
Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO Ca2++2ClO-+ CO2+ H2O =CaCO3↓+ 2HClO
10、铁及其化合物的主要化学性质:
2Fe + 3Cl2 2FeCl3
2FeCl3
3Fe + 2O2 Fe3O4
Fe3O4
Fe + S FeS
FeS
3Fe+4H2O(g) Fe3O4+4H2
Fe3O4+4H2
Fe+2HCl=FeCl2+H2↑Fe+2H+ = Fe2+ + H2↑
Fe + CuSO4 = FeSO4 + Cu Fe + Cu2+ = Fe2+ + Cu
4Fe(OH)2 + O2 + 2H2O == 4 Fe(OH)3
2Fe(OH)3 Fe2O3+3H2O
Fe2O3+3H2O
2FeCl2 + Cl2=2FeCl3
2FeCl3+Fe=3FeCl2
2FeCl3+Cu=2FeCl2+CuCl2
FeCl3 + 3KSCN == Fe(SCN)3 + 3KCl Fe3+ + 3SCN- == Fe(SCN)3(红色溶液)
Fe + 2Fe3+ == 3Fe2+
2Fe3+ + Cu == 2Fe2+ + Cu2+
Fe3+ + 3OH- == Fe(OH)3↓
11、碳及其化合物的主要化学性质:
2C+O2(少量) 2CO
2CO
C+O2(足量) CO2
CO2
C+CO2 2CO
2CO
C+H2O CO+H2(生成水煤气)
CO+H2(生成水煤气)
C+2H2SO4(浓)  CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
C +4HNO3(浓)  CO2↑+4NO2↑+2H2O
CO2↑+4NO2↑+2H2O
2CO+O2 2CO2
2CO2
CO+CuO Cu+CO2
Cu+CO2
3CO+Fe2O3 2Fe+3CO2
2Fe+3CO2
CO2+H2O=H2CO3
CO2+Ca(OH)2(过量)=CaCO3↓+H2O Ca2+ + 2OH- + CO2 == CaCO3↓ + H2O CO2 + 2OH- == CO32- + H2O
2CO2(过量)+Ca(OH)2=Ca(HCO3)2 CO2 + OH- == HCO3-
CO2+NH3+NaCl+H2O=NaHCO3↓+NH4Cl(侯氏制碱法)
12、氮气、氨气及硝酸的主要化学性质:
N2+3H2 2NH3
2NH3
N2+O2 2NO
2NO
N2+3Mg Mg3N2
Mg3N2
2NO+O2=2NO2
3NO2+H2O=2HNO3+NO
4NH3+5O2 4NO+6H2O
4NO+6H2O
NH3+HCl=NH4Cl(白烟)
NH3 + H2O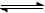 NH3·H2O
NH3·H2O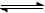 NH4+ + OH-
NH4+ + OH-
NH4HCO3 NH3↑+H2O+CO2↑
NH3↑+H2O+CO2↑
NH4Cl NH3+HCl
NH3+HCl
2NH4Cl + Ca(OH)2 CaCl2 + NH3↑ + H2O
CaCl2 + NH3↑ + H2O
NH4+ + OH- NH3↑+ H2O
NH3↑+ H2O
4HNO3 4NO2↑+O2↑+2H2O
4NO2↑+O2↑+2H2O
4HNO3(浓)+C  CO2↑+4NO2↑+2H2O
CO2↑+4NO2↑+2H2O
4HNO3+Cu=Cu(NO3)2+2NO2↑+2H2 2NO3- + Cu + 4H+ == Cu2+ + 2NO2↑+ 2H2O
8HNO3+3Cu=3Cu(NO3)2+2NO↑+4H2O 2NO3- + 3Cu + 8H+ == 3Cu2+ + 2NO↑+ 4H2O
13、硫及其化合物的化学性质:
S+H2 H2S
H2S
S+Fe FeS
FeS
S+2Cu Cu2S
Cu2S
S+O2 SO2
SO2
3S+6NaOH 2Na2S+Na2SO3+3H2O 3S + 6OH-
2Na2S+Na2SO3+3H2O 3S + 6OH- 2S2- + SO32- + 3H2O
2S2- + SO32- + 3H2O
SO2 + 2H2S=3S+2H2O
SO2+H2O=H2SO3
2NaOH+SO2(少量)=Na2SO3+H2O SO2 + 2OH-== SO32- + H2O
NaOH+SO2(足量)=NaHSO3 SO2 + OH- == HSO3-
2SO2+O2 2SO3
2SO3
2H2SO4(浓)+C CO2↑ +2SO2↑+2H2O
CO2↑ +2SO2↑+2H2O
2H2SO4(浓)+Cu CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
Na2SO3+H2SO4 = Na2SO4+ SO2↑+ H2O SO32- + 2H+ == SO2↑+ H2O
14、铝及其化合物主要化学性质:
4Al+3O2 2Al2O3(纯氧)
2Al2O3(纯氧)
2Al+Fe2O3 Al2O3+2Fe
Al2O3+2Fe
2Al+3H2SO4=Al2(SO4)3+3H2↑ 2Al + 6H+ = 2Al3+ + 3H2↑
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
或
2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑ 2Al+2OH—+6H2O=2[Al(OH)4]—+3H2↑
Al2O3+3H2SO4=Al2(SO4)3+3H2O Al2O3+6H+=2Al3++3H2O
Al2O3+2NaOH+3H2O=2Na[Al(OH)4] Al2O3+2OH—+3H2O=2[Al(OH)4]—
2Al2O3(熔融) 3O2↑ + 4Al
3O2↑ + 4Al
2Al(OH)3 Al2O3+3H2O
Al2O3+3H2O
Al(OH)3+3HCl=AlCl3+3H2O Al(OH)3+3H+=Al3++3H2O
Al(OH)3+NaOH=Na[Al(OH)4] Al(OH)3+OH—=[Al(OH)4]—
AlCl3+3NaOH=Al(OH)3↓+3NaCl Al3+ + 3OH- == Al(OH)3↓
AlCl3+3NH3·H2O=Al(OH)3↓+3NH4Cl Al3+ + 3NH3.H2O == Al(OH)3↓+ 3NH4+
AlCl3+3NaHCO3=Al(OH)3↓+3CO2↑ Al3+ + 3HCO3- == Al(OH)3↓ + 3CO2↑
15、硅及其化合物主要化学性质:
Si(粗)+2Cl2 SiCl4
SiCl4
SiCl4+2H2 Si(纯)+4HCl
Si(纯)+4HCl
Si(粉)+O2 SiO2
SiO2
Si+2NaOH+H2O=Na2SiO3+2H2 Si + 2OH- + H2O == SiO32- + 2H2↑
2C+SiO2 Si+2CO(制得粗硅)
Si+2CO(制得粗硅)
4HF+SiO2=SiF4+2H2O
SiO2+CaO CaSiO3
CaSiO3
SiO2+2NaOH=Na2SiO3+H2O (常温下强碱缓慢腐蚀玻璃)
SiO2+Na2CO3 Na2SiO3+CO2
Na2SiO3+CO2
SiO2+CaCO3 CaSiO3+CO2
CaSiO3+CO2
2NaOH+SiO2=Na2SiO3+H2O SiO2 + 2OH- == SiO32- + H2O
Na2SiO3 + CO2 + H2O == H2SiO3↓+ Na2CO3 SiO32- + CO2 + H2O == H2SiO3↓+ CO32-
16、镁、铜等单质及化合物的性质:
2Mg+O2 2MgO
2MgO
Mg + 2H2O = 2Mg(OH)2↓ + H2↑
Mg + Cl2 MgCl2
MgCl2
2Mg +CO2 2MgO+C
2MgO+C
Mg + H2SO4= MgSO4 + H2↑ Mg + 2H+ == Mg2+ + H2↑
MgO + 2HCl = MgCl2 +H2O MgO + 2H+ == Mg2+ + H2O
Mg(OH)2 + 2HCl = MgCl2 +2H2O Mg(OH)2 + 2H+ = Mg2+ + 2H2O
MgCl2+2NaOH=Mg(OH)2↓+2NaCl Mg2+ + 2OH- = Mg(OH)2↓
2Cu +O2 2CuO
2CuO
2Cu +S  Cu2S
Cu2S
Cu+ Cl2 CuCl2
CuCl2
CuO+H2SO4=CuSO4+H2O CuO + 2H+ == Cu2+ + H2O
Cu(OH)2+H2SO4=CuSO4+2H2O Cu(OH)2 + 2H+ == Cu2+ + 2H2O
Cu(OH)2 CuO + H2O
CuO + H2O
Cu2(OH)2CO3 2CuO + CO2↑+ H2O
2CuO + CO2↑+ H2O
CuCl2+2NaOH=Cu(OH)2↓+2NaCl Cu2+ + 2OH-== Cu(OH)2↓
CuSO4+H2S=CuS↓+H2SO4 Cu2+ +H2S=CuS↓+2H+
