高中有机化学总结
一、烃知识归纳总结:
1、(1)烃的分类 饱和链烃——烷烃CnH2n+2 (n≥1) 链烃 烯烃CnH2n (n≥2) 不饱和链烃—— 烃 炔烃CnH2n-2 (n≥2) 芳香烃(如苯及其同系物)CnH2n-6 (n≥6)
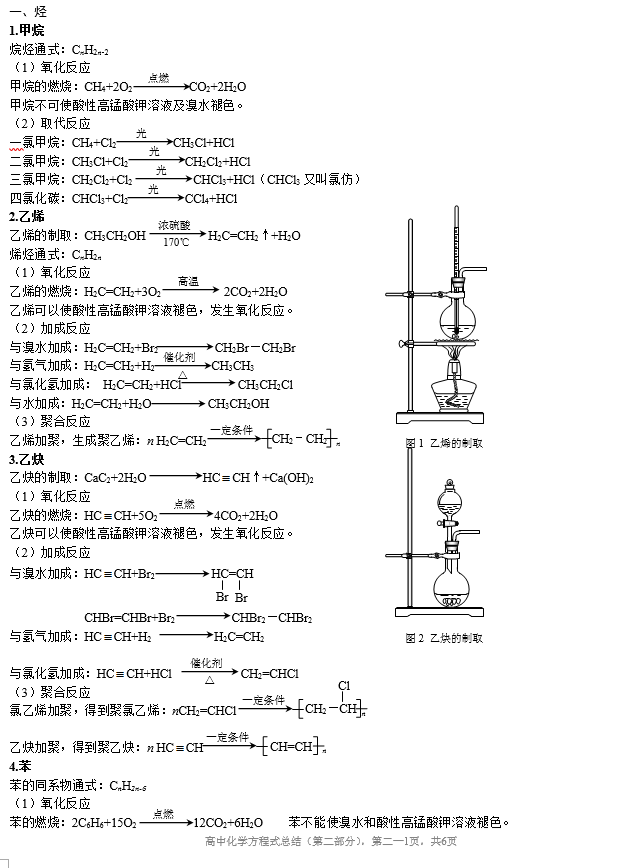
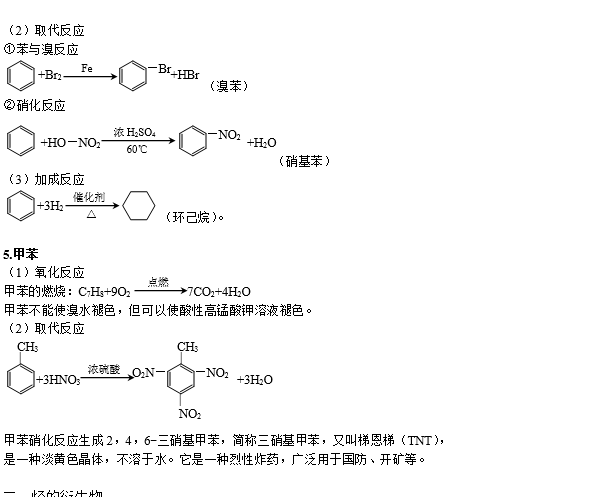
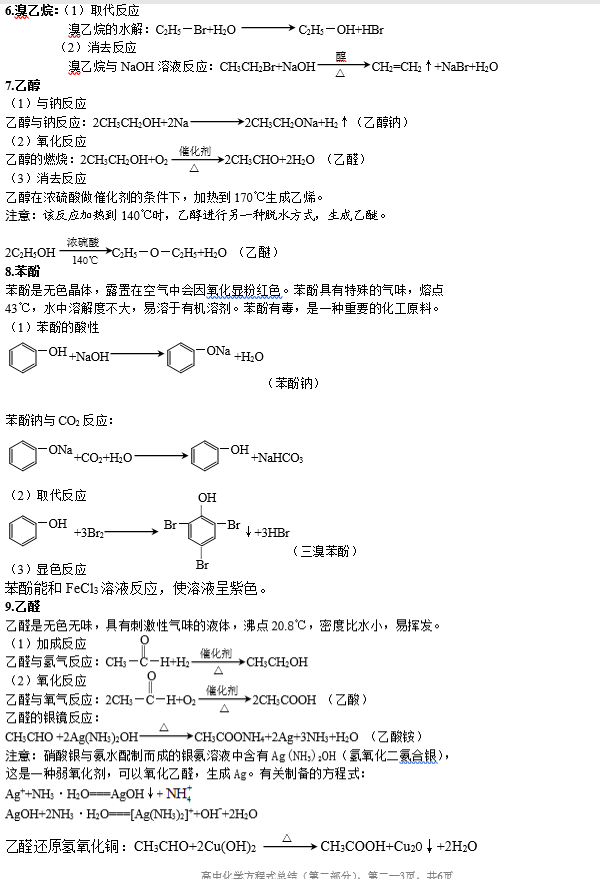
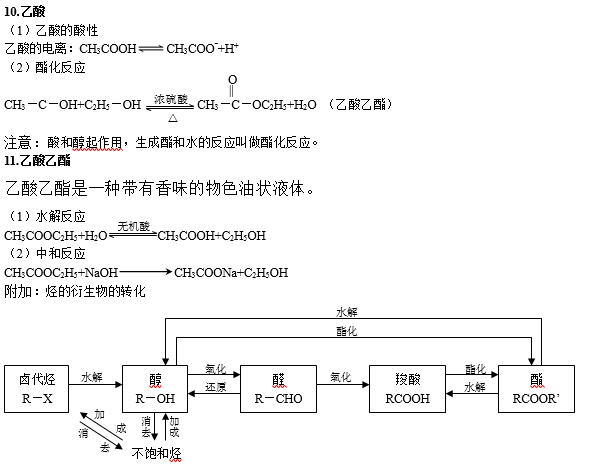
(2)各类烃的结构特点和主要化学性质 结构特点 主要化学性质 烷烃 仅含C—C键 与卤素等发生取代反应、热分解 烯烃 含C==C键 与卤素等发生加成反应,与高锰酸钾发生氧化反应,聚合反应 炔烃 含C≡C键 与卤素等发生加成反应,与高锰酸钾发生氧化反应,聚合反应 苯(芳香烃) 与卤素等发生加成反应,与氢气等发生加成反应。
2、几个重要的概念
(1)同系物:结构相似,在分子组成上相差一个或若干个CH2原子团的物质,互称为同系物; (2)同分异构现象:化合物具有相同的分子式,但具有不同的结构式的现象,叫做同分异构现象; (3)同分异构体:具有同分异构现象的化合物互称为同分异构体;
4、几种重要的有机化学反应类型
(1)氧化反应:包括两层含义①与氧气的燃烧②能否被酸性KMnO4溶液氧化; (2)取代反应:有机物分子里的某些原子团或原子被其他原子或原子团所代替的反应叫取代反应。如烷烃与卤素的反应、苯与液溴的反应、苯的硝化、磺化反应等均属取代反应; (3)加成反应:有机物分子里不饱和碳原子与其他原子或原子团直接结合生成新化合物的反应叫加成反应。如乙烯与溴及其他卤素或氢气的反应、乙炔与卤素的反应等均属加成反应; (4)聚合反应:由相对分子质量小的化合物分子结合成相对分子质量大的高分子的反应叫做聚合反应。如乙烯的聚合、氯乙烯的聚合均属聚合反应;
5、烷烃的系统命名法
系统命名法的基本原则有:①最简化原则;②明确化原则;可解释为一长一近一多一少即主链要长,编号起点离支链最近,支链数目要多,支链位置号码之和要少。 系统命名法的基本步骤可归纳为:①选主链,称某烷;②编号码,定支链;③取代基,写在前,注位置,连短线;④不同基,简在前,相同基,二三连。
…… …… 余下全文

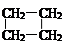
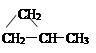 CH3CH=CHCH3、CH2=C(CH3)2、 、
CH3CH=CHCH3、CH2=C(CH3)2、 、

 ⑷ CnH2n-6:芳香烃(苯及其同系物)。如: 、 、
⑷ CnH2n-6:芳香烃(苯及其同系物)。如: 、 、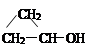
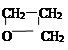
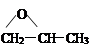 、 、
、 、