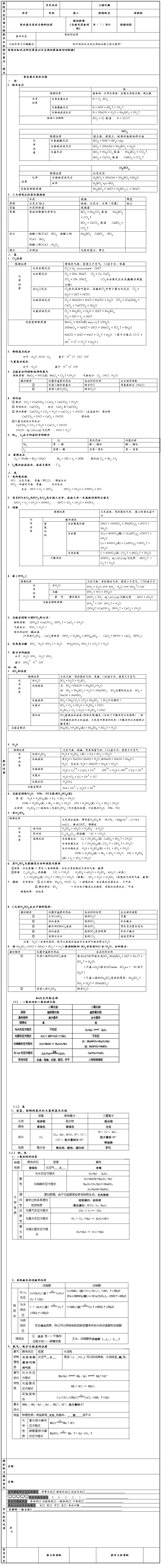
沙头角中学高一化学资料 元素化合物知识总结
元素化合物知识总结
一、各类物质所具有的⑵与碱中和生成对应通性总结: 的盐和水
1、金属单质的通性: ⑶与碱性氧化物化合⑴与非金属单质(如生成对应的盐
Cl2、O2、H2、S、N2、4、碱性氧化物的通性: C等)反应 ⑴与水反应生成对应⑵与酸反应 的碱
⑶与水反应 ⑵与酸中和生成对应⑷与盐发生置换反应 的盐和水
2、非金属单质的通性: ⑶与酸性氧化物化合⑴与非金属单质(如生成对应的盐
Cl2、O2、H2、S、N2、5、酸的通性:
C等)反应 ⑴与指示剂变色(与石⑵与金属单质(如钠、蕊变红,与甲基橙变铁、镁、铝、铜等)反红)
应 ⑵与活泼金属反应生⑶与碱反应 成低价态的盐和氢气 ⑷与水反应 ⑶与碱发生中和反应 ⑸与盐反应 ⑷与碱性氧化物反应
3、酸性氧化物的通性: ⑸与盐反应生成新酸⑴与水反应生成对应和新盐
的酸 6、碱的通性:
~ 1 ~
沙头角中学高一化学资料 元素化合物知识总结
⑴与指示剂变色(与石
蕊变蓝,与甲基橙变
黄)
⑵与非金属反应
⑶酸发生中和反应
⑷酸性氧化物反应
⑸盐反应生成新碱和
新盐
7、盐的通性:
二、研究各类物质性质的方法 ⑴与金属单质发生置换反应 ⑵与非金属单质发生置换反应 ⑶酸反应生成新酸和新盐 ⑷碱反应新碱和新盐 ⑸盐反应生成两种新盐
1、物理性质:颜色、气味、状态、有没有毒性、密度、熔沸点、硬度、柔韧性、导电导热性、溶解性(主
要是在水中的溶解度)等。
2、化学性质:
⑴根据物质类别分析其应有的通性:
⑵从以下几个方面分析物质可能具有的特性:
①分析化合价,总结其氧化性或还原性;②吸水性;③漂白性;④脱水性;⑤腐蚀性;⑥其他违反规律的可能性质
三、纵线(即同主族)归纳元素单质及其化合物性质的方法过程
…… …… 余下全文