实验报告:检测生物组织中的糖类、脂肪和蛋白质
一、 实验原理:
1. 某些化学试剂能使生物组织中得有关化合物产生特定的 反应。
2. 糖类中的还原糖,如 、 与 发生作用,生成 。
3. 脂肪可以被 染成橘黄色,或被 染成红色。
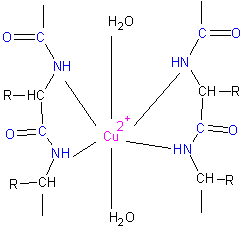
4. 蛋白质与 发生作用,产生 反应。
二、 材料用具:
实验材料:苹果或 梨匀浆,花生种子,豆浆。
用具:双面刀片,试管,试管夹,大小烧杯,小量筒,三脚架,石棉网,火柴,载玻片,盖玻片,毛笔,吸水纸,显微镜等。
试剂:斐林试剂,甲液:质量浓度为 ,乙液:质量浓度为 ;苏丹Ⅲ或苏丹Ⅳ染液,双缩脲试剂:A液:质量浓度为 ,B液质量浓度为 。
三、 方法步骤:
(一) 还原糖的检测和观察
①向试管内注入2ml 。(选择具体材料)
②向试管内注入 斐林试剂,(甲液和乙液 再注入。)
③将试管放入盛有 的大烧杯中加热 。
④观察试管中出现的颜色变化。
(二) 脂肪的检测和观察
…… …… 余下全文


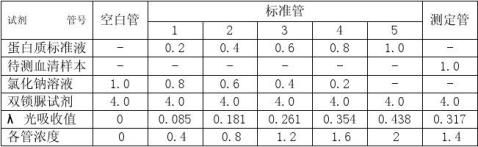
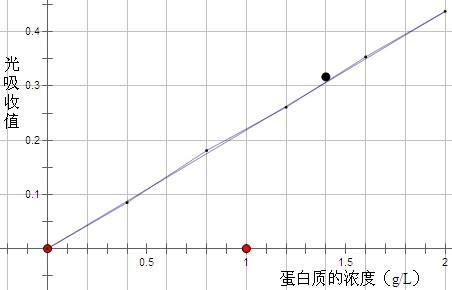


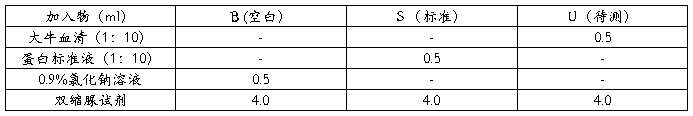
 取3支试管,做好标记(B空白对照,S标准液,U为待测大牛血清),按下表操作:
取3支试管,做好标记(B空白对照,S标准液,U为待测大牛血清),按下表操作: