ds区元素(铜、银、锌、镉、汞)的性质
一、实验目的
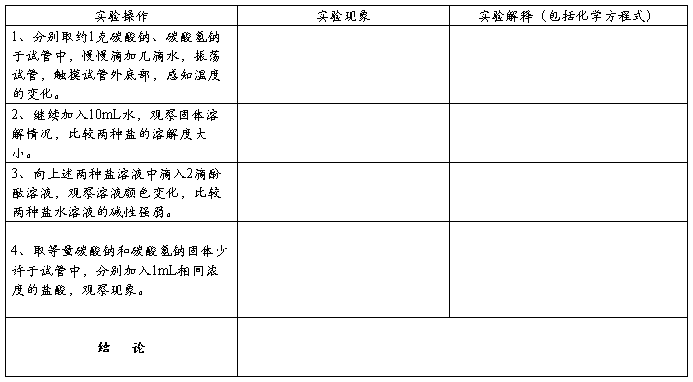
1、掌握铜、锌氢氧化物的酸碱性;
2、掌握铜、银、锌、汞的配合物的生成和性质;
6、掌握铜、银、锌、汞离子的分离与鉴定方法。
二、实验原理
IB IIB
Cu Zn Cu(+2,+1) Zn(+2)
Ag Cd Ag(+1) Cd(+2)
Au Hg Au(+1,+3) Hg(+2,+1)
蓝色的Cu(OH)2呈现两性,在加热时易脱水而分解为黑色的CuO。AgOH在常温下极易脱水而转化为棕色的Ag2O。Zn(OH)2呈两性,Cd(OH)2显碱性,Hg(I, II)的氢氧化物极易脱水而转变为黄色的HgO(II)和黑色的Hg2O(I)。
易形成配合物是这两副族的特性,Cu2+、Ag+、Zn2+、Cd2+与过量的氨水反应时分别生成[Cu(NH3)4]2+、[Ag(NH3)2]+、[Zn(NH3)4]2+、[Cd(NH3)4]2+。但是Hg2+和Hg22+与过量氨水反应时,如果没有大量的NH4+存在,并不生成氨配离子。如:
HgCl2 + 2NH3 = Hg(NH2)Cl↓白+ 2 NH4Cl
Hg2Cl2 + 2NH3 = Hg(NH2)Cl↓白+ Hg↓黑+NH4Cl (观察为灰色)
Cu2+具有氧化性,与I-反应,产物不是CuI2,而是白色的CuI:
…… …… 余下全文