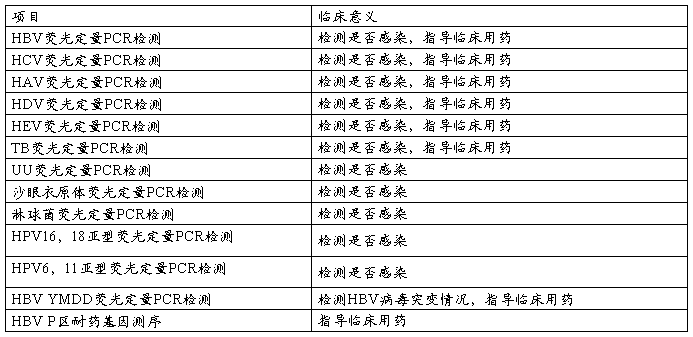
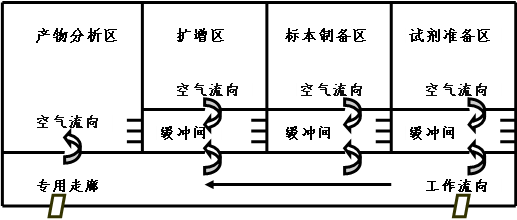
如何看化验报告单
检验报告单是检查所得出的客观数据记录。检验项目很多,这里只从定性和定量两个方面,概略地作一介绍。定性检验,是看送检的标本中有没有“待检物”。一般来说,有待检物存在,报告为“阳性”,反之报告“阴性”。正常时不应有的待检物出现了,称为“阳性”,即为不正常。定量检验表示检验标本中待检物含量的多少。不同地区不同方法测出的检验参考值略有差异,参考值不等于正常值,只是一个正常范围。
⑴ 三大常规 即血、尿、粪常规检查。
血常规包括血红蛋白测定、红细胞计数、白细胞计数及白细胞分类计数4项。
血红蛋白(Hb):正常男性为120-160g/L,女性为110-150g/L;红细胞(RBC)计数:正常男性为4.0-5.5×1012/L,&127;女性为3.5-5.0×1012/L,新生儿为6.0-7.0×1012/L。血红蛋白及红细胞增多,常见于脱水所致血液浓缩或慢性组织缺氧等;其减少则常见于各种贫血;
白细胞(WBC)计数:正常成人为4-10×109/L,新生儿为15-20×109/L,8个月至2岁婴儿为11-12×109/L。白细胞增多常见于炎性感染、出血、中毒、白血病等。其减少常见于流感、麻疹等病毒性传染病及严重败血症、药物或放射线所致及某些血液病等。
白细胞分类计数:白细胞分为5类,
1、中性白细胞,正常为0.50-0.70,&127;增高或减少的原因与白细胞计数相同;
2、淋巴细胞,正常为0.2-0.4,增多时常见于中性白细胞减少;其减少常见于中性白细胞增多;
3、嗜酸性粒细胞,正常为0.005-0.05,增多见于寄生虫病、过敏性疾病及某些皮肤病;
4、嗜碱性粒细胞,正常为0-0.0075,临床意义不大;
5、单核细胞,正常为0.01-0.08,增多时见于急性传染病恢复期。
尿常规包括物理学检查、化学检查及显微镜检查三项。物理学检查主要是观察颜色、透明度、测尿比重。正常尿比重波动范围大,一般在1.015-1.020之间。比重增高,见于高热、糖尿病等;比重低,见于慢性肾炎以及肾功能严重损害等。化学检查主要看酸碱反应、蛋白定性和糖定性。正常尿呈弱酸性或碱性,无蛋白,无糖,常用阴性“─”表示。尿中有蛋白见于肾炎、心衰、发热性疾病和泌尿道感染等;有糖则是糖尿病、显微镜检查主要看有无红细胞、白细胞、上皮细胞、各种管型及结晶等。正常尿中可有少量白细胞、上皮细胞及盐类结晶。如果出现红细胞、白细胞及管型,则有肾脏损害,如肾炎、泌尿系感染等。碱性尿常见磷酸盐结昌,服用磺胺药可见磺胺结晶。
…… …… 余下全文