
篇二 :EDTA标准溶液的标定和水的硬度测定(实验报告)
EDTA标准溶液的标定和水的硬度测定
(四川农业大学生命科学与理学院(625014)应用化学09-2 王雨20096824 )
【摘 要】本实验利用络合滴定法分别标定了EDTA标准溶液、测定了自来水的硬度。
首先,以CaCO3为基准物质、钙指示剂指示滴定终点标定了EDTA标准溶液的浓度,得到其平均浓度为0.01592 mol·L-1。再以铬黑T为指示剂、用标定后的EDTA测定了水的总硬为12.61±0.01(°),以钙指示剂为指示剂测得水的钙硬为9.46±0.01(°),
则有镁硬为3.15±0.01(°)。
【关键词 】EDTA ;标定 ;水 ;硬度
1引言
EDTA是乙二胺四乙酸或其二钠盐的简称(缩写为H4Y或Na2H2Y·2H2O),由于前者的溶解度小,通常用其二钠盐配制标准溶液。尽管EDTA可制得纯品,但EDTA具有与金属离子配位反应普遍性的特点,即使是水和试剂中的微量金属离子或器壁上溶出的金属离子也会与EDTA反应,故通常仍用间接法配制标准溶液。一般先配成浓度约为0.01mol·L-1的溶液,再用基准物质来标定,常用的基准物质是Zn、ZnO、CaCO3、Bi、Cu、MgSO4 7H2O、Hg、Ni、Pb等。本实验控制pH在12~13的酸度下,以钙指示剂指示终点滴定,用CaCO3作为基准物质进行滴定。
7H2O、Hg、Ni、Pb等。本实验控制pH在12~13的酸度下,以钙指示剂指示终点滴定,用CaCO3作为基准物质进行滴定。
首先,所加钙指示剂与少量Ca2+反应,形成具有“足够”稳定性的酒红色配合物,滴定过程中滴加的EDTA与游离的Ca2+配位形成更稳定的(与指示剂配合物比较)配合物,最后EDTA再夺取指示剂配合物中的Ca2+而指示剂游离出来,溶液呈现出指示剂自身(在一定pH范围)的纯蓝色而显示终点。其相关反应:
HIn2- (纯蓝色)+ Ca2+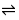 CaIn-(酒红色) +H+
CaIn-(酒红色) +H+
…… …… 余下全文
篇三 :水硬度的测定实验报告
EDTA溶液的配制与标定和水中硬度的测定
实验日期: 年 月 日
处理对象:
实验内容:EDTA溶液的配制与标定和水中硬度的测定
实验原理:
1.EDTA标准溶液的配制(0.01mol/L)——间接法
m=cVM
2.EDTA标准溶液的标定
以与被测物性质相似的物质(CaCO3)作为基准物质标定EDTA溶液。
滴定条件:pH=10(NH3-NH4Cl作为缓冲溶液,其中加入镁溶液,以便用铬黑T作为指示剂)。
标定中的反应
滴定前:Ca2++MgY2-?CaY2-+Mg2+
Mg2++HIn2-?MgIn-+H+
滴定反应:Ca2++H2Y2-?CaY2-+2H+
化学计量点时:MgIn-+H2Y2-?MgY2-+HIn2-
标定结果的计算
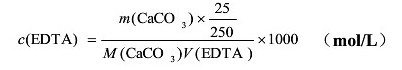
3.水中总硬度的测定
测定中的反应
滴定前:Ca2++MgY2-?CaY2-+Mg2+
Mg2++HIn2-?MgIn-+H+
滴定反应:Ca2++H2Y2-?CaY2-+2H+
Mg2++H2Y2-?MgY2-+2H+
化学计量点时:MgIn-+H2Y2-?MgY2-+HIn2-
测定结果的计算

…… …… 余下全文
篇四 :(十)自来水总硬度的测定
实验十六 配位滴定
(一)自来水总硬度的测定
【目的要求】
1、学习EDTA标准溶液的配制和标定;
2、了解配位滴定法测定自来水总硬度的原理、条件和方法。
【实验原理】
1、Ca2+、Mg2+是决定自来水总硬度的主要离子。用EDTA标准溶液滴定自来水,测定其中Ca2+、Mg2+的总浓度,转换为CaO的浓度,即可得到以CaO为指标测定的自来水的总硬度。
2、本实验采用配位滴定法,滴定剂是EDTA标准溶液,指示剂为K-B指示剂。在pH=10的氨性缓冲溶液中,通过加入三乙醇胺(掩蔽Fe3+、Al3+等)、Na2S(掩蔽Cu2+、Zn2+、Pb2+等),确保只有Ca2+、Mg2+被滴定。滴定时,为提高终点的敏锐性,通常在EDTA溶液中加入适量Mg2+,因为Mg-KB的稳定性大于Ca-KB,滴定过程中,Ca2+把Mg-EDTA中的Mg2+置换出来;终点时,EDTA把Mg-KB中的Mg2+夺出,溶液由紫红色变成蓝绿色。
3、计算公式:
【实验步骤】
1、CaCO3标准溶液的配制。
①在电子天平上准确称取0.08~0.09g CaCO3,置于小烧杯中。
②先用适量水润湿,盖上表面皿,缓缓滴加HCl(1:1,6.0mol·L-1)20mL。
③溶解后,定容于200mL容量瓶,,计算其准确浓度。
2、EDTA标准溶液的配制与标定。
①用台秤称取0.5g EDTA于小烧杯中,再用加重法在分析天平上向小烧杯中加入0.025g MgCl2·6H2O。
②向小烧杯中加入去离子水50mL,加热搅拌至固体溶解,冷却,稀释至300mL,转入试剂瓶中。
③用移液管移取25.00mLCaCO3标准溶液至250mL锥形瓶中,加入20mL氨性缓冲溶液和两滴K-B指示剂,用EDTA溶液滴定至由紫红色变为蓝紫色,即为终点,平行滴定三份取平均值。
3、水样总硬度的测定。
…… …… 余下全文
篇五 :实验报告格式-天然水总硬度的测定
实验报告格式:
实验日期: 实验地点: 指导教师: .
实验名称: 天然水总硬度的测定 .
一、实验目的:
(1)掌握EDTA标准溶液的配置和标定方法。
(2)掌握EBT指示剂的使用条件和终点变化。
(3)掌握EDTA法测定水的总硬度的方法和原理。
…… …… 余下全文
篇六 :实验五 自来水总硬度的测定 (EDTA的标定)
实验五 自来水总硬度的测定 (EDTA的标定) (4学时)
一、实验目的
1. 掌握EDTA标准溶液的配制和标定原理。了解EDTA的性质和用途.
2.了解水的硬度测定的意义和常用的硬度表示方法;
3.掌握EDTA测定水的硬度的原理和方法;
4.掌握铬黑T和钙指示剂的应用,了解金属指示剂的特点
二、水硬度的表示法
一般所说的水硬度就是指水中钙、镁离子的含量。最常用的表示水硬度的单位有:
1. 以度表示,1o=10 ppm CaO,相当10万份水中含1份CaO。
2. 以水中CaCO3的浓度(ppm)计相当于每升水中含有CaCO3多少毫克。
MCaO—氧化钙的摩尔质量(56.08 g/mol),
MCaCO3—碳酸钙的摩尔质量(100.09 g/mol)。
三、测定原理
测定水的总硬度,一般采用配位滴定法即在pH=10的氨性溶液中,以铬黑T作为指示剂,用EDTA标准溶液直接滴定水中的Ca2+、Mg2+,直至溶液由紫红色经紫蓝色转变为蓝色,即为终点。反应如下:
滴定前:EBT + Me(Ca2+、Mg2+)= Me-EBT
(蓝色) pH=10 (紫红色)
滴定开始至化学计量点前:H2Y2- + Ca2+ = CaY2- + 2H+
H2Y2- + Mg2+ = MgY2- + 2H+
…… …… 余下全文
篇七 :化学实验技能操作大赛——自来水硬度的测定


实验室用自来水总硬度测定报告
参赛小组成员:郑玉波、李文
水的总硬度测定
——“实验技能操作大赛”实验室用自来水总硬度分析
20##年11月5日
化学工程与食品科学学院实验室(N3-305)
实验技能大赛第十组参赛小组

…… …… 余下全文
篇八 :实验5 自来水总硬度的测定(讲稿)
实验五 自来水总硬度的测定
一、实验目的
1、掌握EDTA法测定水的总硬度的原理和方法。
2、掌握EDTA标准溶液的配制和标定方法。
3、掌握水硬度的表示方法及计算。
二、实验原理
水的硬度是表示水质的一个重要指标,对工农业用水、饮用水关系很大。所谓水的硬度是指水中各种可溶性钙盐和镁盐的含量,它包括暂时硬度和永久硬度。暂时硬度主要是指水中含钙、镁的酸式碳酸盐,加热能析出沉淀而除去;永久硬度是指钙、镁的硫酸盐、硝酸盐和氯化物,它们在加热时不沉淀。
水的总硬度的测定,一般采用EDTA配位滴定法。在pH=10的氨性缓冲溶液中,以铬黑T为指示剂,用EDTA标准溶液直接测定水中Ca2+、Mg2+总量,终点由紫红色变为纯蓝色。若有Fe3+、Al3+干扰,可用三乙醇胺掩蔽,Cu2+、Pb2+、Zn2+等重金属离子可用KCN、Na 2S予以掩蔽。
滴定前: EBT + Mg2+ ═ Mg-EBT
(蓝色) (紫红色)
化学计量点前:Ca2+ + H2Y2- ═ CaY2- + 2H+
Mg2+ + H2Y2- ═ MgY2- + 2H+
化学计量点: Mg-EBT + H2Y2- ═ MgY2- + EBT + 2H+
(紫红色) (蓝色)
…… …… 余下全文

推荐阅读
猜你喜欢
