大学化学基础实验II实验报告
课程名称:有机化学实验
实验名称:乙酰苯胺的合成与测定
姓 名:张玉
学 号:1108110191
专 业:化学工程与工艺
班 级:化工113
实验日期:

5/25
? 实验目的
1.分馏的原理和操作;
2. 掌握苯胺乙酰化反应的原理和操作;
3. 学习掌握固体化合物重结晶提纯的原理和方法。 ? 实验原理 NH

2

+CH3COOHONHCH3+H2O苯胺(C6H5NH2)与乙酰基化试剂如冰HAc、(CH3CO)2O、CH3COCl等反应可制得乙酰苯胺。
苯胺与CH3COCl反应速度最快,(CH3CO)2O次之,冰HAc最慢。
但冰HAc价格便宜,操作方便,为常用乙酰基化试剂。 其反应方程式为
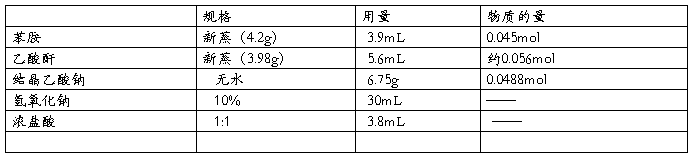
? 实验药品
1.苯胺 5.1g 5ml (0.055moL)
冰醋酸 7.8g 7.4ml (0.13moL)
活性炭0.1g
2.器材:锥形瓶50ml一个 温度计200 ℃一支 量筒10ml一个100ml一个
烧杯250ml两个 圆底烧瓶50 ml 玻璃棒一根 结尾 管一个分馏柱一个 分馏头一个
? 实验步骤
1.0ml圆底烧瓶中加入5ml新蒸馏的C6H5NH2(0.055mol)、
7.4mlCH3COOH(0.13mol)及1-2粒沸石。依次安装分馏柱、蒸馏头、温度计、接液管,接液管伸入10ml小量筒内,收集蒸出的水和乙酸。
2.精灯将溶液缓慢加热,使反应物保持微沸约15min。然后逐渐升高温度,保持温度计读数在100-105℃,约经过45min,
反应生成的水及部分醋酸可蒸出(约4ml)。当温度计的读数下降时,反应即达终点,停止加热。
3.断搅拌下,将反应物趁热慢慢倒入盛有100ml冷水的烧杯中,继续搅拌,充分冷却,使粗乙酰苯胺成细粒状完全析出。抽滤,用5~10ml冷水洗涤粗产品。将粗产品转移到盛有100ml热水的烧杯中,加热至沸,如果仍有未溶解的油珠,需补加热水,直到油珠溶解完全,再多加20%的热水。稍冷,加入0.2g活性炭,煮沸几分钟,趁热用热水漏斗过滤,冷却滤液,待析出晶体后,抽滤,将产品转移至一个预先称重的表面皿中,晾干或置于烘箱中在100℃以上烘干。称重,熔点114℃
…… …… 余下全文
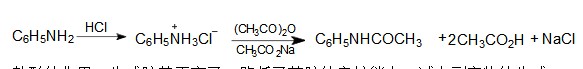

 (mw)
(mw)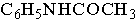
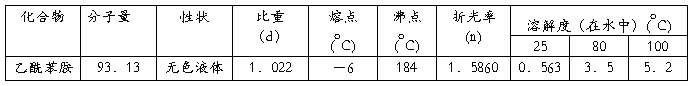
 反应方程式:
反应方程式: