实验五 电导滴定分析法测定未知酸
一.实验目的
1. 掌握电导率仪结构和测定溶液电导值的基本操作;
2.了解电导电极的结构和使用;
3.掌握电导滴定的基本原理和判断终点的办法。
二.实验原理
在滴定分析中,一般采用指示剂来判断滴定终点,但是稀溶液的滴定终点突跃甚小,而有色溶液的颜色会影响对指示剂在终点时颜色变化的判断,因此在稀溶液和有色溶液的滴定分析中,无法采用指示剂来判断终点。
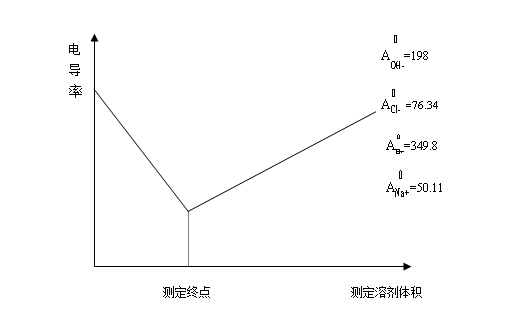
本实验借助于滴定过程中离子浓度变化而引起的电导值的变化来判断滴定终点,这种方法称为电导滴定。NaOH溶液与HCL溶液的滴定中,在滴定开始时,由于氢离子的极限摩尔电导值较大,测定的溶液电导值也较大;随着滴定进行,H+和OH-离子不断结合生成不导电的水,在H+浓度不断下降的同时增加同等量的Na+离子,但是Na+离子导电能力小于H+离子,因此溶液的电导值也是不断下降的;在化学计量点以后,随着过量的NaOH溶液不断加入,溶液中增加了具有较强导电能力的OH-离子,因而溶液的电导值又会不断增加。由此可以判断,溶液具有最小电导值时所对应的滴定剂体积即为滴定终点。
三:实验仪器与试剂
1.DDS-307型电导率仪 2.DJS-1C型电导电极
3.85-1磁力搅拌器一台 4.0.1000mol/L NaOH标准溶液
5.未知浓度HCL溶液 6.10ml移液管1只
7.100ml玻璃烧杯1个
…… …… 余下全文



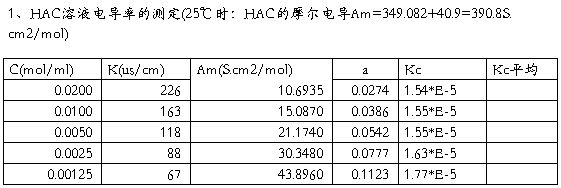
 1、电导G:对于电解质溶液,常用电导表示其导电能力的大小。电导G是电阻R的倒数,即 G=1/R。电导的单位是西门子,常用S表示。1S=1Ω-1
1、电导G:对于电解质溶液,常用电导表示其导电能力的大小。电导G是电阻R的倒数,即 G=1/R。电导的单位是西门子,常用S表示。1S=1Ω-1 (2.5.3)
(2.5.3) (1)
(1) (2)
(2) 总是随着溶液的浓度降低而增大的。
总是随着溶液的浓度降低而增大的。 (3)
(3)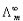 是溶液在无限稀释时的极限摩尔电导率。A为常数,故将
是溶液在无限稀释时的极限摩尔电导率。A为常数,故将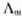 对
对 作图得到的直线外推至C=0处,可求得
作图得到的直线外推至C=0处,可求得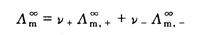 (4)
(4)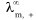 、
、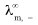 分别表示正、负离子的无限稀释摩尔电导率。
分别表示正、负离子的无限稀释摩尔电导率。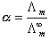 (5)
(5)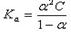 (6)
(6) (1)
(1)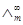 (S·m2·mol-1)
(S·m2·mol-1)