重结晶及过滤实验实验报告
实验时间:2010.04..01 报告人;武伟
一、实验目的
学习和掌握重结晶法纯化固体有机物的基本原理和实验技术。
二、实验原理
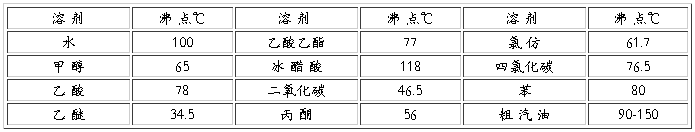
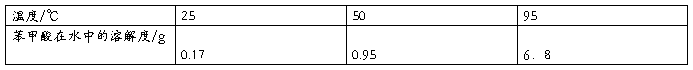
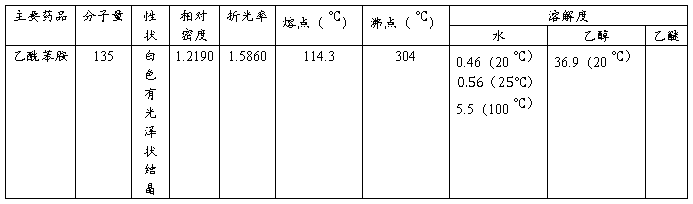
利用混合物中各组分在某种溶剂中溶解度不同或在同一溶剂中不同温度时的溶解度不同而使它们相互分离。固体有机物在溶剂中的溶解度随温度的变化易改变,通常温度升高,溶解度增大;反之,则溶解度降低,热的为饱和溶液,降低温度,溶解度下降,溶液变成过饱和易析出结晶。利用溶剂对被提纯化合物及杂质的溶解度的不同,以达到分离纯化的目的。
三、实验用品
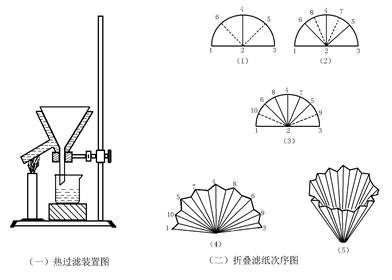
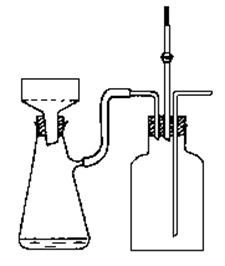
仪器:布氏漏斗、吸滤瓶、抽气管、安全瓶、锥形瓶、循环水真空泵、玻璃棒、表面皿、电炉、滤纸、量筒、刮刀。
四、实验操作步骤和现象
将2 g粗制的乙酰苯胺及70mL的水加入250mL的三角烧瓶中,加热至沸腾,直到乙酰苯胺溶解(若不溶解可适量添加少量热水,搅拌并热至接近沸腾使乙酰苯胺溶解)。取下烧瓶稍冷后再加入计量的活性炭于溶液中,煮沸5-10分钟。趁热用布氏漏斗进行过滤,用一烧杯收集滤液。滤液放置彻底冷却,待晶体析出,抽滤出晶体,并用少量溶剂(水)洗涤晶体表面,抽干后,取出产品放在表面皿上晾干或烘干,称量。
五、产率计算
共得到0.9 g乙酰苯胺产品,粗品的质量为2 g,产率为
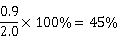
六、思考题
1. 重结晶纯化有机物的原理是什么?
答:原理是有机物在同一溶剂中不同温度下的溶解度差别较大。
2. 理想溶剂具备那些条件?
答:不与溶质反应,溶质的溶解度在不同温度下差别较大。
3. 乙酰苯胺重结晶时出现油珠的原因是什么?
…… …… 余下全文