ʵ�� ����ϼ�ķ�����ʵ�鱨��
�� ���� �� ���� �� �ţ� ���ڣ�
һ��ʵ��Ŀ�ģ�
����ԭ����
����ʵ�鲽������ͼ��
�ġ�ʵ���������ۣ�
1. mol·L-1HCl��ҺŨ�ȵı궨
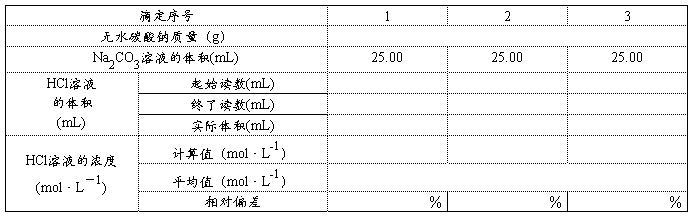
HCl��Һ��Ũ���� mol·L-1
2. ��ϼ�ķ���

���ۣ���ϼ���Һ������ǣ�NaOH mol·L-1��NaHCO3 mol·L-1��
���� ���� ����ȫ��
ʵ�� ����ϼ�ķ�����ʵ�鱨��
�� ���� �� ���� �� �ţ� ���ڣ�
һ��ʵ��Ŀ�ģ�
����ԭ����
����ʵ�鲽������ͼ��
�ġ�ʵ���������ۣ�
1. mol·L-1HCl��ҺŨ�ȵı궨

HCl��Һ��Ũ���� mol·L-1
2. ��ϼ�ķ���

���ۣ���ϼ���Һ������ǣ�NaOH mol·L-1��NaHCO3 mol·L-1��
���� ���� ����ȫ��
��ҵ����רҵʵ��
��ϼ�IJⶨ��˫ָʾ������
�� ���� ������
רҵ�༶�� Ӧ��0704��
ѧ �ţ� 07220413
�� �ڣ� 20##��3��19��
ָ����ʦ�� ��Ƽ
ʵ��һ ��ϼ�ķ���
һ�� ժҪ
ͨ�������ʵ�Ũ�ȵ�HCl��Ȼ���÷�������ˮNa2CO3���б궨����ȷ����4 g���ҵĻ�ϼ��������ܽ�����ѱ궨��HCl����Һ������˫ָʾ�������еζ�������ǰ����������HCl������ж������ijɷ֡����������������ΪNa2CO3��NaHCO3 �Ļ���
����ʵ��Ŀ��
1.����HCl����Һ�����ƺͱ궨�����Լ���Һ�ܵ�ʹ�á�
2.������˫ָʾ�����жϻ�ϼ����ɼ��ⶨ����ֺ�����ԭ���ͷ���
3.��һ�������ζ������͵ζ��յ���ж�
����ʵ��ԭ��
��ϼ���NaOH;��Na2CO3��NaHCO3��Na2CO3�Ļ������ⶨ�����и���ֵĺ���������HCl����Һ�ζ������ݵζ�������pHֵ�仯�������ѡ�����ֲ�ͬ��ָʾ���ֱ�ָʾ��һ���ڶ��յ�ĵ������˫ָʾ��������
���� ���� ����ȫ��
ʵ��ʮһ ��ϼ�ķ�����˫ָʾ������
һ��ʵ��Ŀ��
�� ��һ�������ζ������͵ζ��յ���жϣ�
�� ���ջ�ϼ�����IJⶨԭ���������ͼ��㡣
����ʵ��ԭ��
��ϼ���NaOH ��Na2CO3����Na2CO3 �� NaHCO3�Ļ�������˫ָʾ���������Բⶨ����ֵĺ�����
���ȣ��ڼ�Һ�м����ָ̪ʾ������HCl����Һ�ζ�����Һ�Դ��ۺ�ɫ����Ϊ��һ��ѧ�����㣬��Ӧ���£�
NaOH + HCl = NaCl+ H2O
Na2CO3+ HCl = NaHCO3 +H2O
��ʱ��Ӧ����ΪNaHCO3��NaCl����ҺpHΪ8.3����������HCl��Һ�����ΪV1��ml����
Ȼ�����������ָʾ������HCl����Һ�ζ�����Һ�ɻ�ɫת��Ϊ��ɫ����Ϊ�ڶ���ѧ�����㣬��Ӧ���£�
NaHCO3 + HCl = NaCl + H2O + CO2��
��ʱ��ҺpHΪ3.7����������HCl��Һ�����ΪV2��ml����
����V1��V2�ɼ����ռ���NaOH��Na2CO3�ĺ�����
����ʵ���Լ�
��ϼ�����������ָʾ����1g/Lˮ��Һ������ָ̪ʾ����2g/L�Ҵ���Һ����HCl����Һ
�ġ�ʵ������
������ƽ(����)������ƿ(����)���ձ�(1)������ƿ(1)����Һ��(1)��������(1)����ƿ(3)����ʽ�ζ���(1)
�塢ʵ�鲽��
1����ϼ���Һ������
�õݼ�������ȷ��ȡ0.83-0.85g���������ձ��У�������ȥ����ˮ�ܽ��ת�Ƶ�����
ƿ�ж��ݡ�
2����һ�յ�ĵζ�
����Һ����ȡ��Һһ�ݣ�������ƿ�У�����������ˮ���ټ�2~3�η�ָ̪ʾ������
HCl����Һ�ζ�����Һ�ɺ�ɫת��Ϊ��ɫ�����¶�����
3���ڶ��յ�ĵζ�
��������Һ���ټ�1 ~2�μ���ָʾ����������HCl����Һ�ζ�����Һ�ɻ�ɫת��
Ϊ��ɫ�����¶�����
���� ���� ����ȫ��
��ѧ����ҩ����ѧԺ
��ҵ����רҵʵ��
ʵ����Ŀ�� ��ϼ����
�� ���� Ӧ��0704 ѧ �ţ� 07220410
�� ���� ʵ�����ڣ�
ʵ����Ŀ����ϼ����
һ��ժҪ
��ʵ�����˫ָʾ������ͨ������һ��Ũ�ȵ�HCl���Ի�ϼ�����˶��ԺͶ����ķ������÷�������ˮNa2CO3���궨HClŨ�ȣ����������ζ���õĻ�ϼ���Һ������ǰ����������HCl������ж���Ʒ�еijɷ�ΪNa2CO3��NaHCO3 �Ļ������������ֵİٷֺ�����
����ʵ��Ŀ��
1.������Һ�ܵ�ʹ�ã�
2.����HCl����Һ�����ƺͱ궨������
3.ѧ����˫ָʾ�����ⶨ��ϼ��и���ֵĺ������������ֲ��ζ���ԭ����
4.ѧ���ϼ���ܼ�Ȳⶨ���������㡣
����ʵ��ԭ��
��ϼ���Na2CO3�� NaOH ��Na2CO3��NaHCO3�Ļ����ⶨͬһ�������и���ݵĺ���ʱ������HCl����Һ�ζ���ѡ�����ֲ�ָͬʾ���ֱ�ָʾ��һ���ڶ���ѧ������ĵ�����ݵ���������ѧ������ʱ���ĵ�HCl����Һ�����������б���������ɼ��������ݺ�����
���� ���� ����ȫ��
ʵ��� ��ϼ��и���ֺ����IJⶨ���͵ζ����� һ�� ʵ��Ŀ��
1. �˽�����˫ָʾ�����ⶨNa2CO3��NaHCO3������ԭ���ͷ����� 2. ѧϰ�òα���Һȷ���յ�ķ����� 3. ��һ���������ζ����������� ���� ʵ��ԭ����
��ϼ���NaCO3��NaOH��NaHCO3��Na2CO3�Ļ������ⶨͬһ�������и���ֵĺ���������HCl����Һ�ζ������ݵζ�������pHֵ�仯�������ѡ�÷�̪�ͼ���Ϊָʾ��������֮Ϊ��˫ָʾ��������
����ϼ�����Na2CO3��NaOH��ɣ���һ�ȵ���ʱ����Ӧ���£�
HCl+NaOH?NaCl+H2O
HCl+Na2CO3?NaHCO3+H2O
�Է�̪Ϊָʾ������ɫpH��ΧΪ8.0��10.0������HCl����Һ�ζ���
��Һ�ɺ�ɫǡ�ñ�Ϊ��ɫ�����ʱ�����ĵ��������Һ�����ΪV1��mL����
�ڶ��ȵ���ķ�ӦΪ�� �� HCl+NaHCO3?NaCl+CO2��+H2O �Լ���Ϊָʾ������ɫpH��ΧΪ3.1��4.4��,��HCl����Һ������Һ�ɻ�ɫ��Ϊ��ɫ�����ĵ��������ҺΪV2��mL����
��V1��V2ʱ������ΪNa2CO3��NaOH�Ļ����к�Na2CO3�����ĵ�HCl����ҺΪ2V1��mL�����к�NaOHʱ�����ĵ�HCl��ӦΪ��V1-V2��mL���ݴˣ�����û�ϼ���Na2CO3��NaOH�ĺ�����
��V1��V2ʱ������ΪNa2CO3��NaHCO3�Ļ�����ʱ�к�Na2CO3���ĵ�HCl����Һ�����Ϊ2V1mL���к�NaHCO3���ĵ�HCl����Һ�����Ϊ��V2-V1��
mL������û�ϼ���Na2CO3��NaHCO3�ĺ�����
˫ָʾ�����У�һ�������÷�̪�����ü���ָʾ���������Է�̪��ָʾ��ʱ����ɫ����ɫ�ı仯���������Ҳ��ѡ�üӺ�-����������ָʾ�����Ӻ�ı�ɫ��ΧΪ6.7���ƣ���8.4���죩����������ı�ɫ��ΧΪ8.0���ƣ���9.6����������Ϻ�ı�ɫ����8.3����ɫΪ��ɫ����ɫΪ��ɫ�����ָʾ����ɫ�������������Һ�ζ���Һ����ɫ��Ϊ�ۺ�ɫ����Ϊ�յ㡣
���� ���� ����ȫ��
��ϼ�ķ���
һ��ʵ��Ŀ�ģ�1��ѧ����˫ָʾ�������ϼ����ֵ���ɺͺ�����
2���������ֲ��ζ���ԭ����
3��ѧ��������ֵĺ�����
����ʵ��ԭ�����ڻ�ϼ����Һ���ȼ����ָ̪ʾ������HCl����Һ�ζ��� ��ɫ����ʱ��Һ������NaOH��ȫ���кͣ�Na2CO3Ҳ���ζ� NaHCO3,��Ӧ���£�
NaOH+HCl=NaCl+H2O
Na2CO3+HCl=NaCl+NaHCO3
��ζ����ΪV1(mL)���ټ������ָʾ����������HCl�� ��Һ�ζ�����Һ�ɻ�ɫ��Ϊ��ɫ��Ϊ�յ㡣��ʱNaHCO3���к� H2CO3�ķ�ӦʽΪ��
NaHCO3+HCl=NaCl+H2O+CO2��
���ʱ����HCl����Һ�����ΪV2(mL)������V1��V2������ ��ϼ����ɡ�
����ʵ����������Һ�ܡ���ʽ�ζ��ܡ���ƿ��ϴ����
�Լ���0.1mol��LHCl����Һ������1g��Lˮ��Һ����̪2g��L �Ҵ���Һ��
�ġ�ʵ�鲽�������1������Һ����ȡ25.00mL��ϼ���250mL��ƿ�У��� ��2��3�η�̪����0.1 mol��LHCl����Һ�ζ�����Һ�ɺ�
ɫ��Ϊ ��ɫ��Ϊ��һ�յ㣬����HCl����Һ�����V1��
2���ټ���2�μ��ȣ�������HCl����Һ�ζ�����Һ�ɻ�ɫ -1-1-1-1
��Ϊ��ɫ��Ϊ�ڶ��յ㣬���µڶ�����ȥHCl����Һ���V2��
3��ƽ�вⶨ���Σ�����V1 ��V2�Ĵ�С�жϻ�ϼ����ɣ����� ����ֵĺ�����
�塢ע�����1����ϼ�ϵNaOH��Na2CO3���ʱ����ָ̪ʾ�����ʵ���Ӽ� ������ζ�����ȫʹNaOH�IJⶨ���ƫ�ͣ�Na2CO3�IJⶨ�� ��ƫ�ߡ�
���� ���� ����ȫ��
��ϼ�ķ���(˫ָʾ����)
����ˣ���Τ��
1 ʵ��Ŀ��
����(1) �˽����ζ�����Ӧ�á�
����(2) ����˫ָʾ�����ⶨ��ϼ��ԭ������ɳɷݵ��б��㷽����
2 ʵ��ԭ��
������ϼ���Na2CO3�� NaOH ��Na2CO3��NaHCO3�Ļ������ⶨͬһ�������и���ݵĺ���������HCl����Һ�ζ���ѡ�����ֲ�ָͬʾ���ֱ�ָʾ��һ���ڶ���ѧ������ĵ�����ݵ���������ѧ������ʱ���ĵ�HCl����Һ�����������б���������ɼ��������ݺ�����
�����ڻ�ϼ������м����ָ̪ʾ������ʱ��Һ�ʺ�ɫ����HCl����Һ�ζ�����Һ�ɺ�ɫǡ�ñ�Ϊ��ɫʱ������Һ������NaOH��ȫ���кͣ�Na2CO3���к͵�NaHCO3������Һ�к� NaHCO3����δ���ζ�����Ӧ����:
NaOH + HCl = NaCl + H2O
Na2CO3 + HCl = NaCl + NaHCO3
������ζ���ȥ��HCl����Һ�����Ϊ V1(mL) ���ټ������ָʾ����������HCl����Һ�ζ�����Һ�ɻ�ɫ��Ϊ��ɫ����ʱ��Һ�е� NaHCO3 (����Na2CO3��һ�����к����ɵģ����������к��е�)���кͳ�CO2��H2O��
NaHCO3 + HCl = NaCl + CO2 + H2O
������ʱ�������ĵ�HCl����Һ(����һ�����㵽�ڶ����������ĵ�)�����ΪV2(mL)��
������ V1 > V2 ʱ������ΪNa2CO3��NaOH�Ļ����к�Na2CO3����HCl�Ƿ���������ģ���������Ӧ����ȡ����ζ�Na2CO3�����ĵ�HCl�����Ϊ2V2 �����к� NaOH �����ĵ� HCl�����Ϊ(V1 �CV2) ���ʼ���NaOH��Na2CO3�ĺ�����ʽӦΪ:
���� ���� ����ȫ��
�� ʵ��һ��NaOH��HCl����Һ�����Ƽ��Ƚϵζ�
1.HCl��NaOH����Һ�ܷ���ֱ�����Ʒ����ƣ�Ϊʲô��
������NaOH���������տ����е�CO2��ˮ�֣�ŨHCl��Ũ�Ȳ�ȷ����������HCl��NaOH����Һʱ������ֱ�ӷ���
2.����������Һʱ��Ϊʲô����Ͳ��ȡHCl����̨�ӳ�ȡNaOH��S���������������ܺͷ�����ƽ��
�������������ڱ���ȡ�費ͬ�����������������ƽ������ȷ��ȡһ�����ľ��ܺ�����������HCl��Ũ�Ȳ����� NaOH������CO2��ˮ�֣�����ֻ��Ҫ����Ͳ��ȡ ����̨�ӳ�ȡNaOH���ɡ�
3.����Һװ��ζ���֮ǰ��ΪʲôҪ�ø���Һ��ϴ�ζ���2��3�Σ�����ƿ�Ƿ�Ҳ���ø���Һ��ϴ���ɣ�Ϊʲô��
��Ϊ�˱���װ���ı���Һ��ϡ�ͣ�����Ӧ�øñ���Һ��ϴ�ι�2��3�Ρ�����ƿ����ˮҲ����Ӱ�챻���������ı仯��������ƿ�������ñ���Һ��ϴ���ɡ�
4.�ζ����ٽ��յ�ʱ�����εIJ������������еģ�
�𣺼����εIJ�����:����ʽ�ζ��ܵ���������ת�����ʽ�ζ��ܵ��齺�����ɶ���ʹ�����Һ���ڹܿڣ�����ƿ�ڱ���ܿڽӴ���ʹҺ������������ϴƿ�Դ�ˮ���¡�
������ʵ�����NaOH��Һ�����Ƽ�ʳ�ð״�����ȵIJⶨ
1.��μ����ȡ�����ڱ���������ػ�Na2CO3��������Χ���Ƶ�̫���̫�ٶԱ궨�к�Ӱ�죿
�������ڵζ������У�Ϊ�˼��ٵζ��ܵĶ�����һ�����ı���Һ�����Ӧ��20��25ml֮�䣬��ȡ����Ĵ�Լ����Ӧ����ʽ��ã�
���� ��������ʳƵ�̫�࣬�����Ƶı���Һ��Ũ������һ�λ��ι�������ɵ����ͽϴ�ȡ�����ʵ���Ҳ����̫�٣���Ϊÿһ�ݻ����ʶ�Ҫ�������γ��������ÿ����±0.1mg������ÿ�ݾͿ�����±0.2mg������ˣ���ȡ�����ʵ�����Ӧ����0.2000g����������ʹ���������������1�� ��
���� ���� ����ȫ��
