碘钟反应
2012301040010 杨平
一、实验目的
1.掌握“碘钟”反应的原理。学会运用“碘钟”反应设计动力学实验的方法。
2.测定过硫酸根与碘离子的反应速率常数.反应级数和反应活化能.
二、实验原理
在水溶液中,过二硫酸铵与碘化钾发生如下反应:
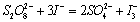 (1)
(1)
为了能够测定一定时间(Δt)内S2O82- 浓度的变化量,在混合过二硫酸铵、碘化钾溶液的同时加入一定体积已知浓度并含有淀粉(指示剂)的Na2S2O3 溶液,在式(1)进行的同时,有下列反应进行:
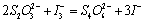 (2)
(2)
反应(2)进行得非常快,而反应(1)却缓慢得多,故反应(1)生成的I3 -立即与S2O32- 作用生成无色的S4O62- 和I? ,因此反应开始一段时间内溶液无颜色变化,但当Na2S2O3耗尽,反应(1)生成的微量碘很快与淀粉作用,而使溶液呈现特征性的蓝色。由于此时(即Δt) S2O32- 全部耗尽,所以S2O82- 的浓度变化相当于全部用于消耗Na2S2O3。由上可知,控制在每个反应中硫代硫酸钠的物质的量均相同,这样从反应开始到出现蓝色的这段时间可作为反应初速的计量。由于这一反应能显示自身反应进程,故称为“碘钟”反应。
…… …… 余下全文

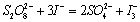 (1)
(1) 会优先和
会优先和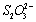 反应而被还原成
反应而被还原成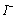 :
: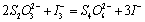 (2)
(2)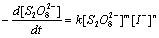 (3)
(3)