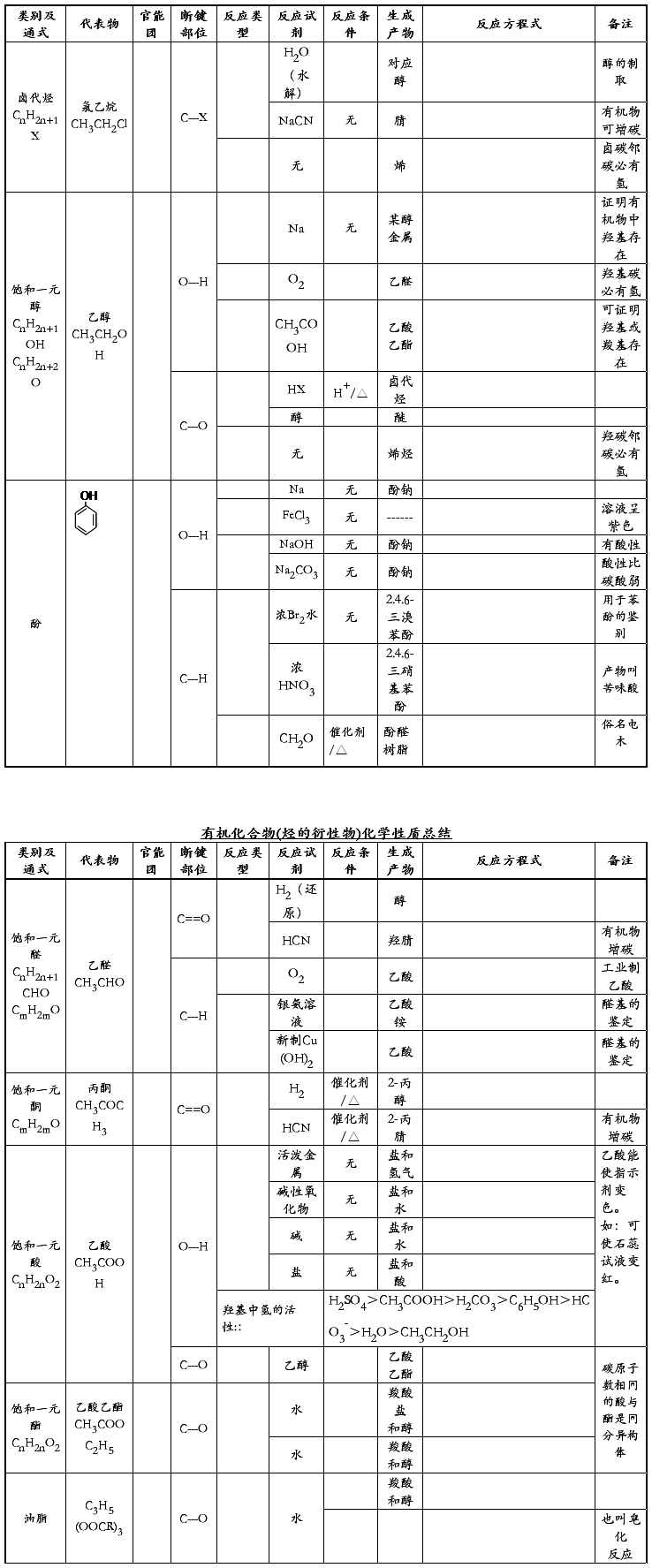
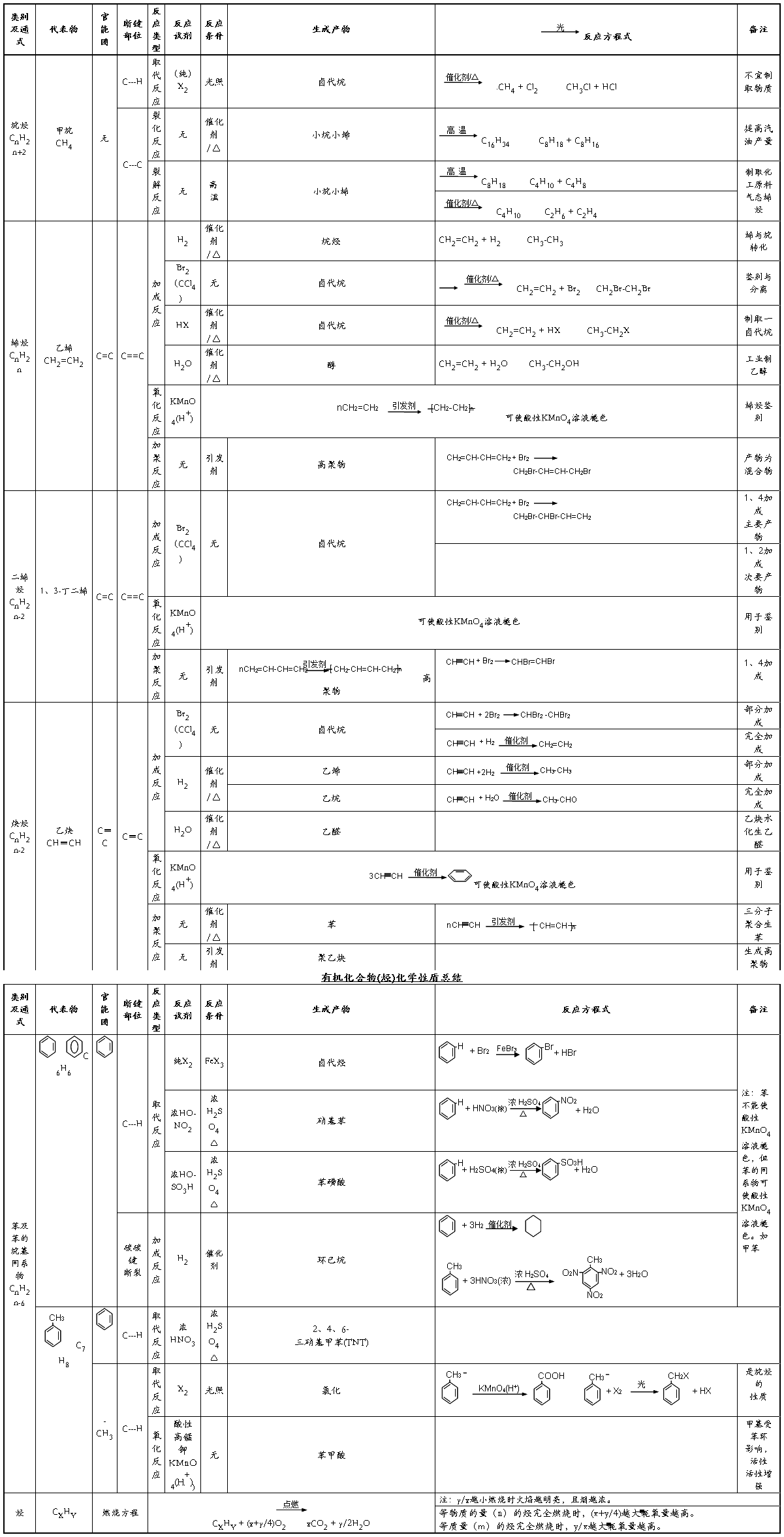
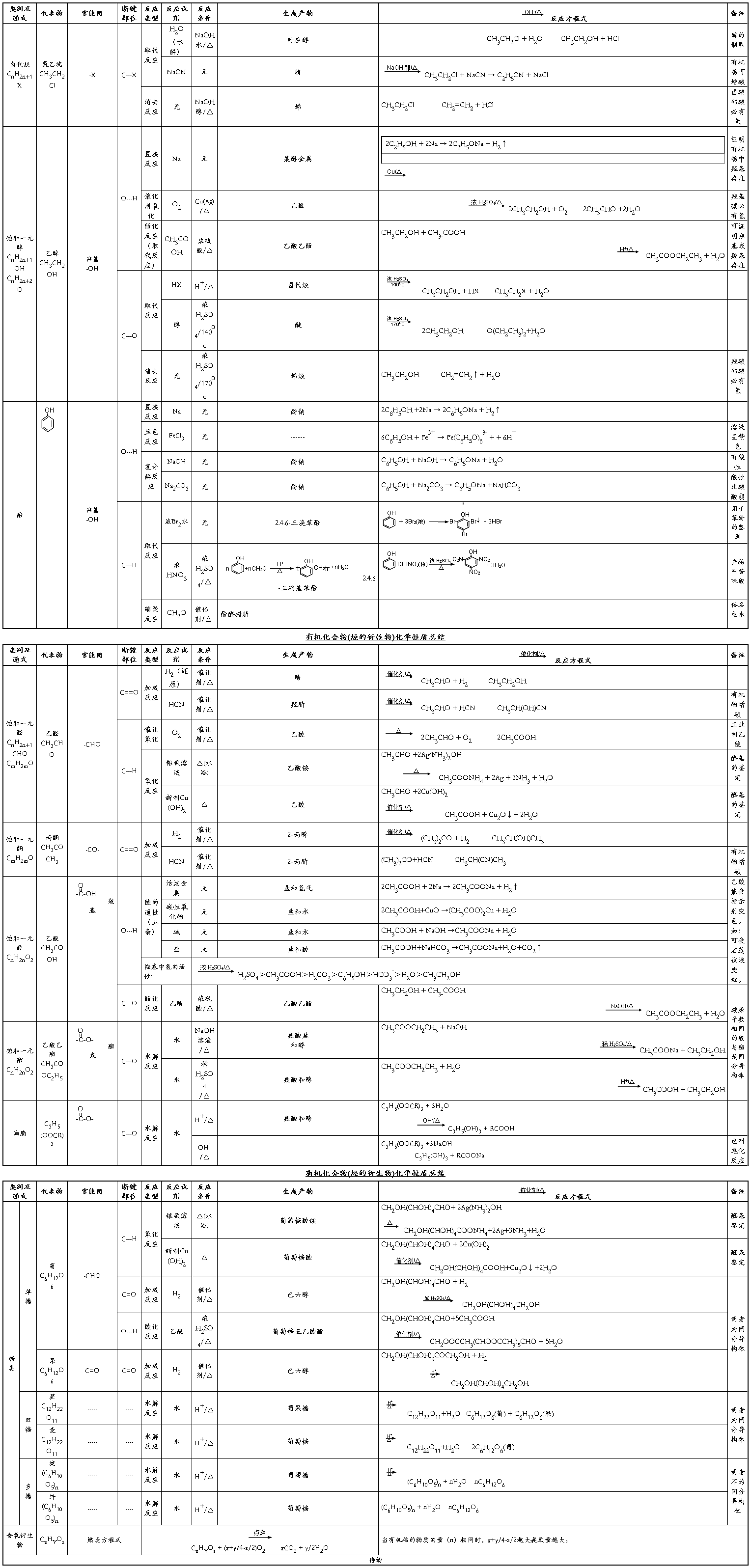
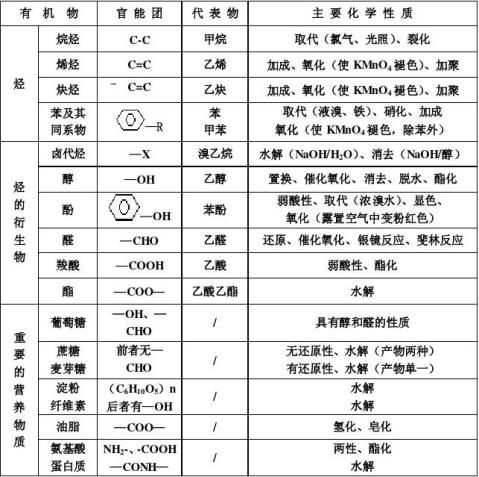
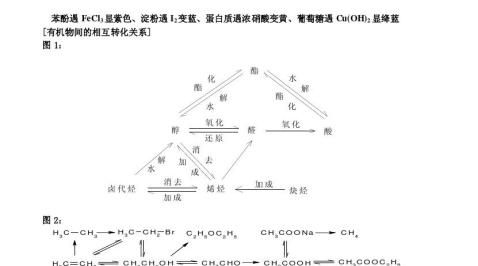
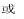有机物性质总结
一、 脂肪烃
1、 烷烃 (1) 物理性质:
①状态:在室温下,含有1~4个碳原子的烷烃为气体;常温下,含有
5~8个碳原子的烷烃为液体;含有8~16个碳原子的烷烃可以为固体,也可以为液体;含有17个碳原子以上的正烷烃为固体。
②密度:烷烃的密度随相对分子质量增大而增大,这也是分子间相互
作用力的结果,密度增加到一定数值后,相对分子质量增加而密度变化很小。且均小于水的密度。
③熔点、沸点:同类烃中,碳原子个数越多,熔点和沸点越高;碳原
子个数相同时,支链越多,熔点和沸点就越低。
④溶解性:可溶于非极性溶剂如四氯化碳、烃类化合物中,不溶于极
性溶剂,如水中。
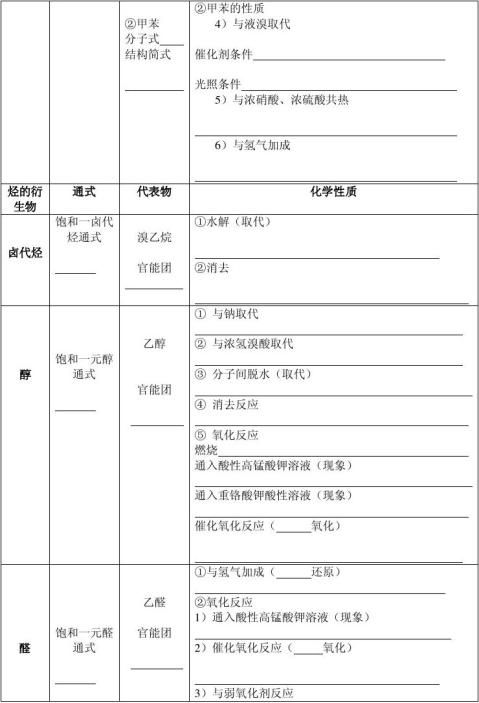
(2) 化学性质:(以甲烷为例)
①氧化反应:CH4+2O2→CO2+2H2O(燃烧)
②取代反应:CH4+Cl2→(光照)CH3Cl(气体)+HCl
CH3Cl+Cl2→(光照)CH2Cl2(油状物)+HCl CH2Cl2+Cl2→(光照)CHCl3(油状物)+HCl CHCl3+Cl2→(光照)CCl4(油状物)+HCl
2、 烯烃
(1)物理性质:C2~C4烯烃为气体;C5~C18为易挥发液体;C19以上固体。
随着相对分子质量的增加,沸点和密度升高。相同碳原子个数的烷烃和烯烃,烯烃沸点比烷烃高
(2)化学性质:(以乙烯为例)
①氧化反应:1、CH═CH+3O→2CO+2HO(燃烧)2、使酸性高猛酸钾
2
2
2
2
2
溶液褪色。
②加成反应: CH2═CH2+Br2→CH2Br—CH2Br(常温下使溴水褪色)
CH2═CH2+HCl—催化剂、加热→CH3—CH2Cl(制氯乙烷) CH2═CH2+H2O—催化剂、170℃→CH3CH2OH(制酒精) ③加聚反应:nCH2═CH2→-[CH2—CH2]-n (制聚乙烯)
…… …… 余下全文