高中化学知识点总结
必修一
引言
1、知道化学科学的主要研究对象和发展趋势
2、能列举一些对化学科学发展有重大贡献的科学家及其成就
3、知道化学是在分子层面上认识物质和合成新物质的一门科学
4、了解物质的组成、结构和性质和关系
5、认识化学变化的本质
第一章 从实验学化学
第一节 化学实验的基本方法
1、能识别化学品安全使用标识。 2、能记录实验现象和数据,完成实验报告。
3、认识实验方案、条件控制、数据处理等方法。
4、学会运用以实验为基础的实证研究方法。
5、学会分离、提纯实验方法;掌握过滤和蒸发、蒸馏和萃取等基本实验操作;
6、学会NH4+、Fe3+、Cl-、SO42-、CO32-等常见离子的检验方法
第二节 化学计量在实验中的应用
1、物质是度量物质所含微粒多少的物理量,并通过物质的量建起宏观和微观量的关系
2、物质的量及其单位的含义,明确1摩尔的含义:
3、能进行物质的量与微观粒子数之间的换算。
4、知道、气体摩尔体积以及物质的量浓度的含义。
5、能进行物质的量与物质质量、标准状况下气体体积、溶质的物质的量浓度之间的换算。
6、能利用物质的量及其相关关系定量上认识化学反应,并进行简单计算;
7、初步学会配制一定物质的量浓度的溶液,了解容量瓶在配制中应用。
第二章 化学物质及变化
第一节 物质的分类
1、能运用元素的观点学习和认识物质。 2、能从物质的组成和性质对物质进行分类。
3、知道胶体是一种重要的分散系,能列举一些生活中的胶体。
4、了解胶体与其他分散系的区别。
5、能运用胶体的性质(丁达尔现象),解释简单的实验现象和生产、生活中的实验问题。
第二节 离子反应
1、写强电解质的电离方程式。
2、识离子反应及其发生的条件;从微粒观(电离的观点)的视角认识物质在水溶液中的存在形式及所发生的反应。
…… …… 余下全文

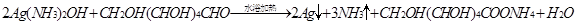 ;
; 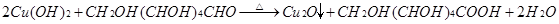 。
。 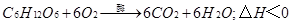 ;
; 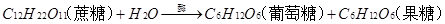
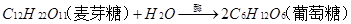
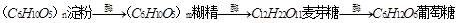 ,也可在酸的催化下逐步水解,其方程式
,也可在酸的催化下逐步水解,其方程式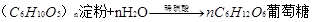 。 淀粉的特性:I2能使淀粉溶液变成蓝色。这是实验室检验淀粉或I2存在的重要原理。
。 淀粉的特性:I2能使淀粉溶液变成蓝色。这是实验室检验淀粉或I2存在的重要原理。 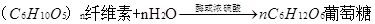 。纤维素不能作为人类的营养食物,但在人体内不可或缺,如:能刺激肠道蠕动和分泌消化液,有助于失误和废物的排泄……。
。纤维素不能作为人类的营养食物,但在人体内不可或缺,如:能刺激肠道蠕动和分泌消化液,有助于失误和废物的排泄……。 











 CO2 + 2H2O
CO2 + 2H2O CH2Cl2 + 2HCl
CH2Cl2 + 2HCl C + 2H2
C + 2H2 CH2BrCH2Br
CH2BrCH2Br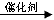 CH3CH2OH
CH3CH2OH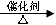 CH3CH3
CH3CH3