物质的量知识点复习
1、 摩尔
物质的量是国际规定的七个基本物理量之一,用来表示含一定数目粒子的集体,符号是n,单位是mol。
摩尔是计量原子、分子、或离子等微观粒子的物质的量的单位。 阿伏伽德罗常数是任何粒子的粒子数,符号是NA,常用6.02×1023
这个近似值。
2、 摩尔质量
1mol任何粒子或物质的质量以克为单位时,在数值上都与相对原子质量或相对分子质量相等。
摩尔质量是指单位物质的量的物质所具有的质量,符号是M,常用单位是g〃mol-1
3、 使用摩尔这个概念时应注意的事项
(1) 摩尔是物质的量单位,每摩尔物质含有阿伏伽德罗常数个粒子,
摩尔简称摩,符号mol。
(2) 摩尔的量度对象是构成物质的基本粒子,这里的“粒子”是指
“基本单元”,这个基本单元可以是分子、原子、离子、电子、质子、中子等单一粒子,也可以是这些粒子的特定组合。如1molCaCl2可以说含1molCa2+,2molCl-或3mol阴、阳离子,或
含54mole-等。
(3) 摩尔概念只适用微观不适用于宏观。
(4) 使用摩尔表示物质的量时,应该用化学式指明粒子种类,而不
是使用该粒子的中文名称。
4、 气体摩尔体积
当分子数目相同时,气体体积大小主要决定于气体分子间的距离。要比较一定质量的气体体积,必须在相同温度和压强下进行。
气体摩尔体积:单位物质的量气体所占的体积,符号为Vm,单位是L/mol或m3/mol。
标准状况下气体的摩尔体积:标准状况下,即温度为0℃,压强为101Kpa时,1mol任何气体所占的体积都约是22.4L。
5阿伏伽德罗定律及推论:
根据气体状态方程PV=nRT=mRT可以得到以下定律和推论: M
(1) 同温同压下,相同体积的任何气体都含有相同数目的分子。(阿
伏伽德罗定律)
(2)同温同压下的不同气体,其体积之比等于物质的量之比,等于所含粒子数目之比。V1n1N1?? V2n2N2
…… …… 余下全文

 ,
,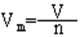
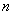
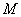
 所含的原子数作为摩尔的基准。即每摩尔物质含有阿伏加德罗常数个微粒,近似值为6.02×1023。
所含的原子数作为摩尔的基准。即每摩尔物质含有阿伏加德罗常数个微粒,近似值为6.02×1023。
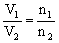 。
。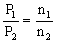 。
。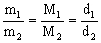 。
。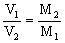 。
。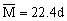 (∴d=
(∴d=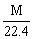 )(1mol的物质所具有的质量)
)(1mol的物质所具有的质量)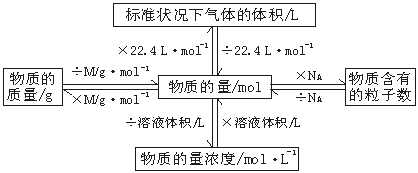
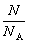
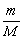 M=
M=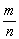 m=M·n
m=M·n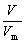 n=
n=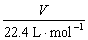 (标准状况) Vm =
(标准状况) Vm = 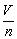 V=
V=
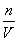 n=c·V
n=c·V 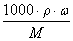 (密度的单位:g/cm3 ) n=
(密度的单位:g/cm3 ) n=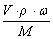
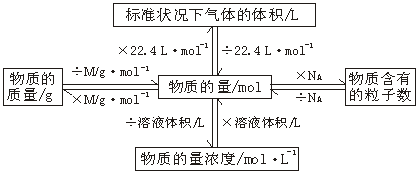
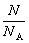
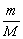 M=
M= m=M·n
m=M·n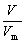 n=
n=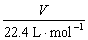 (标准状况) Vm =
(标准状况) Vm =  V=
V=
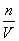 n=c·V
n=c·V 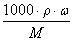 (密度的单位:g/cm3 ) n=
(密度的单位:g/cm3 ) n=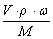
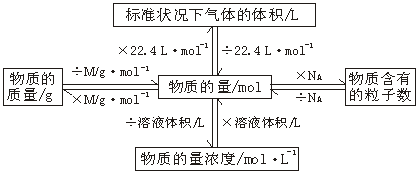
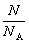
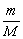 M=
M=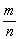 m=M·n
m=M·n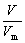 n=
n=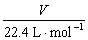 (标准状况) Vm =
(标准状况) Vm = 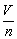 V=
V=
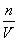 n=c·V
n=c·V 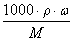 (密度的单位:g/cm3 ) n=
(密度的单位:g/cm3 ) n=
