篇二 :高中化学必修2知识点归纳总结律
高中化学必修2知识点归纳总结
第一章 物质结构 元素周期律
一、原子结构
 质子(Z个)
质子(Z个)
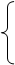 原子核 注意:
原子核 注意:
中子(N个) 质量数(A)=质子数(Z)+中子数(N)
 1.原子(
A X ) 原子序数=核电荷数=质子数=原子的核外电子数
1.原子(
A X ) 原子序数=核电荷数=质子数=原子的核外电子数
核外电子(Z个)
★熟背前20号元素,熟悉1~20号元素原子核外电子的排布:
H He Li Be B C N O F Ne Na Mg Al Si P S Cl Ar K Ca
2.原子核外电子的排布规律:①电子总是尽先排布在能量最低的电子层里;②各电子层最多容纳的电子数是2n2;③最外层电子数不超过8个(K层为最外层不超过2个),次外层不超过18个,倒数第三层电子数不超过32个。
电子层: 一(能量最低) 二 三 四 五 六 七
…… …… 余下全文
篇三 :化学必修2知识点总结
高考圈-让高考没有难报的志愿
苏教版化学必修2专题知识点
一、元素周期表
★熟记等式:原子序数=核电荷数=质子数=核外电子数
1、元素周期表的编排原则:
①按照原子序数递增的顺序从左到右排列;
②将电子层数相同的元素排成一个横行——周期;
③把最外层电子数相同的元素按电子层数递增的顺序从上到下排成纵行——族
2、如何精确表示元素在周期表中的位置:
周期序数=电子层数;主族序数=最外层电子数
口诀:三短三长一不全;七主七副零八族
熟记:三个短周期,第一和第七主族和零族的元素符号和名称
3、元素金属性和非金属性判断依据:
①元素金属性强弱的判断依据:
单质跟水或酸起反应置换出氢的难易;
元素最高价氧化物的水化物——氢氧化物的碱性强弱; 置换反应。
②元素非金属性强弱的判断依据:
单质与氢气生成气态氢化物的难易及气态氢化物的稳定性;
最高价氧化物对应的水化物的酸性强弱; 置换反应。
4、核素:具有一定数目的质子和一定数目的中子的一种原子。
①质量数==质子数+中子数:A == Z + N
②同位素:质子数相同而中子数不同的同一元素的不同原子,互称同位素。(同一元素的各种同位素物理性质不同,化学性质相同)
二、 元素周期律
1、影响原子半径大小的因素:①电子层数:电子层数越多,原子半径越大(最主要因素) ②核电荷数:核电荷数增多,吸引力增大,使原子半径有减小的趋向(次要因素) ③核外电子数:电子数增多,增加了相互排斥,使原子半径有增大的倾向
2、元素的化合价与最外层电子数的关系:最高正价等于最外层电子数(氟氧元素无正价) 负化合价数 = 8—最外层电子数(金属元素无负化合价)
3、同主族、同周期元素的结构、性质递变规律:
同主族:从上到下,随电子层数的递增,原子半径增大,核对外层电子吸引能力减弱,失电
高考圈-让高考没有难报的志愿
…… …… 余下全文
篇四 :化学必修2第一二章知识点总结
化学必修2第一二章知识点总结
★第一章
§第一节
1.元素周期表按照相对原子质量由大到小依次排列
2.化学性质相似的元素放在一个纵行
3.按照原子周期表中的顺序给元素编号,得到原子序数
5.原子序数=核电荷数=质子数=核外电子数2
6.元素周期表7个横行叫周期,每周期电子层数相同,左→右原子序数依次递增。周期序数=电子层数
7.第一(2)、二(8)、三(8)周期为短周期,其他周期为长周期
8.周期表有18个纵行.8、9、10叫第Ⅷ族,第ⅠA族(除H):碱金属元素,第ⅦA族:卤族元素,0族:稀有气体元素
9.碱金属元素与氧气、水的反应
4Li+O2=加热2Li2O
2Na+O2=加热Na2O2
2Na+2H2O=2NaOH+H2↑
2K+2H2O=2KOH+H2↑
10.碱金属元素除铯外,成银白色,比较柔软,有延展性,密度小(上→下↗),熔点低(上→下↘),导热、电性好
11.卤族元素由F2→I2颜色越来越深,密度逐渐增大,熔、沸点逐渐增高
12.卤族元素与氢气的反应
H2+F2=2HF
H2+Cl2=光照或点燃2HCl
H2+Br2=加热2HBr
H2+I2≈加热2HI
13.从F2到I2氧化性逐渐减弱,与H2的反应程度越来越不剧烈JIU,氢化物越来越不稳定
14.质量数(A)=质子数(Z)+中子数(N)≈相对原子质量
15.具有一定数目质子和中子的原子叫核素,质子数相同而中子数不同的同一元素的不同原子互称同位素
16.氕质子数1中子数0,氘质子数1中子数1,氚质子数1中子数2;它们的一氧化物分别为水、重水、超重水
§第二节
1.用n=1,2,3,4,5,6,7或K、L、M、N、O、P、Q来表示从内到外的电子层,离核近的区域内运动的电子能量低,远的高
2.同周期元素金属性↓,非金属性↑;同一主族金属性↑,非金属性↓
3.元素最高正价与最低负价之和为8
…… …… 余下全文
篇五 :人教版化学必修2有机物知识点总结
一、化石燃料
化石燃料:煤、石油、天然气
天然气的主要成分:CH4
石油的组成元素主要是碳和氢,同时还含有S、O、N等。主要成分各种液态的碳氢化合物,还溶有气态和固态的碳氢化合物
煤是有机化合物和无机化合物所组成的复杂的混合物。煤的含量是C其次H、O
 二、结构
二、结构
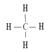
1、甲烷:分子式:CH4 结构式:
电子式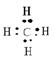 正四面体结构
正四面体结构
天然气三存在:沼气、坑气、天然气
2、化学性质
一般情况下,性质稳定,跟强酸、强碱或强氧化剂不反应
…… …… 余下全文
篇六 :人教版化学必修二第一章知识点总结
嘉祥一中高一化学 系列之知识清单
第一章 物质结构 元素周期表
第一节 元素周期表
一、周期表
原子序数 = 核电荷数 = 质子数 = 核外电子数
1、依据
横行:电子层数相同元素按原子序数递增从左到右排列
纵行:最外层电子数相同的元素按电子层数递增从上向下排列
2、结构
周期序数=核外电子层数 主族序数=最外层电子数
 短周期(第1、2、3周期)
短周期(第1、2、3周期)
 周期:7个(共七个横行)
周期:7个(共七个横行)
周期表 长周期(第4、5、6、7周期)
 主族7个:ⅠA-ⅦA
主族7个:ⅠA-ⅦA

 族:
16
个(共
18
个纵行)
副族7个:IB-
ⅦB
族:
16
个(共
18
个纵行)
副族7个:IB-
ⅦB
第Ⅷ族1个(3个纵行)
零族(1个)稀有气体元素
二.元素的性质和原子结构
(一)碱金属元素:
 1、原子结构 相似性:最外层电子数相同,都为1个
1、原子结构 相似性:最外层电子数相同,都为1个
递变性:从上到下,随着核电核数的增大,电子层数增多,原子半径增大
2、物理性质的相似性和递变性:
(1)相似性:银白色固体、硬度小、密度小(轻金属)、熔点低、易导热、导电、有展性。
(2)递变性(从锂到铯):①密度逐渐增大(K反常) ②熔点、沸点逐渐降低
结论:碱金属原子结构的相似性和递变性,导致物理性质同样存在相似性和递变性。
3、化学性质
 (1)相似性:
(1)相似性:
 4Li + O2 Li2O 2Na + O2 Na2O2
4Li + O2 Li2O 2Na + O2 Na2O2
…… …… 余下全文
篇七 :高一化学必修2有机物知识点总结
必修二有机化学知识总结
一、化石燃料
化石燃料:煤、石油、天然气
天然气的主要成分:CH4
石油的组成元素主要是碳和氢,同时还含有S、O、N等。主要成分各种液态的碳氢化合物,还溶有气态和固态的碳氢化合物
煤是有机化合物和无机化合物所组成的复杂的混合物。煤的含量是C其次H、O
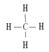 二、结构
二、结构
1、甲烷:分子式:CH4 结构式:
电子式 正四面体结构
正四面体结构
天然气三存在:沼气、坑气、天然气
2、化学性质
…… …… 余下全文
篇八 :高中化学必修2知识点归纳总结
高中化学必修2知识点归纳总结 第一章 物质结构 元素周期律
一、原子结构
质子(Z个)
原子核 注意:
中子(N个) 质量数(A)=质子数(Z)+中子数(N)
1.原子( A X ) 原子序数=核电荷数=质子数=原子的核外电子数
核外电子(Z个)
★熟背前20号元素,熟悉1~20号元素原子核外电子的排布: H He Li Be B C N O F Ne Na Mg Al Si P S Cl Ar K Ca
2.原子核外电子的排布规律:①电子总是尽先排布在能量最低的电子层里;②各电子层最多容纳的电子数是2n2;③最外层电子数不超过8个(K层为最外层不超过2个),次外层不超过18个,倒数第三层电子数不超过32个.
电子层: 一(能量最低) 二 三 四 五 六 七
对应表示符号: K L M N O P Q 3.元素、核素、同位素
元素:具有相同核电荷数的同一类原子的总称.
核素:具有一定数目的质子和一定数目的中子的一种原子.
同位素:质子数相同而中子数不同的同一元素的不同原子互称为同位素.(对于原子来说) 二、元素周期表 1.编排原则:
①按原子序数递增的顺序从左到右排列
②将电子层数相同的各元素从左到右排成一横行.(周期序数=原子的电子层数) ③把最外层电子数相同的元素按电子层数递增的顺序从上到下排成一纵行.
主族序数=原子最外层电子数
2.结构特点:
核外电子层数 元素种类
第一周期 1 2种元素
短周期 第二周期 2 8种元素
周期 第三周期 3 8种元素
元 (7个横行) 第四周期 4 18种元素
素 (7个周期) 第五周期 5 18种元素
周 长周期 第六周期 6 32种元素
期 第七周期 7 未填满(已有26种元素)
表 主族:ⅠA~ⅦA共7个主族
族 副族:ⅢB~ⅦB、ⅠB~ⅡB,共7个副族
(18个纵行) 第Ⅷ族:三个纵行,位于ⅦB和ⅠB之间
…… …… 余下全文

推荐阅读
猜你喜欢
