
本科学生实验报告
学号 姓名
学院 专业、班级
实验课程名称
教师及职称
开课学期 至 学年 学期
…… …… 余下全文
SHH-250SD型药品稳定性试验箱验证报告
(设备编号:HYS-WDX-01 )
1、验证目的
SHH-250SD型药品稳定性试验箱于20xx年初购买,主要用来考察原料药或药物制剂在温度、湿度影响下随时间变化的规律,为药品生产、包装、贮存、运输条件提供科学依据,同时可通过试验建立药品的有效期。通过验证,以文件形式记录所确认SHH-250SD药品稳定性试验箱在安装、运行、性能确认方面的要求、可接受标准;证实并描述该设备的使用目的,运行正常;成功地完成确认,证明此设备能满足稳定性试验的要求。 2 验证实施概要 2.1验证所需仪器和设备
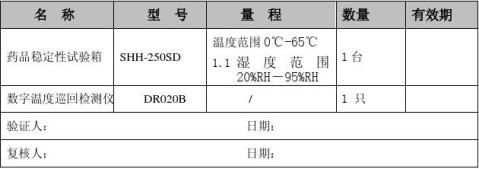
2.2 验证步骤 2.2.1 安装确认
20xx年3月5日,购进重庆永生试验仪器厂制造的型号为SHH-250SD型药品稳定性试验箱一台,放置在化验室药品稳定性试验室。20xx年3月9日,验证小组对该设备的外观、安装环境及资料进行确认。确认结果如下:
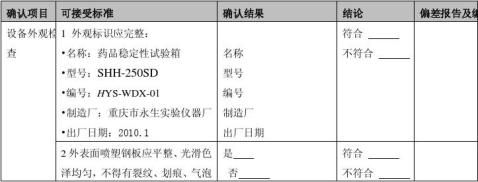
1
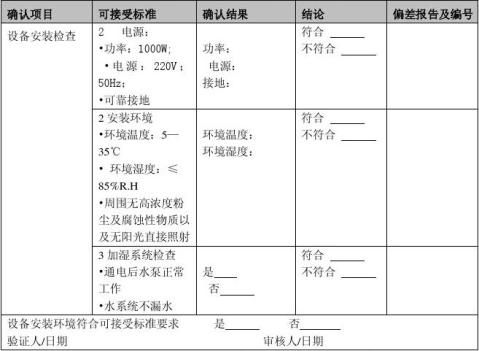
2

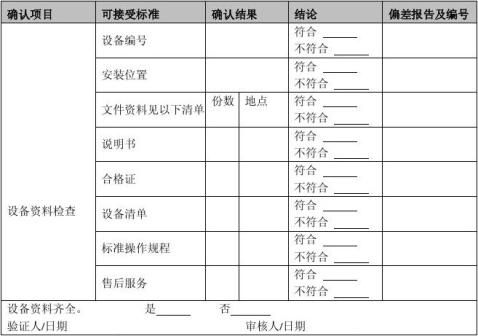

2.2.2运行确认 2.2.2.1 运行确认过程
20xx年3月5日,验证小组对SHH-250SD型药品稳定性试验箱进行了通电测试、断电测试,记录如下:
3
20xx年3月9日至3月13日,对SHH-250SD型药品稳定性试验箱的温度、相对湿度进行比对,比对记录见附件1,比对结果满足可接受标准。20xx年5月5日,由南京市计量监督检察院现场对SHH-250SD型药品稳定性试验箱进行校准,20xx年5月12日,对该设备的校准报告进行检测结果评价,满足稳定性试验要求。校准报告及评价报告见附件2、附件3。
20xx年5月5日,对SHH-250SD型药品稳定性试验箱进行空载测试,空载测试项目包括温湿度偏差试验、温湿度均匀度试验、波动度试验。将试验箱温度、湿度分别设置到40.0℃、75%RH后,将型号为DR020B的数字温度巡回检测仪按以下点布置 :温度测试点9个用0~8表示,湿度测试点3个用甲、乙、丙表示。在设备工作室内上、中、下布置9个温度测量点和3个湿度测量点,中点为0点,上下层各布4个点;各点距工作室内壁的距离为对应边长的10%;详细位置如下图:
…… …… 余下全文
戴维南定理
学号: 姓名: 成绩:
一 实验原理及思路
一个含独立源,线性电阻和受控源的二端网络,其对外作用可以用一个电压源串联电阻的
等效电源代替,其等效电压源的电压等于该二端网络的开路电压,其等效内阻是将该二端网络中所有的独立源都置为零后从从外端口看进去的等效电阻。这一定理称为戴维南定理。
本实验采用如下所示的实验电路图a
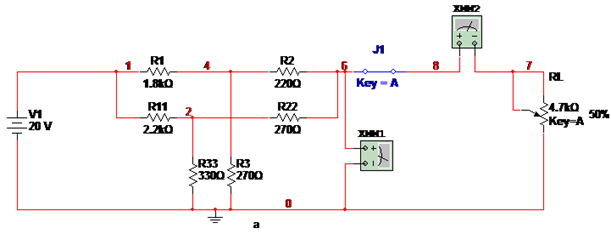
等效后的电路图如下b所示
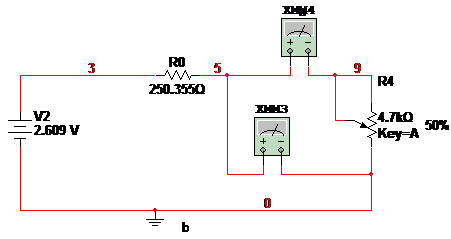
测它们等效前后的外特性,然后验证等效前后对电路的影响。
二 实验内容及结果
⒈计算等效电压和电阻
计算等效电压: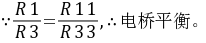 Uoc=
Uoc=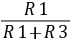 =2.6087V。
=2.6087V。
计算等效电阻:R=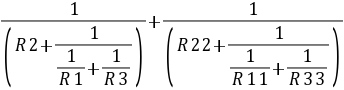 =250.355
=250.355
⒉用Multisim软件测量等效电压和等效电阻
测量等效电阻是将V1短路,开关断开如下图所示
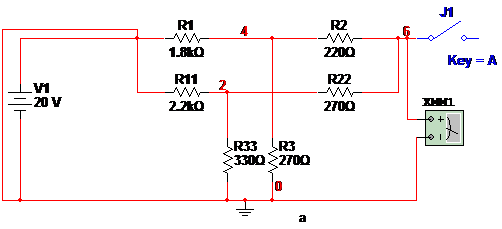
Ro=250.335
测量等效电压是将滑动变阻器短路如下图
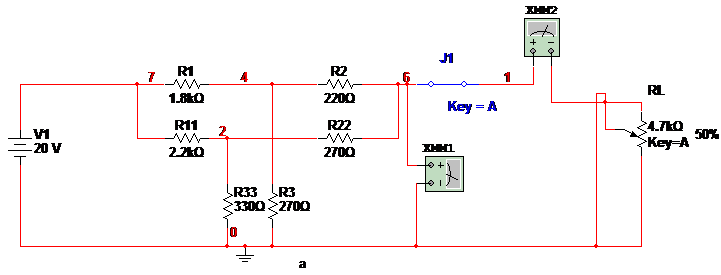
Uo=2.609V
⒊用Multisim仿真验证戴维南定理
仿真数据

原电路数据

等效电路数据
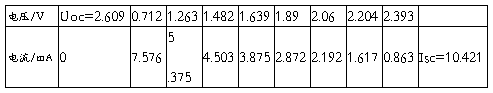
通过OriginPro 软件进行绘图,两条线一致。
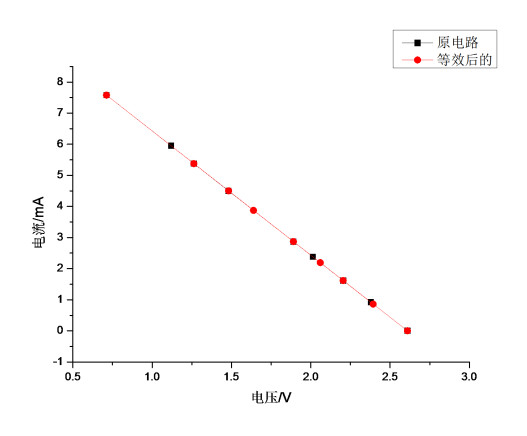
⒋在实验板上测量等效电压和等效电阻



通过OriginPro 软件进行绘图,两条线基本一致。
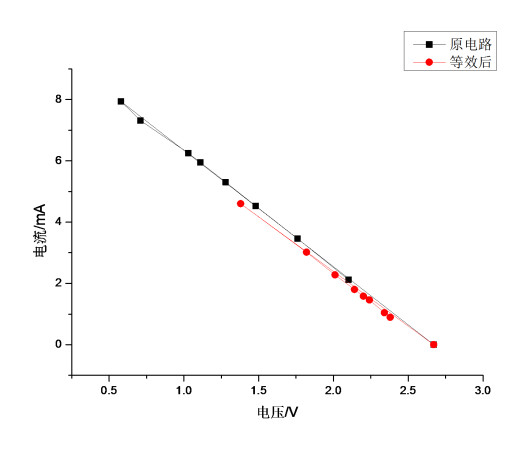
由上面的数据及图线得知等效前后不影响电路的外特性,即验证了戴维南定理。
三 结论及分析
本实验,验证了戴维南定理即等效前后的电路的外特性不改变。
进行板上实验时,存在一定的误差,而使电路线性图不是非常吻合。可能是仪器的误差,数据不能调的太准确,也可能是内接和外接都有误差。
本实验最大的收获是学会用一些仿真软件,去准确的评估实际操作中的误差。
改进的地方是进行测量时取值不能范围太窄,要多次反复测量以防实验发生错误。
…… …… 余下全文
《电子汽车衡(衡器载荷测量仪法)》
检定规程
试验
验
证报告
《电子汽车衡(衡器载荷测量仪法)》检定规程起草小组
20##年3月
《电子汽车衡(衡器载荷测量仪法)》检定规程
试验验证报告
1 目的
通过对具有代表性的电子汽车衡进行试验的方法,验证所修订的《电子汽车衡(衡器载荷测量仪法)》检定规程的科学性、合理性和可行性。
2 验证方法
在规程修订过程中,修订小组做了大量的试验,为规程的修订积累了充足的试验数据和经验,使规程得以顺利编制完成。现在,规程已基本编制完毕,为验证其科学性、合理性和可行性,选取了市场上占有率最大,且最具代表性的电子汽车衡(SCS-30、SCS-80、SCS-150),分别由福建省计量科学研究院、厦门市计量测试院和泉州市计量所使用衡器载荷测量仪,依据修订后的检定规程逐条进行试验,并按规程附录所提供的检定记录格式出具检定记录(见附录)。
3 试验数据分析
(1)对规程第6条通用技术要求进行了逐条检查,被检汽车衡完全符合要求。起草小组认为,规程所规定的通用技术要求能够涵盖电子汽车衡的技术要求,包含了完整的计量法制标志和计量器具标识要求。通用技术要求完整、充分,操作简单易行。
(2)按规程要求对汽车衡计量性能进行逐项检定,包括置零准确度、偏载、称量性能、重复性、除皮准确度和除皮后称量性能,被检汽车衡完全符合要求。
通过计量性能检定,起草小组认为规程所规定的计量性能要求、计量标准和检定方法完整、充分、可行,能够保证对电子汽车衡的各项计量性能的考核,通过检定后,能够保证电子汽车衡的计量性能的准确可靠。规程中第7条规定的检定方法严谨可靠,且充分考虑了电子汽车衡的被检状态和使用状态的一致性,具有较强的可操作性。
…… …… 余下全文
可靠性验证试验报告需要写写什么?
可靠性验证试验报告是承制方进行可靠性试验的正式记录,供订购方用来评价可靠性要求得到满足的程度。包括定期可靠性验证试验报告及最终可靠性验证试验报告。最终报告应包括关于受试产品可靠性全
面分析及其有关数据和信息的简要说明。其中包括用以说明试验数据、故障与时间的关系。
具体细节如下:
试验报告每一台受试产品的试验记录、每一次故障的故障报告以及试验故障总报告。
每一台受试产品的试验记录应包括如下内容:
(a)
受试产品标识。包括产品名称、生产厂名、产品型号、受试产品排序号;
(b)
每次观测与操作的记录。包括日期时间、工作条件、环境条件、性能参数值、工作计时器的累积读数、
观测与操作人员姓名、其他。
每一次故障的故障报告应该包括如下内容:
有试验操作人员填报的如下:
(a)
故障识别。故障出现日期和日历时间,受试产品排序号、故障涉及的零、组、部件,出故障时产品的工
作条件及环境条件,计时器的累积读数,试验操作人员姓名;
(b)
故障模式。故障的原始现象,哪些产品特性参数超出了容许限?哪些一标志是出现故障?
(c)
有关的故障分析报告要点;
(d)
对故障的类别意见;
(e)
建议的修复或纠正措施;
(f)
其他需说明的内容。
由维修人员填报的如下:
(a)
故障确认。确认的方法和仪器仪表,故障确认的观测结果;
(b)
维修说明。采取的维修措施,维修期间产品的工作时间,维修日期及时刻,维修时间、维修人员的所属
单位及姓名。
(c)
更换的零、组、部件记录。零、组、部件(元器件)的名称、型号规格、生产厂名、生产出厂日期、安
装在产品上的部位(具体到电路上的位置);
(d)
故障原因的意见;
(e)
故障分类的意见;
(f)
排除故障的纠正措施;
(g)
其他需说明的内容。
…… …… 余下全文
稳定性试验箱
验证报告

验证组织:

1.设备基本情况
1.1概述
概述
药品稳定试验箱采用镍铬丝电加热器作为加热器、二套进口原装松下小型风冷全封闭耐热型制冷压缩机作为制冷机调节温度,采用电热蒸气式加湿器(选用纯净水或蒸馏水供水)调节设备的湿度。能提供5℃~65℃的温度控制范围及20%RH~95%RH的湿度控制范围。药品稳定试验箱有效空间内各点的温度变差应小于设定温度值的±1℃,温度波动度应小于±0.3℃,湿度变差应小于设定湿度值的±2%RH。
2.验证目的: 本方案用于确认药品稳定性试验箱的安装、运行和性能确认,确保药品稳定性试验箱的安装正确,且药品稳定性试验箱在合格的安装条件下能正常运转,能提供稳定的温湿度条件。
3.职责
3.1 验证领导小组
3.2 设备科
4.验证内容
4.1 安装确认(IQ):药品稳定性试验箱对药品稳定性试验箱供应商所提供的技术资料进行核查、对药品稳定性试验箱及备品备件及安装进行检查。见附表1药品稳定性试验箱安装确认项目检查表
4.1.1 安装确认所需文件资料
4.1.2关键性仪器仪表的校验确认
4.1.3 评价仪器的安装是否符合GMP及供应商提议的要求
4.2校正:按国家有关规定每年对本仪器请有关部门由有资质的检定机构或人员对药品稳定性试验箱本体仪表及验证仪配套仪表的校准进行检查确认,
提供相应检查证书。相应记录
4.3 运行确认(OQ):进行运行确认的目的是在不使用任何试剂的条件下,确认该仪器能够达到设计要求。见附表2药品稳定性试验箱运行确认项目检查表
4.3.2 温湿度测定:通过测定箱内不同点的温湿度,来证明该设备的温度与湿度的准确度。附录3温湿度原始数据(准确性)记录
4.2.3启闭确认:药品稳定性试验箱从室温开始运行到稳定工作所需要的最少时间为启闭时间。记录温度从室温到设定温度所用的时间,并将结果记录于附录
…… …… 余下全文
文件编号:

产品包 装 材 料
验证报告
拟 制 日 期 年月日
审 核 日 期 年月日
批 准 日 期 年月日
版 号 生效日期 年月日

有限公司
产品包装材料验证报告
一、总则
1 包装材料的要求
依据:YY/T0681.1、YY/T0313 、YZB/国《体》产品注册标准。
用作制造XXXX的包装材料原料是原始材料,应有原料的来源,明确其历史和可追溯性,并受到控制,以确保成品始终能满足要求。
2 包装材料的设计必须在满足原定用途的条件下,既能够确保内包装材料的符合性,又把对使用者或患者的安全造成危害的可能性降低到最小程度。
2.1 包装材料与XXXX的相容性(即包装与医疗器材相互无不良影响):主要考虑的有:包装材料的安全性毒性的要求,拟包装的医疗器械的大小和形状,对物理和其它防护的要求,医疗器械对特殊危险例如辐射、湿气、机械性撞击,静电放射的敏感性。
…… …… 余下全文
