西安交通大学实验报告
课 程 大学化学实验 实验名称 电解质溶液及配位化合物
系 别 电气 实 验 日 期 2011年11月11日
专业班号 钱学森12 组别 二 交报告日期
…… …… 余下全文
新型稀土配位聚合物{Ln2(m-bdc)3(H2O)2}n
(Ln = Eu,Tb,Gd)的合成及掺杂后结构和荧光分析
一、 实验目的
1、 了解稀土配合物的一些合成方法后选择合适的方法进行合成稀土配合物
2、 熟悉物质的一些表征手段
3、 学会如何进行分析表征得到的数据
二、 实验原料及仪器
六水硝酸铕/钆/铽;间苯二甲酸;N,N-二甲基甲酰胺(DMF);氢氧化钾;所有原料均为市场销售的分析纯试
剂。实验用水为实验室自制去离子水
三、稀土配合物的合成过程
1、采用水-DMF 混合溶剂热方法合成稀土配合物,将 0.5 mmol 硝酸铕(0.223g)溶于 10 mL 蒸馏水中,0.5 mmol 间苯二甲酸(0.083 g)溶于 3 mL DMF 溶液中,即以 1∶ 1 的摩尔比将两种溶液混合,搅拌 45 min 后得白色均匀混合相.
2、在步骤1中搅拌的时间里,称量1.4g氢氧化钾,后用50ml的容量瓶定容得到 0.5 mol/L 的氢氧化钾溶液。
3、调白色均匀混合相 pH = 5 ~ 6。将溶液转移至 25
mL 带有聚四氟乙烯内衬的不锈钢反应釜中,在烘箱内以 170 ℃恒温加热晶化 4 天,降温到室温后,所得产物经过滤,用 DMF 充分洗涤,得到白色粉末状物质。
4、然后可进行掺杂实验,步骤同上,只是将0.5mmol硝酸铕变为0.25mmol(0.1115g)的硝酸铕和0.25mmol
硝酸钆或者硝酸铽的混合物,其他不变。
…… …… 余下全文
稀土有机配合物的制备及性能测定
北京化工大学
理学院
姓名:
班级:
学号:
时间:2014.5.8,2014.5.21
一、实验目的
1.了解稀土元素的基本知识。
2.理解光致发光的基本原理。
3.熟练掌握稀土盐和稀土有机配合物的制备方法。
4.熟悉荧光光谱仪、差热-热重分析仪和红外光谱的结构、原理和应用。
二、实验内容
1.稀土盐的制备和稀土配合物的制备。
2.稀土配合物的荧光光谱测定、紫外光谱测定和红外光谱测定。
三、实验原理
通常稀土离子与有机配体首先形成稀土配合物,然后在光照或者通电流的情况下,能量通过配体吸收,然后传递给稀土离子,稀土离子能级从激发态跃迁回基态的时候会产生发光现象。但并不是所有的稀土离子与有机配体配位形成配合物以后都能得到较好的光致发光,只有能级匹配的稀土配合物才能够发射出较强的可见光。能级匹配包含两方面的内容:(1)有机配体的三线态与稀土离子最低激发态能级的匹配程度;(2)稀土离子最低激发态与基态之间的能量差对应的光波波长是否在可见光范围。
…… …… 余下全文
稀土有机配合物的制备及性能测定
一、实验目的
1. 了解稀土元素的基本知识。
2. 理解光致发光的基本原理。
3. 熟练掌握稀土盐和稀土有机配合物的制备方法。
4. 熟悉荧光光谱仪、差热-热重分析仪和红外光谱的结构、原理和应用。
二、实验原理
1. 基本知识简介
由于稀土元素具有优异的物理和化学性能,特别是具有优异的光电磁和催化性能,已经在国民经济和现代科学技术的各个领域得到了重要的应用,所以稀土元素被誉为新材料的宝库。我国是稀土资源大国,仅目前发现的包头稀土储量就占世界稀土含量的90%以上,对稀土资源进行深度加工制成高附加值的新型功能材料具有重要的意义。尤其是徐光宪院士稀土分离技术的工业化使得稀土的价格大大下降,这更为稀土的发展创造了优越条件。
☆稀土元素的发光
稀土元素在元素周期表中主要包括从57-71号的15种元素(La,Ce,Pr,Nd,Pm,Sm,Eu,Gd,Tb,Dy,Ho,Er,Tm,Yb,Lu),也包括21号Sc和39号Y元素。对于前面15种元素来说,都含有4f轨道,具有镧系收缩现象。稀土离子因为存在着4f轨道,所以能级结构非常复杂,有些能级之间的跃迁就会产生发光现象。单独的稀土离子一般来说很难发出较强的光,通常都是稀土离子与有机配体首先形成稀土配合物。然后在光照或者通电流的情况下,能量通过配体吸收,然后传递给稀土离子,稀土离子能级从激发态跃迁回基态的时候会产生发光现象。
因为稀土离子各自都有不同的能级结构,所以并不是所有的稀土离子与有机配体配位形成配合物以后都能得到较好的光致发光。只有能级匹配的稀土配合物才能够发射出较强的可见光。能级匹配包含两方面的内容:(1)有机配体的三线态与稀土离子最低激发态能级的匹配程度;(2)稀土离子最低激发态与基态之间的能量差对应的光波波长是否在可见光范围。
…… …… 余下全文
一、实验目的
1. 掌握三氯化六氨合钴(III)的合成及其组成测定的操作方法, 通过对产品的合成和组分的测定,确定配合物的实验式和结构。
2. 练习三种滴定方法(酸碱滴定,氧化还原滴定,沉淀滴定)的操作。
3. 通过对溶液的配制和标定、仪器的使用、处理实验结果等提高学生独立分析能力、解决问题的综合能力。
二、实验内容——三氯化六氨合钴(III)的制备及组成的测定
Ⅰ、三氯化六氨合钴(III)的制备
(1)实验原理:
钴化合物有两个重要性质:第一,二价钴离子的盐较稳定;三价钴离子的盐一般是不稳定的,只能以固态或者配位化合物的形式存在。
显然,在制备三价钴氨配合物时,以较稳定的二价钴盐为原料,氨-氯化铵溶液为缓冲体系,先制成活性的二价钴配合物,然后以过氧化氢为氧化剂,将活性的二价钴氨配合物氧化为惰性的三价钴氨配合物。反应需加活性炭作催化剂。反应方程式:
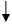 2CoCl2·6H2O + 10NH3 + 2NH4Cl + H2O2 ====2[Co(NH3)6]Cl3 + 14H2O
2CoCl2·6H2O + 10NH3 + 2NH4Cl + H2O2 ====2[Co(NH3)6]Cl3 + 14H2O
(橙黄色)
(2) 实验仪器及试剂:
仪器: 锥形瓶(250ml)、滴管、水浴加热装置、抽滤装置、温度计、蒸发皿、量筒(10ml、25ml、100ml)
…… …… 余下全文
华南师范大学实验报告
课程名称:结构实验 实验项目:磁化率的测定
1. 掌握古埃 (Gouy)磁天平测定磁化率的原理和方法。
2. 通过对一些配位化合物磁化率的测定,计算中心离子的不成对电子数,并判断d电子的排布情况和配位体场的强弱。
1、摩尔磁化率和分子磁矩 :
物质在外磁场作用下,由于电子等带电体的运动,会被磁化而感应出一个附加磁场。物质被磁化的程度用磁化率χ表示,它与附加磁场强度和外磁场强度的比值有关:
Hˊ=4πχH0 (1)
χ为无因次量,称为物质的体积磁化率,简称磁化率,表示单位体积内磁场强度的变化,反映了物质被磁化的难易程度。化学上常用摩尔磁化率 χm表示磁化程度,它与χ的关系为
χm = χM/ρ (2)
式中M、ρ 分别为物质的摩尔质量与密度。χm的单位为m 3 ?mol?1。
…… …… 余下全文
甘氨酸高钴配合物异构体的制备和鉴别
【实验目的】
①了解配合物异构体的制备和性质;
②了解紫外可见吸收光谱在鉴别异构体方面的应用。
【实验原理】
氨基酸作为配体和金属离子形成配合物时,在不同的条件下,可以氮配位、以氧配位,或以氮和氧一同配位,形成不同的键合几何异构体。例如Co(Ⅲ)离子与甘氨酸可以形成多种异构体,本实验制备Ⅰ、Ⅲ两种键合几何异构体:
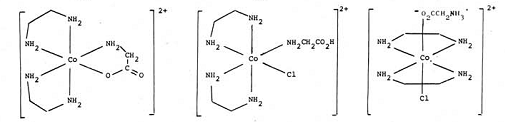
Ⅰ Ⅱ Ⅲ
紫外光谱可以用来鉴别配合物所具有的不同几何构型。在CoA4B2型配合物中1T1g态被分裂,trans-CoA4B2分裂后在300~700nm范围出现三个d-d跃迁吸收峰,cis-CoA4B2分裂后则只有两个吸收峰。
【实验仪器与试剂】
①仪器
磁力搅拌器,恒温水浴锅,蒸发皿,布氏漏斗,抽滤瓶,循环水泵,容量瓶,烧杯,紫外可见光谱仪;
②试剂
二氯化钴,甘氨酸(A.R.),氢氧化钠(A.R.),浓盐酸(A.R.),高氯酸钠(C.P.),乙二胺(>99%,A.R.),无水乙醇(A.R.),乙醚(A.R.),冰,过氧化氢(30%)。
…… …… 余下全文
磁化率的测定
(1)掌握古埃磁天平测定物质磁化率的实验原理和技术。
(2)通过对一些配位化合物磁化率的测定,计算中心离子的不成对电子数,并判断d电子的排布情况和配位体场的强弱。
物质在磁场中被磁化,在外磁场强度H的作用下,产生附加磁场。该物质内部的磁感应强度B为:
B=H+4πI=H+4πkH (1)
式中,I称为体积磁化强度,物理意义是单位体积的磁矩。式中k=I/H称为物质的体积磁化率。I和k分别除以物质的密度ρ可以得到σ和χ,σ=I/ρ称为克磁化强度;χ=k/ρ称为克磁化率或比磁化率。χm=kM/ρ称为摩尔磁化率(M是物质的摩尔质量)。这些数据都可以从实验测得,是宏观磁性质。在顺磁、反磁性研究中常用到χ和χm,铁磁性研究中常用到I、σ。
不少文献中按宏观磁性质,把物质分成反磁性物质。顺磁性物质和铁磁性物质以及亚铁磁性物质、反铁磁性物质积累。其中,顺磁性物质χm>0而反磁性物质的χm<0。
古埃法是一种简便的测量方法,主要用在顺磁测量。简单的装置包括磁场和测力装置两部分。调节电流大小,磁头间距离大小,可以控制磁场强度大小。测力装置可以用分析天平。为了测量不同温度的数据,要使用变温、恒温和测温装置。
样品放在一个长圆柱形玻璃管内,悬挂在磁场中,样品管下端在磁极中央处,另一端则在磁场强度为零处。
样品在磁场中受到一个作用力。
dF=kHAdH (2)
式中,A表示圆柱玻璃管的截面积。
样品在空气中称量,必须考虑空气修正,即
…… …… 余下全文
