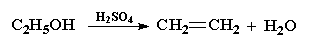工科化学实验预习报告
实验题目:三草酸合铁酸钾的制备
实验目的:1、熟悉络合物的基本知识
2、掌握合成K3[Fe (C2O4)3]·3H2O的基本原理和操作技术
实验原理:
实验以硫酸亚铁铵为原料,与草酸在酸性溶液中先制得草酸亚铁沉淀,然后再用草酸亚铁在草酸钾和草酸的存在下,以过氧化氢为氧化剂,得到铁(Ⅲ)草酸配合物,主要反应为: (NH4)2Fe(SO4)2 + H2C2O4 + 2H2O
=FeC2O4·2H2O↓+ (NH4)2SO4 + H2SO4
2FeC2O4·2H2O + H2O2 + 3K2C2O4 + H2C2O4
=2K3[Fe(C2O4)3]·3H2O
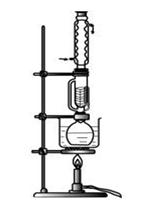
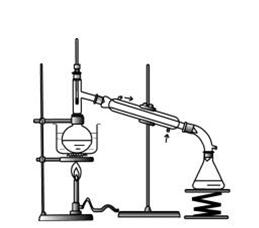
实验仪器及试剂:电子天平,抽滤装置,烧杯,酒精灯,水浴装置,表面皿。 (NH4)2Fe(SO4)2?6H2O ,H2C2O4?2H2O,
H2SO4(2 mol/L),饱和K2C2O4溶液,
乙醇(95%), H2O2(3%)
实验步骤:
1、 草酸亚铁的制备
称取适量硫酸亚铁铵固体放在烧杯中,然后加适量蒸馏水和H2SO4,加热溶解后,再加入一定量草酸溶液,加热搅拌至沸,然后迅速搅拌片刻,防止飞溅。停止加热,静置。待黄色晶体FeC2O4·2H2O沉淀后倾析,弃去上层清液,加入适量蒸馏水洗涤晶体,搅拌并温热,静置,弃去上层清液,即得黄色晶体草酸亚铁。
2、三草酸合铁(III)酸钾的制备
往草酸亚铁沉淀中,加入饱和K2C2O4溶液,313K下水浴加热,恒温下慢慢滴加H2O2溶液,沉淀转为深棕色,加热溶液至沸以去除过量的H2O2,静置一会。
然后加入草酸溶液(沉淀溶解,溶液变为翠绿色),溶液的pH值保持在4~5, 加入95%的乙醇,混匀后冷却,可以看到烧杯底部有晶体析出(翠绿色) 。晶体完全析出后,抽滤,用乙醇淋洒滤饼,抽干混合液。固体产品置于一表面皿上,置暗处晾干。称重,计算产率。
…… …… 余下全文

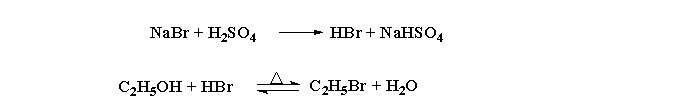
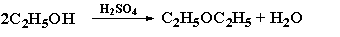 副反应:
副反应: