化学工程学院本科生专业实验报告


题 目 乙酸丁酯的合成及精制
学生姓名 ##
学 号 ##
实验组号 2 - 12
组 员 ##
…… …… 余下全文
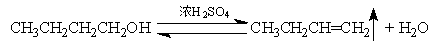
实验十:乙酸正丁酯的制备
一、实验目的
1.学习羧酸与醇反应制备酯的原理和方法。
2.学习利用恒沸去水以提高酯化反应收率的方法。
3.学习使用分水器回流去水的原理和使用方法。
二、实验原理
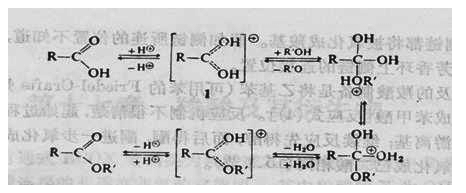
主反应式:
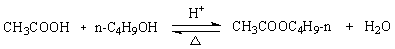
副反应式:
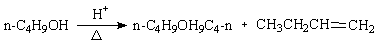
三、主要试剂及产品的物理常数:(文献值)
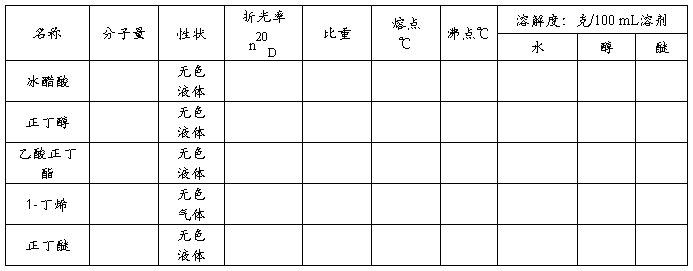
乙酸正丁酯、水及正丁醇形成二元或三元恒沸液的组成及沸点
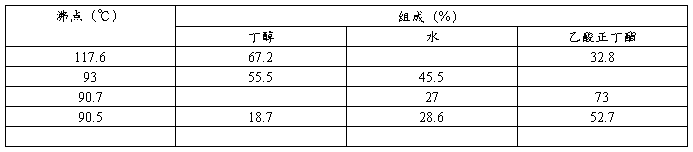
四、实验装置图
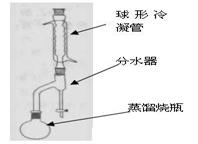
五、操作流程
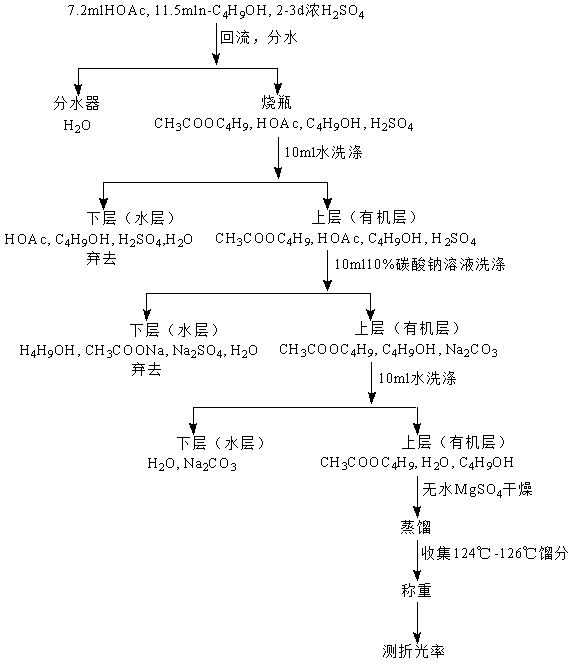
六、思考题
3、问题讨论
1)酯化反应有哪些特点?本实验是根据什么原理来提高乙酸正丁酯产率??又如何加快反应速度?
答:该反应为可逆的,增加某一反应物的量(采用丁醇过量),并使用分水器通过恒沸原理将水除去,破坏反应平衡,提高乙酸丁酯的产率。
2)在提纯粗产品的过程中,用碳酸钠溶液洗涤主要除去哪些杂质?若改用氢氧化钠溶液是否可以?为什么?
实验步骤
1)50 mL圆底烧瓶中,加11.5 mL (0.125 mol) n-BuOH, 7.2 mL CH3COOH (0.125 mol) 和3-4d浓H2SO4(催化反应), 混匀,加2颗沸石。
2)接上回流冷凝管和分水器。在分水器中预先加少量水至略低于支管口(约为1~2 cm),目的是使上层酯中的醇回流回烧瓶中继续参与反应,用笔作记号并加热至回流,不需要控制温度,控制回流速度1~2d/s。
3)反应一段时间后,把水分出并保持分水器中水层液面在原来的高度。
4)大约40 min后,不再有水生成 (即液面不再上升),即表示完成反应。
5)停止加热,记录分出的水量。
6)将分水器分出的酯层和反应液一起到入分液漏斗中,用10 mL水洗涤,并除去下层水层(除去乙酸及少量的正丁醇);有机相继续用10 mL混合物 10mL H2O 有机相(上层)10mL1有机相(上层) 10 mL 10%Na2CO3 洗涤至中性(除去硫酸);上层有机相再用10 mL 的水洗涤除去溶于酯中的少量无机盐,最后将有机层到入小锥形瓶中,用无水可硫酸镁干燥。
…… …… 余下全文

1.共沸蒸馏原理及夹带剂的作用
…… …… 余下全文
安徽工程大学
本科毕业设计(论文)开题报告
题目:年产8万吨乙酸正丁酯生产工艺设计
课 题 类 型: 设计? 实验研究□ 论文□ 学 生 姓 名: 彭炜强
学 号: 3100404236
专 业 班 级: 化工102
教 学 单 位:生物与化学工程学院 指 导 教 师: 沈凤翠 讲师
开 题 时 间: 20xx年1月3日
2014 年 3月 8 日
一、毕业设计(论文)内容及研究意义(价值)
1.1本课题研究的主要内容
乙酸正丁酯(n-Butyl Acetate,C6H12O2)又称乙酸丁酯; 醋酸正丁酯是具有水果香味的无色透明、可燃性液体,其香味比乙酸戊酯略小。它可与醇、酮、醋和大多数常用的有机溶剂互溶。天然的乙酸正丁酯主要存在于葡萄、樱桃、香蕉、苹果等植物中,且易挥发,难溶于水,能溶解油脂莘脑、树胶、松香等。其相对密度d420为0.8825,折光率n D20为1.3941,沸点为126.1℃,凝固点-77.9℃,闪点(开杯)33℃,蒸汽压(20℃)l.33kpa,汽化热309.4J/g,比热容(20℃)l.9lJ[1]。
乙酸正丁酯是一种重要的工业化学品,是化工、香料和医药等行业的重要原料,广泛用于硝化纤维、香料、医药、火棉胶、人造革和涂料等工业[2-4]。作为一种重要的化学中间体和有机溶剂,它大量用于塑料、树脂、树胶、涂料等的生产和其他化学分支。
乙酸正丁酯的生产对国民经济以及各行各业的发展有着重要的意义,也对人民生活质量的改善和提高起着重要的作用。最近几年,由于全球范围内对环境保护的要求日趋严格。人们倾向于减少甲苯、二甲苯、酮类等溶剂的用量。由于乙酸正丁酯是甲苯、二甲苯、酮类很好的取代品,其应用前景十分广阔。
1.2课题研究的意义
乙酸正丁酯作为良好的有机溶剂,主要用做硝基漆和过氯乙烯漆的稀释剂,在人造革、封皮纸及塑料工业中用作溶剂,在医药上用于红霉素生产的溶剂,还可用于印花薄膜、香料和化妆品等领域。近年随着我国涂料、塑料和胶粘剂行业的飞速发展,给乙酸正丁酯提供了巨大的消费市场,国内产量也不断增长,扩能活跃。
…… …… 余下全文
乙酸丁酯的合成及纯化
一、实验目的
1、认识酯化反应原理,掌握乙酸正丁酯的制备方法。
2、掌握共沸蒸馏分水法的原理和分水器(油水分离器)的使用。
二、实验原理
酸与醇反应制备酯,是一类典型的可逆反应:

副反应:
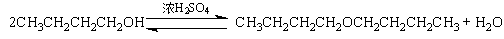
为了促使反应向右进行,通常采用增加酸或醇的浓度或连续地移去产物(酯和水)的方式来达到的。在实验过程中二者兼用。至于是用过量的醇还是用过量的酸,取决于原料来源的难易和操作上是否方便等诸因素。提高温度可以加快反应速度。
三、主要仪器与试剂
仪器 : 蒸馏装置玻璃磨口仪器、球形冷凝管、分水器、圆底烧瓶(50ml)、温度计(150℃)、锥形瓶(50ml)、烧杯(400ml)、分液漏斗、量筒(10ml、50ml)、电热套、铁架台、铁夹及十字头、铁圈、橡胶水管、天平
试剂 : 正丁醇、冰醋酸、浓硫酸、11%碳酸钠溶液、无水硫酸镁、冰块、沸石、甘油、pH试纸
四、实验内容
1、50 mL圆底烧瓶中,加11.5 mL (0.125 mol) 正丁醇, 7.2 mL冰醋酸(0.125 mol) 和3~4d浓H2SO4(催化反应), 混匀,加2颗沸石。
2、接上回流冷凝管和分水器。在分水器中预先加少量水至略低于支管口(约为1~2 cm),目的:使上层酯中的醇回流回烧瓶中继续参与反应,用笔作记号并加热至回流,不需要控制温度,控制回流速度1~2d/s。
3、反应一段时间后,把水分出并保持分水器中水层液面在原来的高度。
4、大约40 min后,不再有水生成 (即液面不再上升),即表示完成反应。
5、停止加热,记录分出的水量。
6、将分水器分出的酯层和反应液一起到入分液漏斗中,用10 m L水洗涤,并除去下层水层(除去乙酸及少量的正丁醇);有机相继续用10 m L 10% Na2CO3 洗涤至中性(除去硫酸);上层有机相再用10 m L 的水洗涤除去溶于酯中的少量无机盐,最后将有机层到入小锥形瓶中,用无水可硫酸镁干燥。
…… …… 余下全文


大学化学基础实验II实验报告
课程名称:有机化学实验
实验名称:乙酸正丁酯的制备与 折光率的测定
姓 名:张玉
学 号:1108110191
专 业:化学工程与工艺
班 级:化工113
实验日期:5/10
乙酸正丁酯的制备与折光率的测定
 实验目的
实验目的
1. 通过乙酸正丁酯的两种不同的制备方法,了解酯化反应的操作及原理。
2. 进一步熟悉分水器的使用。
3. 学习折光率的测定原理和操作方法。
 反应原理
反应原理
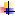 主要药品
主要药品
正丁醇 7.4g 9.2ml (0.1mol)
冰醋酸(用分水器) 6g 5.8ml (0.1mol)
浓硫酸 10%碳酸钠溶液 无水硫酸镁
实验仪器
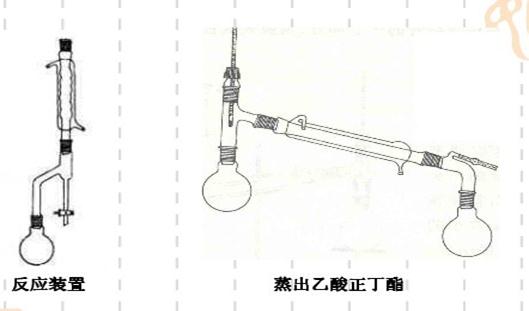
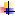 实验步骤
实验步骤
在干燥的100ml圆底烧瓶中,加入9.2ml正丁醇和5.8ml冰醋酸,再加入2至3滴浓硫酸,充分振荡,加入2粒沸石,瓶口安装分水器,分水器上装回流冷凝管,并在分水器中预先加入8ml容积的水。在石棉网上加热回流,反应一定时间后把水逐渐除去,保持分水器中水层液面在原来高度。约40min后不再有水生成,表示反应完毕。停止加热,记录分出的水量,冷却后卸下回流冷凝管,把分水器中分出的脂层和圆底烧瓶中的反应液一起倒入分液漏斗中。脂层用10%碳酸钠溶液10ml洗涤至没有酸性。分去水层,将脂层再用10ml水洗涤一次,分去水层。将脂层倒入锥形瓶中,加入少量无水硫酸镁干燥。
…… …… 余下全文
实验六 乙酸正丁酯的制备1
一、实验目的
1、认识酯化反应原理,掌握乙酸正丁酯的制备方法。
2、掌握共沸蒸馏分水法的原理和分水器(油水分离器)的使用。
3、学习有机物折光率的测定方法。
二、实验重点、难点
1、重点:掌握乙酸正丁酯的制备方法。
掌握共沸蒸馏分水法的原理和分水器(油水分离器)的使用。
2、难点:掌握共沸蒸馏分水法的原理和分水器(油水分离器)的使用。
三、实验学时
4学时
四、实验原理
酸与醇反应制备酯,是一类典型的可逆反应:
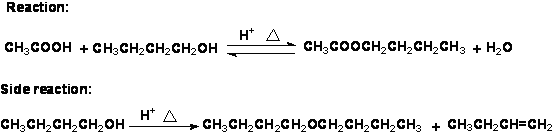
为提高产品收率,一般采用以下措施:
1、使某一反应物过量;
2、在反应中移走某一产物(蒸出产物或水);
3、使用特殊催化剂
用酸与醇直接制备酯,在实验室中有三种方法。
第一种是共沸蒸馏分水法,生成的酯和水以沸臃物的形式蒸出来,冷凝后通过分水器分出水,油层回到反应器中。
第二种是提取酯化法,加入溶剂,使反应物、生成的酯溶于溶剂中,和水层分开。
第三种是直接回流法,一种反应物过量,直接回流。
制备乙酸正丁配用共沸蒸馏分水法较好。为了将反应物中生成的水除去,利用酯、酸和水形成二元或三元恒沸物,采取共沸蒸馏分水法。使生成的酯和水以共沸物形式逸出,冷凝后通过分水器分出水层,油层则回到反应器中。
五、仪器、试剂与装置
仪器 蒸馏装置玻璃磨口仪器、球形冷凝管、分水器、圆底烧瓶(50ml)、温度计(150℃)、锥形瓶(50ml)、烧杯(400ml)、电热套、分液漏斗、量筒(10ml、50ml)、电热套、铁架台、铁夹及十字头、铁圈、橡胶水管、天平
试剂 正丁醇(11.5ml)、冰醋酸(7.2ml)、浓硫酸、10%碳酸钠溶液、无水硫酸镁、冰块、沸石、甘油、pH试纸
…… …… 余下全文
